Содержание
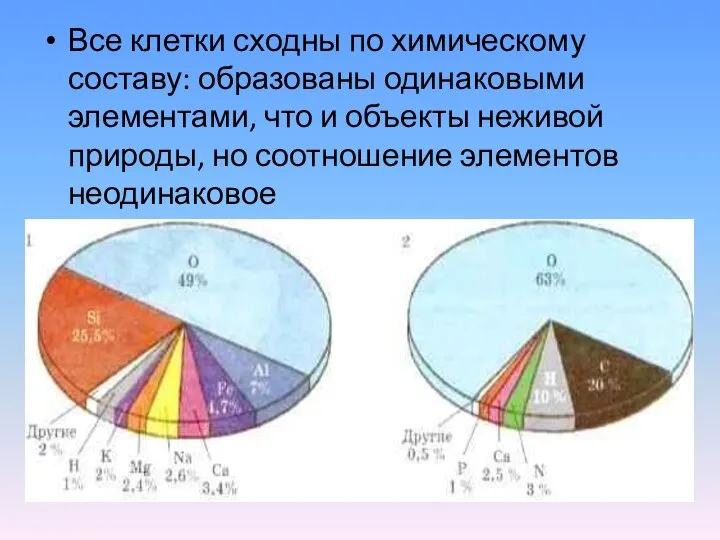
- 2. Все клетки сходны по химическому составу: образованы одинаковыми элементами, что и объекты неживой природы, но соотношение
- 3. Основу организмов составляют четыре элемента ( В организмах на их долю приходится 95%)
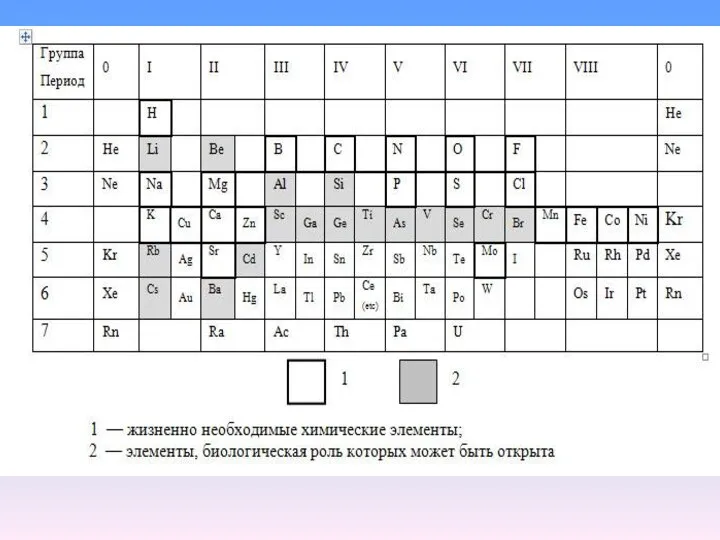
- 4. В составе клеток: более 80 химических элементов, наиболее распространены 24. Элементы, входящие в состав организмов, называют
- 6. Элементы- биогены:
- 7. Вода Содержание воды колеблется от 60 до 98 % в зависимости от типа клеток.
- 8. Свойства воды Полярность молекул Способность молекул образовывать водородные связи Большое поверхностное натяжение Высокая теплоемкость Высокие температуры
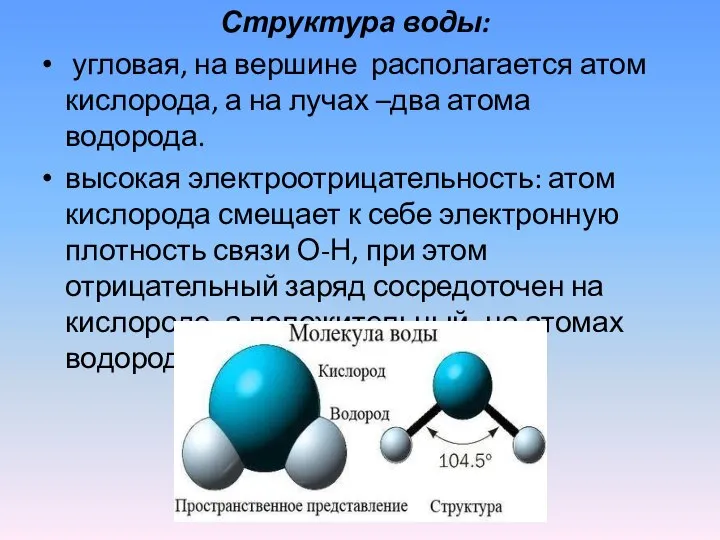
- 9. Структура воды: угловая, на вершине располагается атом кислорода, а на лучах –два атома водорода. высокая электроотрицательность:
- 10. Молекула воды - вид диполя
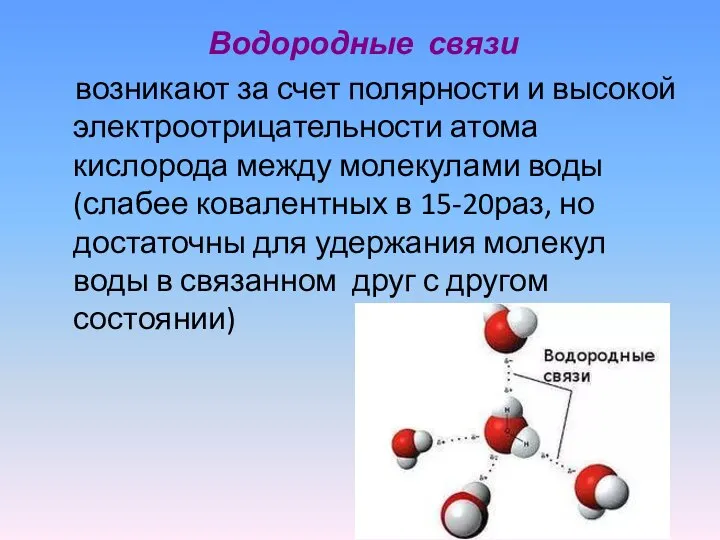
- 11. Водородные связи возникают за счет полярности и высокой электроотрицательности атома кислорода между молекулами воды (слабее ковалентных
- 12. За счет полярности и водородных связей молекулы воды способны соединяться между собой и с другими веществами.
- 13. высокая теплопроводность: тепло быстро и равномерно распределяется по всему объему воды в клетках (препятствует их перегреванию
- 14. Вода - универсальный полярный растворитель Гидрофильные вещества - хорошо растворимые в воде(соли, сахара, аминокислоты); Гидрофобные вещества-
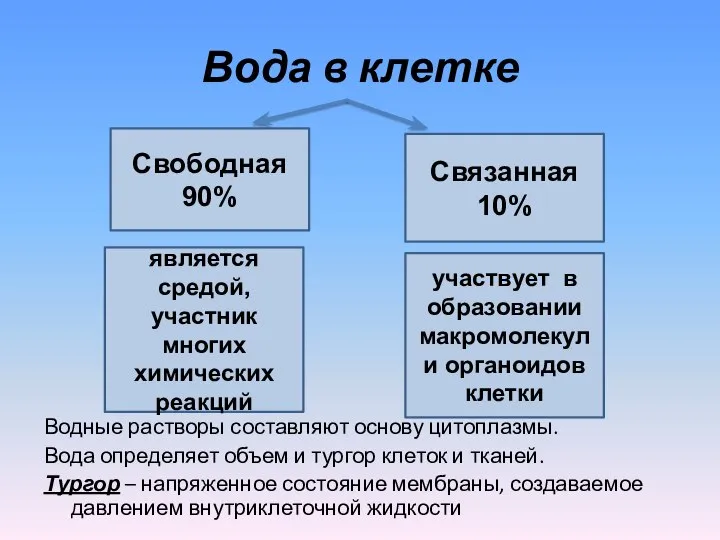
- 15. Вода в клетке Водные растворы составляют основу цитоплазмы. Вода определяет объем и тургор клеток и тканей.
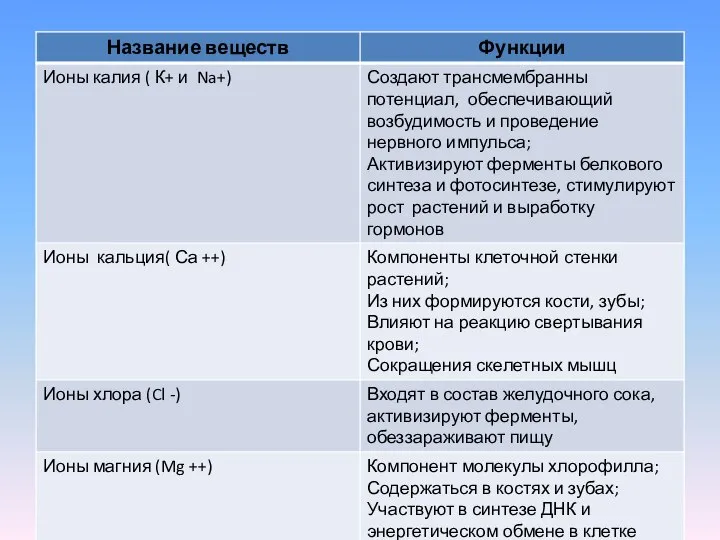
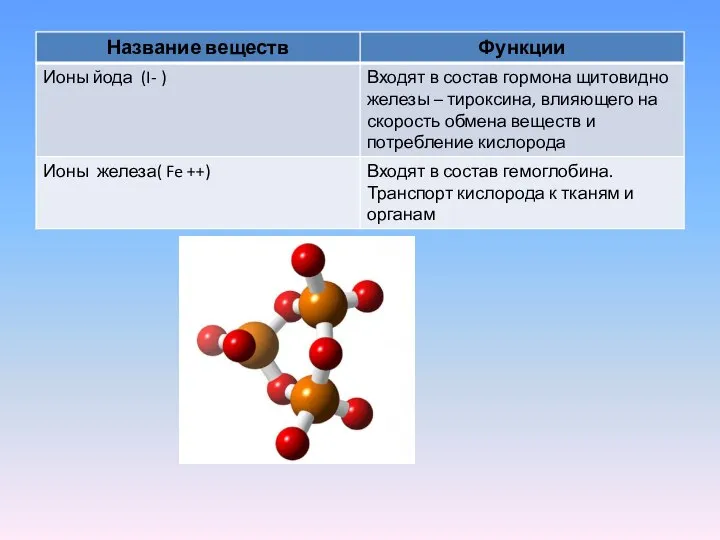
- 16. Минеральные вещества Присутствуют в клетке в виде ионов и нерастворимых солей Нерастворимые соли представлены фосфатами и
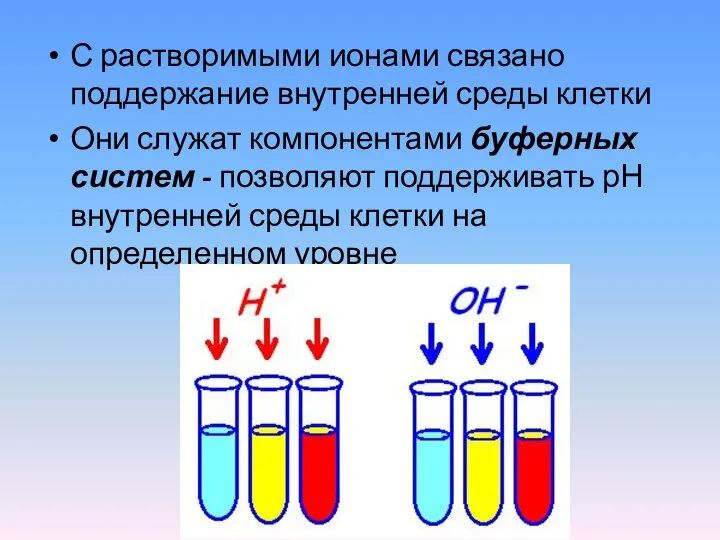
- 19. С растворимыми ионами связано поддержание внутренней среды клетки Они служат компонентами буферных систем - позволяют поддерживать
- 20. Медь (Сu) участвует в процессах кроветворения, фотосинтеза Марганец (Мn)- повышает урожайность растений, активизирует фотосинтез Бор (B)-
- 22. Скачать презентацию











 Неметаллы. Агрегатные состояния неметаллов
Неметаллы. Агрегатные состояния неметаллов Викторина Важнейшие классы веществ. Химические реакции. 8 класс
Викторина Важнейшие классы веществ. Химические реакции. 8 класс Оңай балқитын флюстерді қолдана отырып хромкенді шекемтастар алу мүмкіндігін зерттеу
Оңай балқитын флюстерді қолдана отырып хромкенді шекемтастар алу мүмкіндігін зерттеу Электролиз
Электролиз Химическое равновесие и способы его смещения
Химическое равновесие и способы его смещения Растворы, растворимость
Растворы, растворимость kristallichekaya_reshenka_vidy
kristallichekaya_reshenka_vidy Взаимодействие элементов-неметаллов между собой. 8 класс
Взаимодействие элементов-неметаллов между собой. 8 класс Кислород и сера. Их положение в ПСХЭ. Значение и применение
Кислород и сера. Их положение в ПСХЭ. Значение и применение Технологии получения и преобразования текстильных материалов. Синтетические волокна (9 класс)
Технологии получения и преобразования текстильных материалов. Синтетические волокна (9 класс) Сера и ее соединения
Сера и ее соединения Свойства жидкостей
Свойства жидкостей Закон сохранения массы
Закон сохранения массы Альдегиды и кетоны (часть 2)
Альдегиды и кетоны (часть 2) Азот
Азот Химические структуры
Химические структуры Кислород – это самый распространенный на нашей планете элемент
Кислород – это самый распространенный на нашей планете элемент ИКТ как средство реализации проблемного обучения на уроках химии
ИКТ как средство реализации проблемного обучения на уроках химии Тест по химии
Тест по химии Химическая формула. Химия 8 класс
Химическая формула. Химия 8 класс Фундаментальные механизмы биохимической адаптации
Фундаментальные механизмы биохимической адаптации Презентация на тему Ковалентная неполярная связь
Презентация на тему Ковалентная неполярная связь  Водород
Водород Понятие аналитической химии, её цели и задачи. Химический анализ, его задачи
Понятие аналитической химии, её цели и задачи. Химический анализ, его задачи Металлическая связь_1
Металлическая связь_1 Аминокислоты
Аминокислоты Изготовление искусственного янтаря
Изготовление искусственного янтаря Презентация на тему Синтетические моющие средства
Презентация на тему Синтетические моющие средства