Слайд 2Водород самый распространенный элемент во вселенной

Слайд 3История открытия
Впервые этот газ в чистом виде выделил 240 лет назад английский

химик Генри Кавендиш. Свойства полученного им газа были настолько удивительны, что ученый принял его за легендарный «флогистон», «теплород» — вещество, по канонам науки того времени определявшее температуру тел. Он прекрасно горел (а огонь считался почти чистым флогистоном), был необычайно легок, в 15 раз легче воздуха, хорошо впитывался металлами и так далее.
Слайд 4Другой великий химик, француз Антуан-Лоран Лавуазье, уже в 1787 году доказал, что

полученное Кавендишем вещество — вполне обычный, хотя и очень интересный химический элемент. Свое название он получил оттого, что при горении давал не дым, сажу и копоть, а воду.
Слайд 5Общая характеристика:
Водород занимает первое место в периодической системе (Z = 1). Он

имеет простейшее строение атома: ядро атома окружено электронным облаком. Электронная конфигурация 1s1.
В одних условиях водород проявляет металлические свойства (отдает электрон), в других — неметаллические (принимает электрон). Однако по свойствам он более сходен с галогенами, чем со щелочными металлами. Поэтому водород помещают в VII группу периодической системы элементов Д.И. Менделеева, а в I группе символ водорода заключают в скобки.
Слайд 7Водород в природе:
Водород широко распространен в природе — содержится в воде, во

всех органических соединениях, в свободном виде — в некоторых природных газах. Содержание его в земной коре достигает 0,15% ее массы (с учетом гидросферы — 1%). Водород составляет половину массы Солнца.
Слайд 8Каждую секунду Солнце излучает в космическое пространство энергию, эквивалентную примерно 4 млн т массы.

Эта энергия рождается в ходе слияния четырех ядер водорода, протонов, в ядро гелия;
Слайд 9За время существования Солнца уже около половины водорода в его центральной области
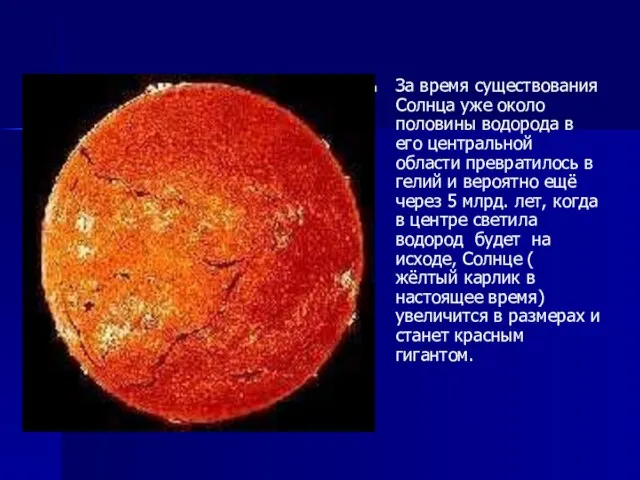
превратилось в гелий и вероятно ещё через 5 млрд. лет, когда в центре светила водород будет на исходе, Солнце ( жёлтый карлик в настоящее время) увеличится в размерах и станет красным гигантом.
Слайд 10Молекула водорода
Молекула водорода состоит из двух атомов. Возникновение связи между ними

объясняется образованием обобщенной пары электронов (или общего электронного облака):
Н:Н или Н2
Благодаря этому обобщению электронов молекула Н2 более энергетически устойчива, чем его отдельные атомы. Чтобы разорвать в 1 моль водорода молекулы на атомы, необходимо затратить энергию 436 кДж:
Н2 = 2Н, ∆H° = 436 кДж/моль
Этим объясняется сравнительно небольшая активность молекулярного водорода при обычной температуре.
Слайд 11Физические свойства.
Водород — это самый легкий газ (он в 14,4 раза легче

воздуха), не имеет цвета, вкуса и запаха. Мало растворим в воде (в 1 л воды при 20°С растворяется 18 мл водорода). При температуре — 252,8°С и атмосферном давлении переходит в жидкое состояние. Жидкий водород бесцветен.
Кроме водорода с массовым числом 1 существуют изотопы с массовыми числами 2 и 3 — дейтерий D и тритий Т.
ГазообразныйГазообразный водород может существовать в двух формах (модификациях) — в виде ортоГазообразный водород может существовать в двух формах (модификациях) — в виде орто- и пара- водорода.
В молекуле ортоводорода (т. пл. -259,20 °С, т. кип. -252,76 °С) ядерные спины направлены одинаково (параллельны), а у параводорода (т. пл. -259,32 °С, т. кип. -252,89 °С) — противоположно друг другу (антипараллельны).
Слайд 13Получение:
Вплоть до конца XIX века получение водорода было делом достаточно хлопотным. Добывали
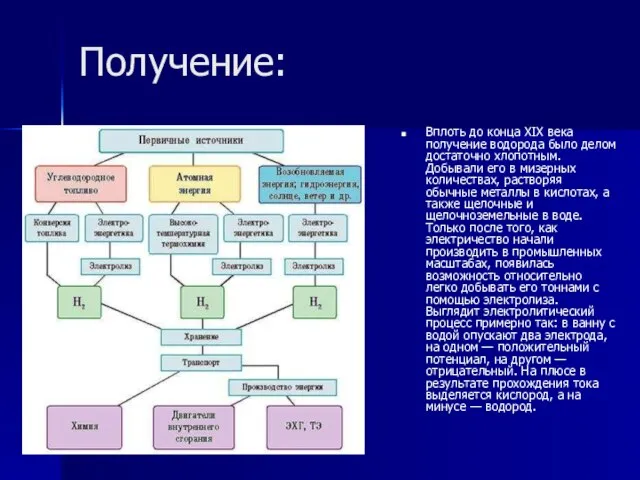
его в мизерных количествах, растворяя обычные металлы в кислотах, а также щелочные и щелочноземельные в воде. Только после того, как электричество начали производить в промышленных масштабах, появилась возможность относительно легко добывать его тоннами с помощью электролиза. Выглядит электролитический процесс примерно так: в ванну с водой опускают два электрода, на одном — положительный потенциал, на другом — отрицательный. На плюсе в результате прохождения тока выделяется кислород, а на минусе — водород.
Слайд 14Эксперимент по получению водорода из воды с помощью солнечной энергии

Слайд 15Применение:
Наработав в достаточном количестве этот легкий газ, люди сначала приспособили его для

воздушных полетов. В этом качестве первый элемент Таблицы Менделеева применяли вплоть до 1937 года, когда в воздухе сгорел крупнейший в мире, в два футбольных поля размером, заполненный водородом немецкий дирижабль «Гинденбург». Катастрофа унесла жизни 36 человек, и на таком использовании водорода был поставлен крест. С тех пор аэростаты заправляют исключительно гелием. Гелий — газ, увы, более плотный, но зато негорючий. .
Слайд 16Водородная энергетика
В недалёком будущем основным источником получения энергии станет реакция горения водорода,

и водородная энергетикаВ недалёком будущем основным источником получения энергии станет реакция горения водорода, и водородная энергетика вытеснит традиционные источники получения энергии (угольВ недалёком будущем основным источником получения энергии станет реакция горения водорода, и водородная энергетика вытеснит традиционные источники получения энергии (уголь, нефтьВ недалёком будущем основным источником получения энергии станет реакция горения водорода, и водородная энергетика вытеснит традиционные источники получения энергии (уголь, нефть и др.). При этом предполагалось, что для получения водорода в больших масштабах можно будет использовать электролиз воды.
Слайд 17Водородные автомобили
В 1979 году компания BMW выпустила первый автомобиль, вполне успешно ездивший

на водороде, при этом не взрывавшийся и выпускавший из выхлопной трубы водяной пар. В эпоху усиливающейся борьбы с вредными выхлопами машина была воспринята как вызов консервативному автомобильному рынку. Вслед за BMW в экологическую сторону потянулись и другие производители. К концу века каждая уважающая себя автокомпания имела в запаснике хотя бы один концепт-кар, работающий на водородном топливе.
Слайд 19Водород и будущее
Слова «дейтерий» и «тритий» напоминают нам о том, что сегодня

человек располагает мощнейшим источником энергии, высвобождающейся при реакции:
21Н + 31Н → 42Не +10n + 17,6 МэВ.
Эта реакция начинается при 10 млн градусов и протекает за ничтожные доли секунды при взрыве термоядерной бомбы, причем выделяется гигантское по масштабам Земли количество энергии.
Водородные бомбы иногда сравнивают с Солнцем. Однако мы уже видели, что на Солнце идут медленные и стабильные термоядерные процессы. Солнце дарует нам жизнь, а водородная бомба – сулит смерть...
















 Презентация на тему Азотная кислота и ее свойства
Презентация на тему Азотная кислота и ее свойства  Водород
Водород Получение метанола из синтез-газа
Получение метанола из синтез-газа Лекарственные средства – производные пиримидина
Лекарственные средства – производные пиримидина Chem-квест. Химический диктант
Chem-квест. Химический диктант Виготовлення водних розчинів з заданою масовою часткою розчиненої речовини
Виготовлення водних розчинів з заданою масовою часткою розчиненої речовини 9. Потомки светоносного элемента
9. Потомки светоносного элемента Химия - неотъемлемая часть жизни
Химия - неотъемлемая часть жизни Стратегия обучения решению задач по химии
Стратегия обучения решению задач по химии Вещество. Свойства вещества. Урок №2
Вещество. Свойства вещества. Урок №2 Ліпіди
Ліпіди Химия. 8 класс
Химия. 8 класс Презентация на тему Неорганические и органические основания
Презентация на тему Неорганические и органические основания  Товароведение и экспертиза пластических масс и изделий из них
Товароведение и экспертиза пластических масс и изделий из них Презентация на тему Свойства черных и цветных металлов
Презентация на тему Свойства черных и цветных металлов  Элемент протактиний
Элемент протактиний Виведення плям органічного походження
Виведення плям органічного походження Stereoselective total syntheses of guanacastepenes N and O
Stereoselective total syntheses of guanacastepenes N and O Растворы, растворимость
Растворы, растворимость Анализ воды природных источников посёлков Фруктовая и Красная Пойма городского округа Луховицы
Анализ воды природных источников посёлков Фруктовая и Красная Пойма городского округа Луховицы Вода в природе. Состав, свойства и применение воды
Вода в природе. Состав, свойства и применение воды 01_Osnovnye_ponyatia_i_zakony_khimii
01_Osnovnye_ponyatia_i_zakony_khimii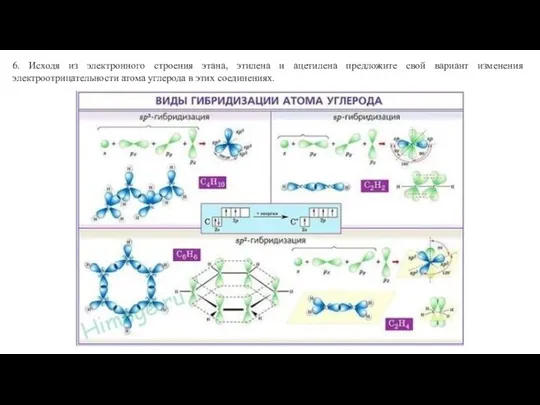 Виды гибридизации атома углерода
Виды гибридизации атома углерода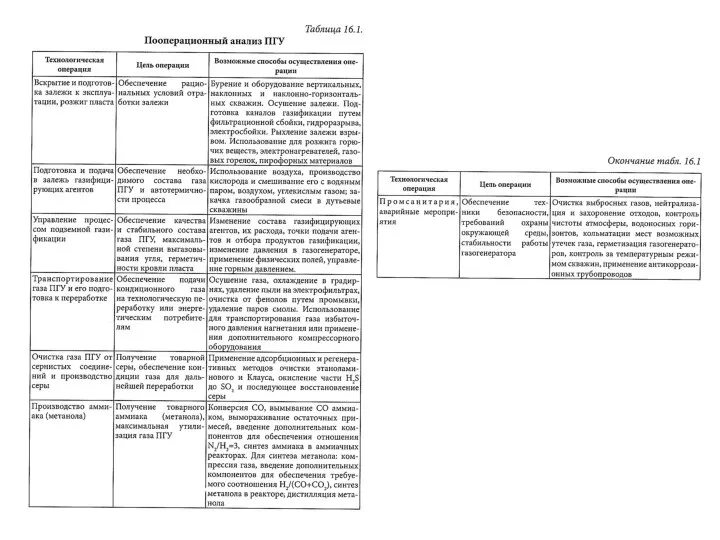 Пооперационный анализ ПГУ
Пооперационный анализ ПГУ Презентация на тему Вещества в твоей жизни
Презентация на тему Вещества в твоей жизни  Кислоты, соли
Кислоты, соли Золоторудное поле Дуэт
Золоторудное поле Дуэт Презентация по Химии "Незнайка в стране химия"
Презентация по Химии "Незнайка в стране химия"