Содержание
- 2. ХИМИЧЕСКАЯ СВЯЗЬ И КРИСТАЛЛИЧЕСКОЕ СТРОЕНИЕ. Химическая связь — явление взаимодействия атомов.
- 3. ХИМИЧЕСКАЯ СВЯЗЬ В ВЕЩЕСТВАХ
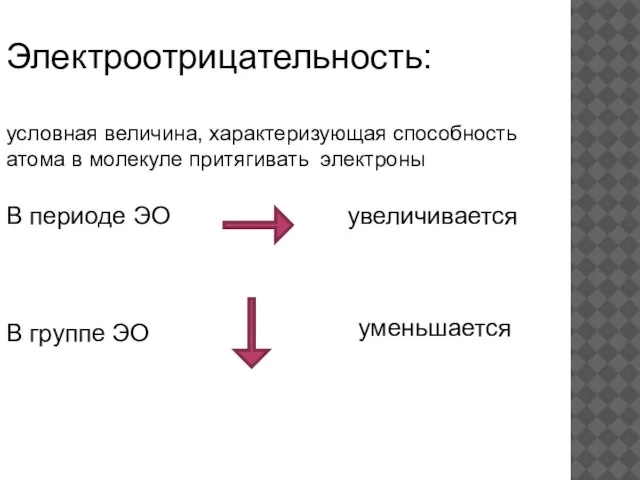
- 4. Электроотрицательность: условная величина, характеризующая способность атома в молекуле притягивать электроны В периоде ЭО увеличивается В группе
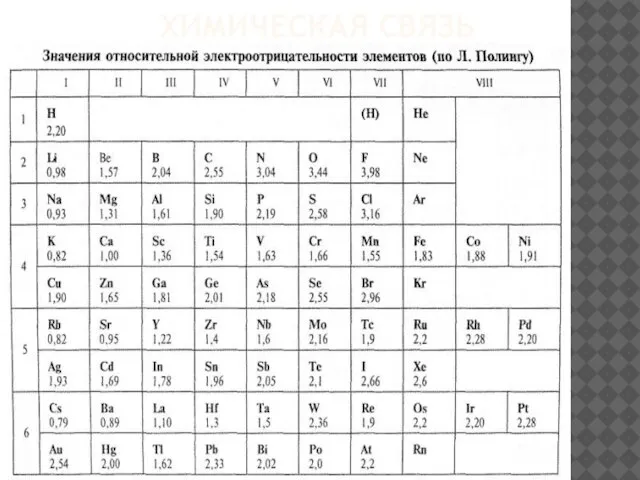
- 5. ХИМИЧЕСКАЯ СВЯЗЬ
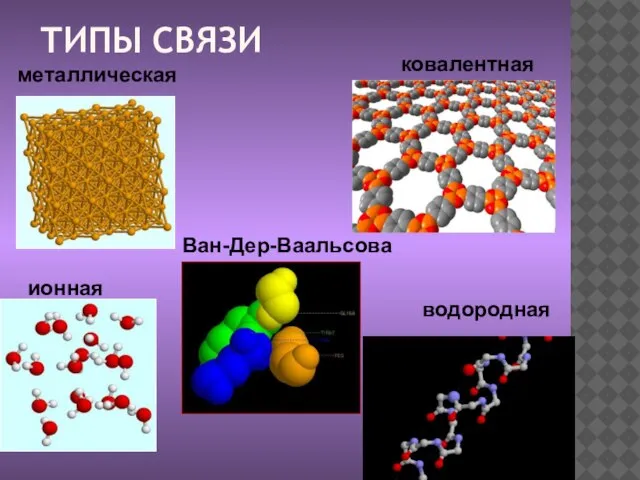
- 6. ТИПЫ СВЯЗИ металлическая ковалентная ионная Ван-Дер-Ваальсова водородная
- 7. Определение типа связи по разности ЭО элементов в соединении: ∆ ЭО 0 ковалентная неполярная связь ∆
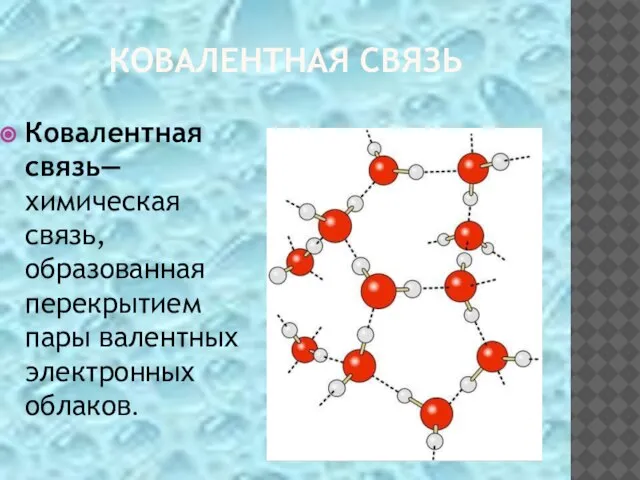
- 8. КОВАЛЕНТНАЯ СВЯЗЬ Ковалентная связь— химическая связь, образованная перекрытием пары валентных электронных облаков.
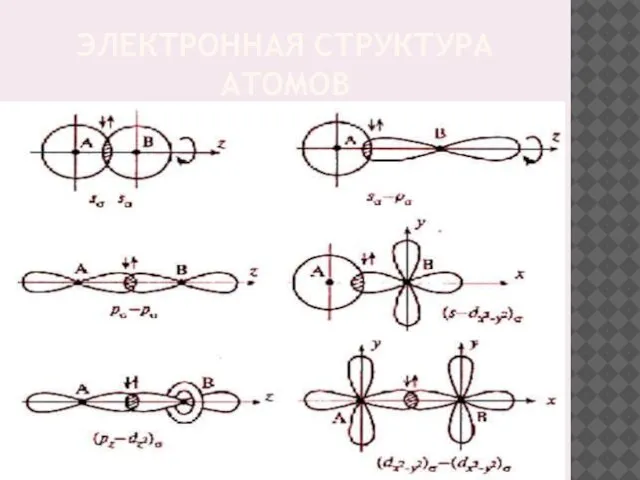
- 9. ЭЛЕКТРОННАЯ СТРУКТУРА АТОМОВ
- 10. ХИМИЧЕСКАЯ СВЯЗЬ
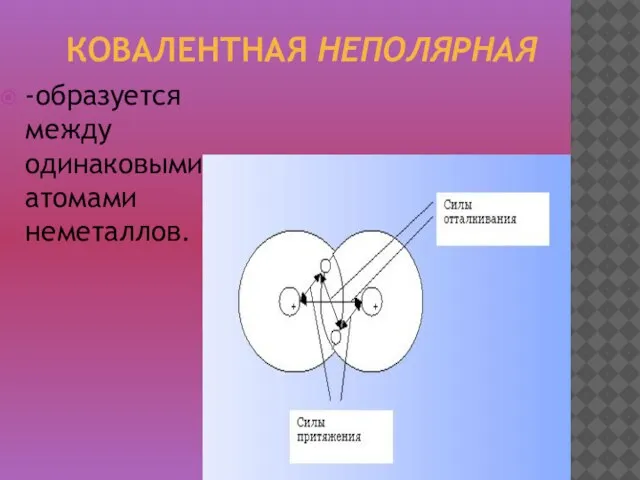
- 11. КОВАЛЕНТНАЯ НЕПОЛЯРНАЯ -образуется между одинаковыми атомами неметаллов.
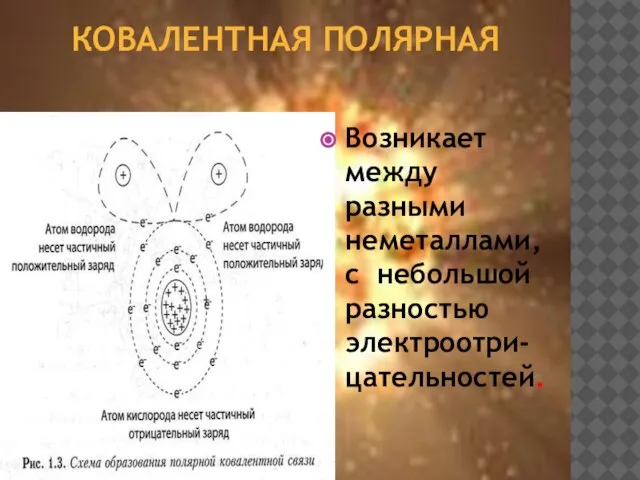
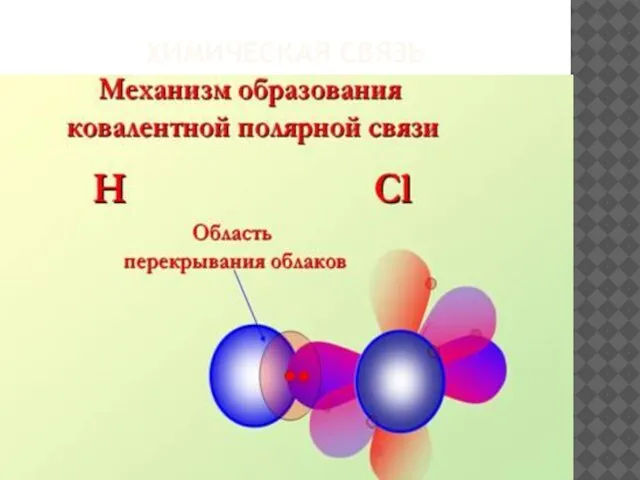
- 12. КОВАЛЕНТНАЯ ПОЛЯРНАЯ Возникает между разными неметаллами, с небольшой разностью электроотри-цательностей.
- 13. ХИМИЧЕСКАЯ СВЯЗЬ
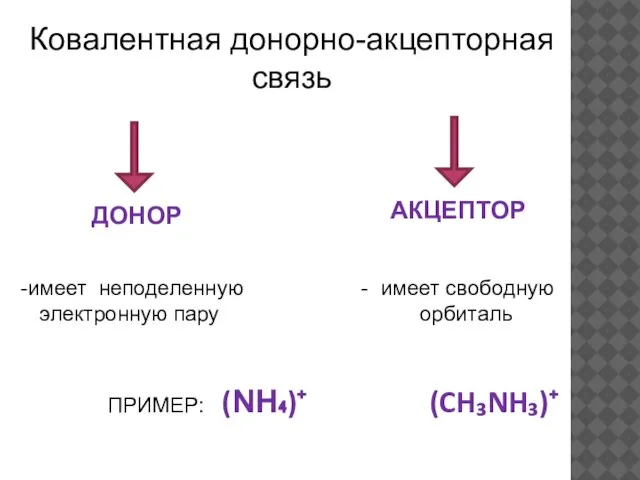
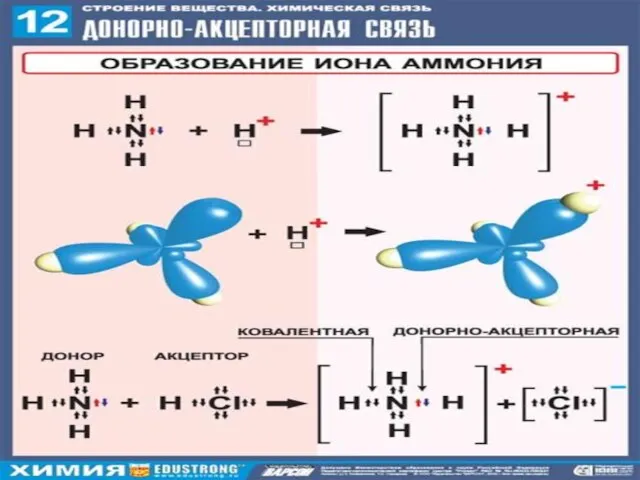
- 14. Ковалентная донорно-акцепторная связь ДОНОР АКЦЕПТОР имеет неподеленную - имеет свободную электронную пару орбиталь ПРИМЕР: (NH₄)⁺ (CH₃NH₃)⁺
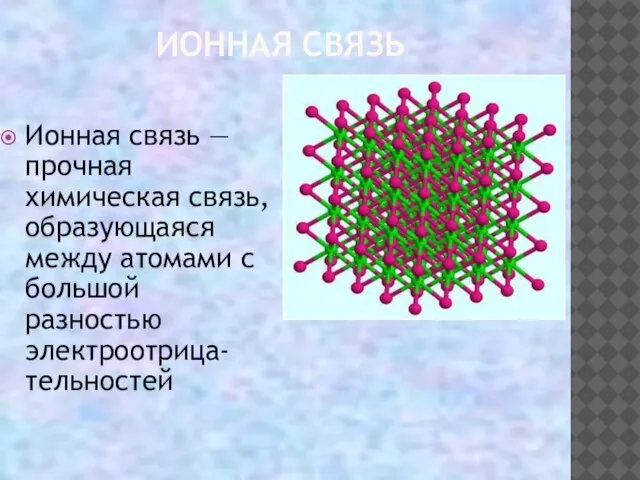
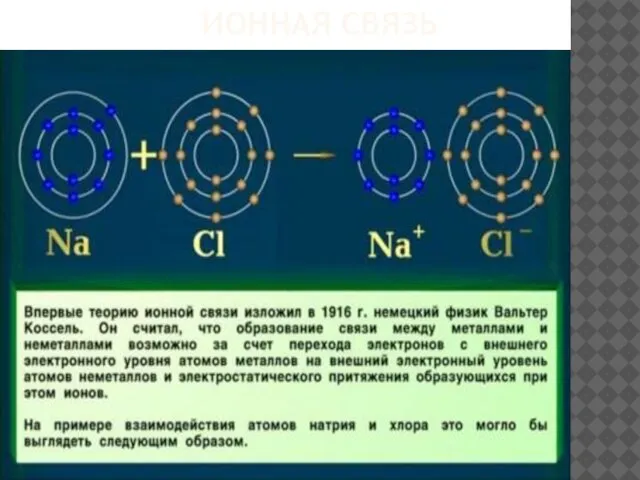
- 16. ИОННАЯ СВЯЗЬ Ионная связь — прочная химическая связь, образующаяся между атомами с большой разностью электроотрица-тельностей
- 17. ИОННАЯ СВЯЗЬ
- 18. СТЕПЕНЬ ОКИСЛЕНИЯ Сте́пень окисле́ния ( формальный заряд) — условная численная величина электрического заряда, приписываемого атому в
- 19. СТЕПЕНЬ ОКИСЛЕНИЯ Алгоритм определения степени окисления: Найдите элемент(-ты) с постоянной степенью окисления ( постоянная валентность; таблицы
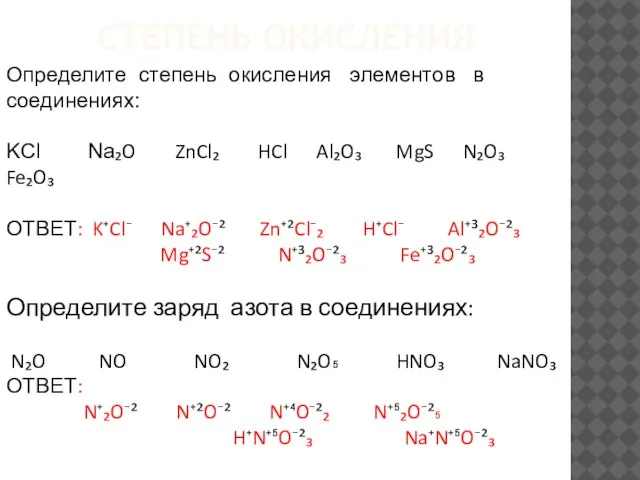
- 20. СТЕПЕНЬ ОКИСЛЕНИЯ Определите степень окисления элементов в соединениях: KCl Na₂O ZnCl₂ HCl Al₂O₃ MgS N₂O₃ Fe₂O₃
- 21. Определите степень окисления марганца в соединениях: MnO Mn₂O₅ MnCl₂ HMnO₄ K₂MnO₄ MnO₂ ОТВЕТ: Mn⁺²O⁻² Mn⁺⁵₂O⁻²₅ Mn⁺²Cl⁻₂
- 22. Определите вид химической связи в соединениях: Cl₂ , H₂O , CO , OF₂ , H₂ ,
- 24. Скачать презентацию







 Презентация на тему Окислительно-восстановительные реакции
Презентация на тему Окислительно-восстановительные реакции  Презентация на тему Сложные эфиры. Жиры
Презентация на тему Сложные эфиры. Жиры  Пентоза - відновлювальна сировина для синтезу фуранових сполук
Пентоза - відновлювальна сировина для синтезу фуранових сполук Дождь из облака
Дождь из облака По страницам истории российской химической науки
По страницам истории российской химической науки Явление хемилюменисценции
Явление хемилюменисценции Сложные вещества кислоты
Сложные вещества кислоты Что изучает химия?
Что изучает химия? Окислительно-восстановительные реакции. Классификация ОВР
Окислительно-восстановительные реакции. Классификация ОВР Термодинамика. Основные понятия и законы. Особенности термодинамики живых систем
Термодинамика. Основные понятия и законы. Особенности термодинамики живых систем Аналитический обзор по теме Процесс разложения аммиака
Аналитический обзор по теме Процесс разложения аммиака Презентация на тему Игра «Путешествие в страну Атомолия»
Презентация на тему Игра «Путешествие в страну Атомолия»  Белки
Белки Углеводороды. Общие знания
Углеводороды. Общие знания Ca КАЛЬЦИЙ
Ca КАЛЬЦИЙ Органическая химия. Йенс Якоб Берцелиус (1779 - 1848)
Органическая химия. Йенс Якоб Берцелиус (1779 - 1848) Презентация на тему Альдегиды (10 класс)
Презентация на тему Альдегиды (10 класс)  Щелочные металлы
Щелочные металлы Жесткость воды и способы ее устранения
Жесткость воды и способы ее устранения Презентация на тему Валентность и степень окисления (8 класс)
Презентация на тему Валентность и степень окисления (8 класс)  Основной государственный экзамен. Химия 2022. Задание 2
Основной государственный экзамен. Химия 2022. Задание 2 Своя игра. Атомы
Своя игра. Атомы ИКТ как средство реализации проблемного обучения на уроках химии
ИКТ как средство реализации проблемного обучения на уроках химии Алюминий. Применение
Алюминий. Применение Хлороводород и соляная кислота
Хлороводород и соляная кислота Химические свойства оксидов
Химические свойства оксидов Химическая связь. Строение вещества
Химическая связь. Строение вещества Презентация на тему Основания и их классификация
Презентация на тему Основания и их классификация