Слайд 2
Почему молекулярная формула воды Н2О ?

Слайд 3Валентность−это свойство атомов одного химического элемента соединяться со строго определенным числом атомов

другого химического элемента.
Слайд 4За единицу валентности принята валентность водорода−он одновалентен
Кислород двухвалетен
Схема образования молекулы воды
Н−

+ −О− + −Н → Н−О−Н
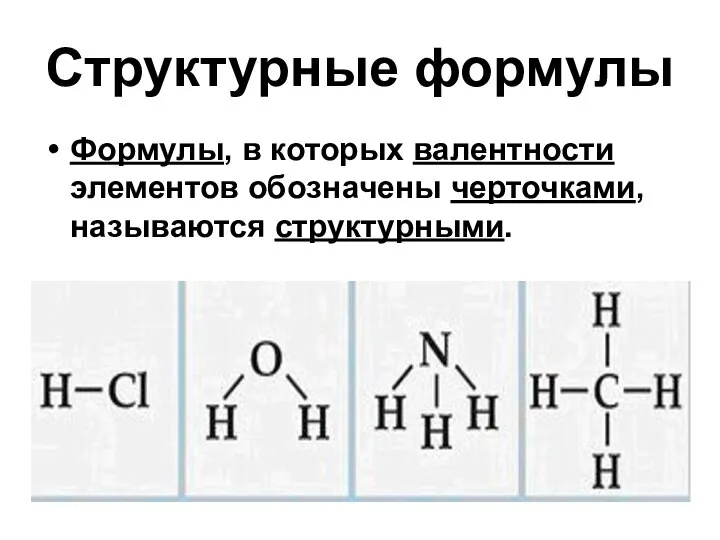
Слайд 5Структурные формулы
Формулы, в которых валентности элементов обозначены черточками, называются структурными.
Слайд 6Углекислый газ
О=С=О СО2
Кислород двухвалентен
Углерод четырехвалентен

Слайд 7Бинарные соединения
Вещества, молекулы которых состоят из 2-х элементов, называются бинарными

Слайд 8Составление формул по валентности

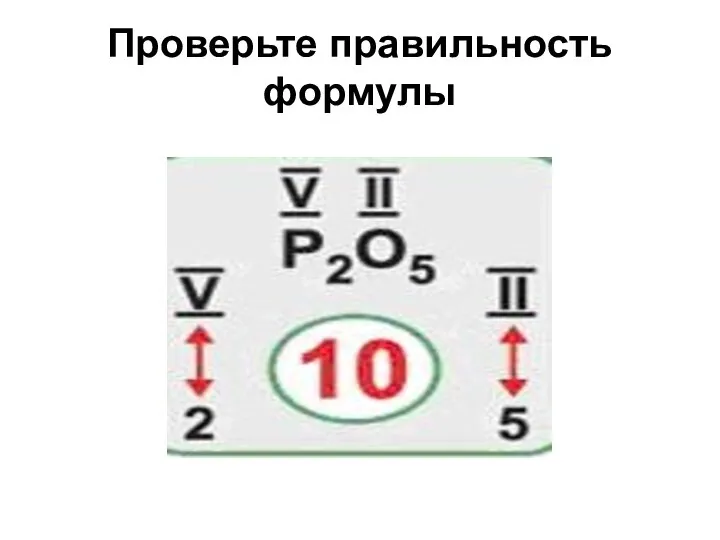
Слайд 9Проверьте правильность формулы
Слайд 10Определение валентности по положению элемента в ПС
Высшая валентность по кислороду = номеру

группы (А)
Низшая валентность по водороду = 8 − номер группы (А)
Слайд 11Названия веществ
Элемент + O(II) → оксиды
Элемент + S(II) → сульфиды
Элемент +

Cl(I) → хлориды
Слайд 12Постоянная валентность
Элементы I A ; II A; III A
Фтор одновалентен
Кислород двухвалентен

Слайд 13Переменная валентность
Элементы побочных подгрупп
Элемента IV (A); V (A); VI (A); VII (A)













 Свойства воды
Свойства воды Классы неорганических веществ. Типы химических реакций Конкурс знаний
Классы неорганических веществ. Типы химических реакций Конкурс знаний Экстракция
Экстракция Алкены (этиленовые углеводороды)
Алкены (этиленовые углеводороды) Растворы электролитов
Растворы электролитов Кислотність бджолиного обніжжя
Кислотність бджолиного обніжжя Предмет химии, простые и сложные вещества
Предмет химии, простые и сложные вещества (Bu4N)2[Mo6I8(OOCCH3)6]. Синтез
(Bu4N)2[Mo6I8(OOCCH3)6]. Синтез Химические процессы на кухне (урок №7)
Химические процессы на кухне (урок №7) Синтез ланшенгенина дэ
Синтез ланшенгенина дэ Примеры реакций в жизни и в быту. Реакции по направлению процесса
Примеры реакций в жизни и в быту. Реакции по направлению процесса Инновационное производство синтетических мелкокодисперсных оксидов и оборудования для их изготовления
Инновационное производство синтетических мелкокодисперсных оксидов и оборудования для их изготовления Основные положения теории электролитической диссоциации
Основные положения теории электролитической диссоциации Изомерия
Изомерия Презентация на тему Обобщение: предельные и непредельные углеводороды
Презентация на тему Обобщение: предельные и непредельные углеводороды  Презентация на тему Железо и его соединения (9 класс)
Презентация на тему Железо и его соединения (9 класс)  Водород. Свойства, применение
Водород. Свойства, применение Неорганосфера. Неметаллы
Неорганосфера. Неметаллы Признаки химических реакций
Признаки химических реакций Проблемное обучение на уроках химии
Проблемное обучение на уроках химии Окислительно-восстановительные реакции. Типы химических реакций
Окислительно-восстановительные реакции. Типы химических реакций Алкины. Химические свойства
Алкины. Химические свойства Вода и ее свойства
Вода и ее свойства proekt_TTU_3_1
proekt_TTU_3_1 Термопласты: основные представители, сравнение свойств и область их применения
Термопласты: основные представители, сравнение свойств и область их применения Презентация на тему Натуральные волокна
Презентация на тему Натуральные волокна  Полимеры. Виды полимеров
Полимеры. Виды полимеров Карбоновые кислоты
Карбоновые кислоты