закрепить умения составлять структурные формулы веществ.
изучить химические свойства амфотерных гидроксидов
Развивающие:
развить умение устанавливать причинно-следственные связи,
умение прогнозировать свойства веществ, исходя из их строения
способствовать развитию грамотного химического языка;
развивать умение анализировать, исследовать, формировать аналитическое мышление.
Воспитательные:
повышение предметной мотивации (через использование ИТК средств обучения),
воздействуя на эмоциональную сферу школьника формировать такие чувства, как уверенность в своих силах, удовлетворение от умственной деятельности .
*



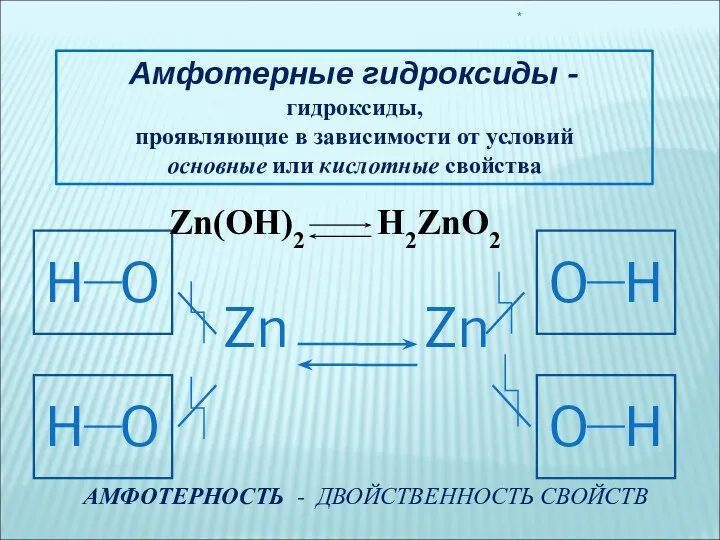
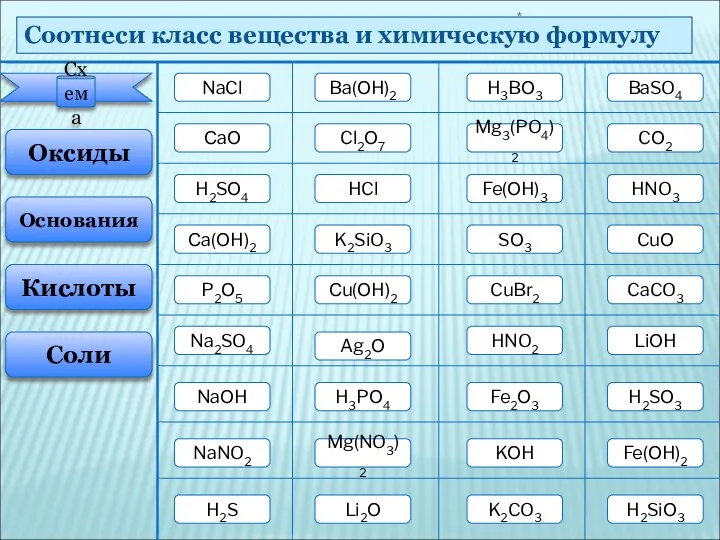




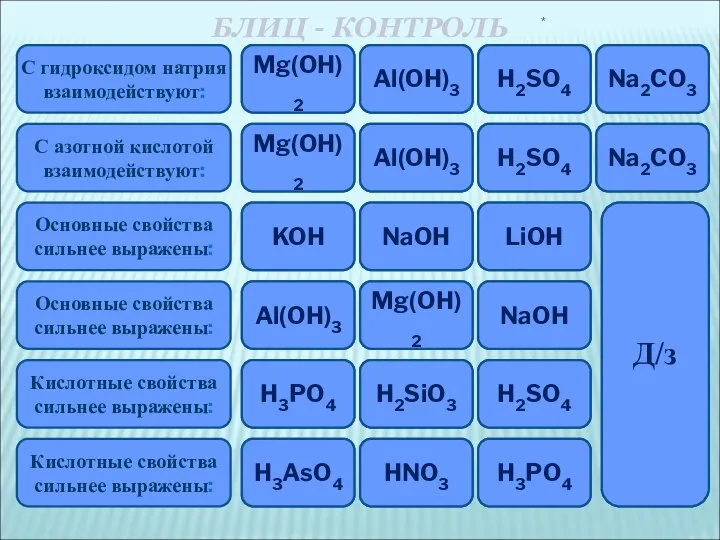
 Пусть имя Д.И. Менделеева будет нашей путеводной звездой
Пусть имя Д.И. Менделеева будет нашей путеводной звездой Химия. Какой химический элемент преобладает в составе каменного угля? Тест
Химия. Какой химический элемент преобладает в составе каменного угля? Тест Бер нигезле чикле карбон кислоталары
Бер нигезле чикле карбон кислоталары Ароматические углеводороды
Ароматические углеводороды Презентация на тему Подготовка к ГИА по химии
Презентация на тему Подготовка к ГИА по химии  Презентация на тему Важнейшие классы неорганических соединений
Презентация на тему Важнейшие классы неорганических соединений  Соли. Состав солей
Соли. Состав солей Альдегиды
Альдегиды Калифорний Cf
Калифорний Cf Химические формулы
Химические формулы Предмет органической химии. Теория химического строения органических веществ. 9 класс
Предмет органической химии. Теория химического строения органических веществ. 9 класс Эмпирические правила
Эмпирические правила Алюміній. Фізичні та хімічні властивості
Алюміній. Фізичні та хімічні властивості Изомерия. Упрощенная классификация органических соединений
Изомерия. Упрощенная классификация органических соединений Реакторы периодического действия. (Лекция 4)
Реакторы периодического действия. (Лекция 4) Типы кристаллических решеток. Тест
Типы кристаллических решеток. Тест Закономерности изменения окислительно-востановительных свойств соединений в периодах и группах
Закономерности изменения окислительно-востановительных свойств соединений в периодах и группах Основные понятия химии
Основные понятия химии Степени окисления и формулы веществ
Степени окисления и формулы веществ 1.2. Измерения веществ
1.2. Измерения веществ Свойства воды
Свойства воды Методы изготовления из резины и латекса
Методы изготовления из резины и латекса Исследование растворимости в системе уксусная кислота-этиловый спирт-этилацетат-вода методом изотермического титрования при 60˚C
Исследование растворимости в системе уксусная кислота-этиловый спирт-этилацетат-вода методом изотермического титрования при 60˚C Алканы – строение, химические свойства
Алканы – строение, химические свойства Типы химических реакций
Типы химических реакций Химическая связь в комплексных соединениях
Химическая связь в комплексных соединениях Стереоизомерия
Стереоизомерия Общая характеристика элементов главной подгруппы VI группы (подгруппы кислорода)
Общая характеристика элементов главной подгруппы VI группы (подгруппы кислорода)