Содержание
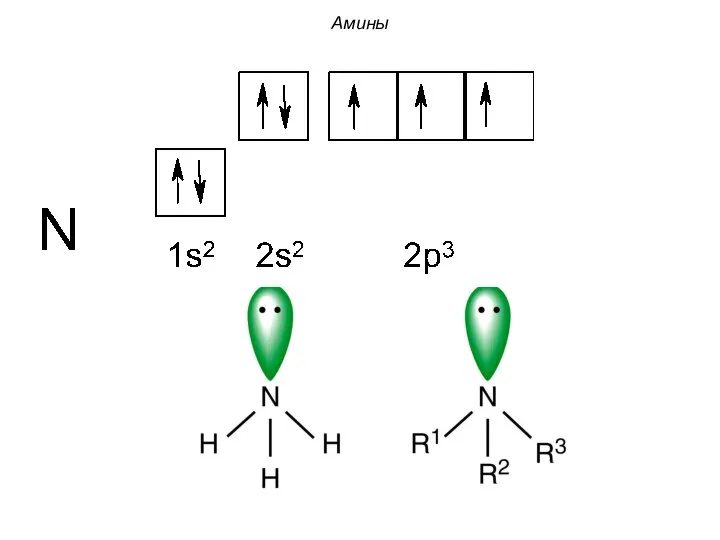
- 2. Амины
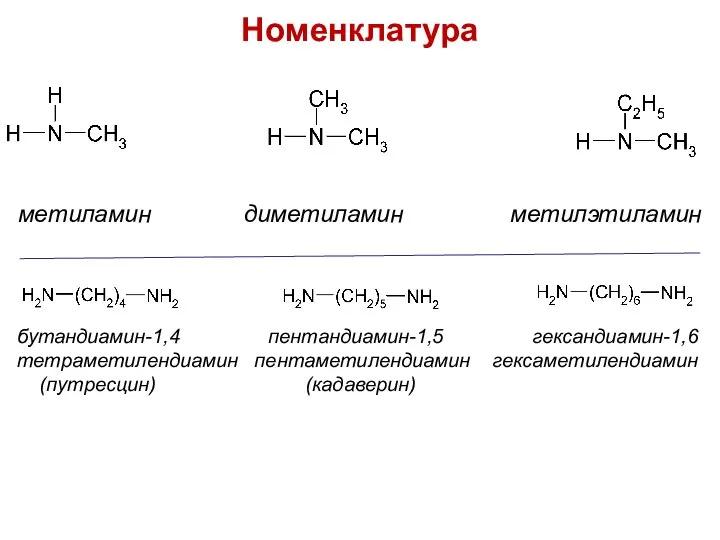
- 3. Номенклатура метиламин диметиламин метилэтиламин бутандиамин-1,4 пентандиамин-1,5 гександиамин-1,6 тетраметилендиамин пентаметилендиамин гексаметилендиамин (путресцин) (кадаверин)
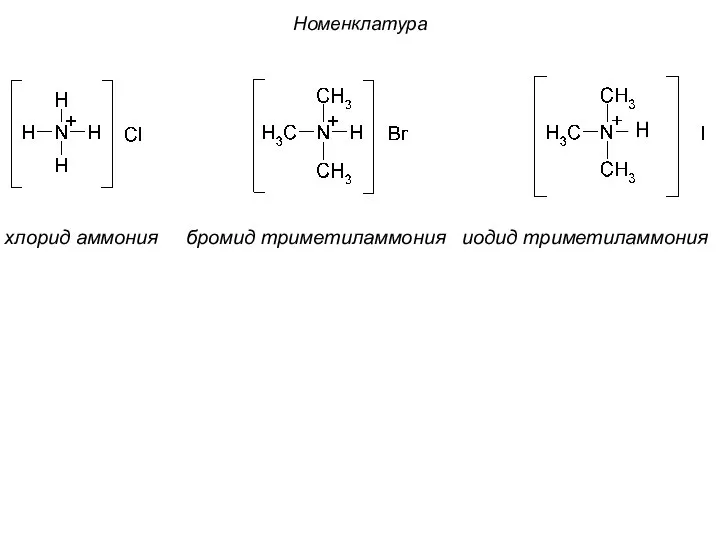
- 5. хлорид аммония бромид триметиламмония иодид триметиламмония Номенклатура H
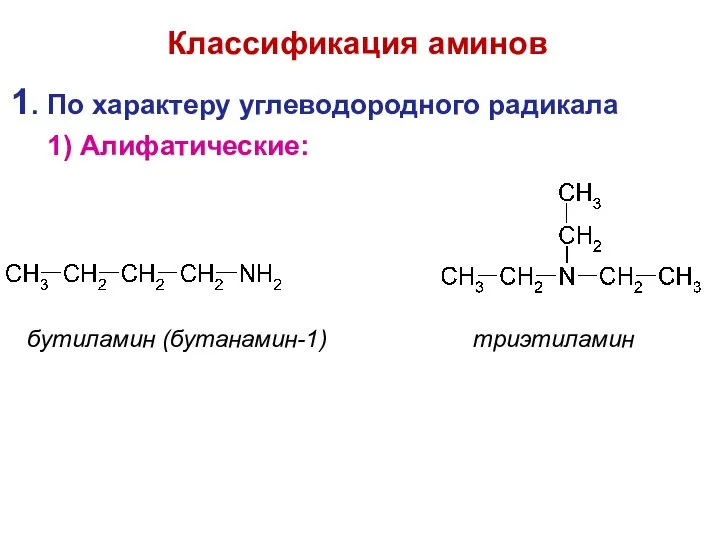
- 6. 1. По характеру углеводородного радикала 1) Алифатические: бутиламин (бутанамин-1) триэтиламин Классификация аминов
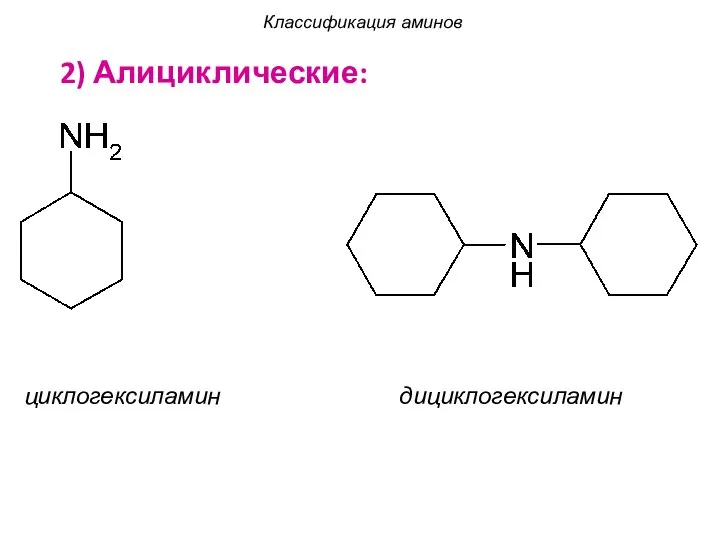
- 7. 2) Алициклические: циклогексиламин дициклогексиламин Классификация аминов
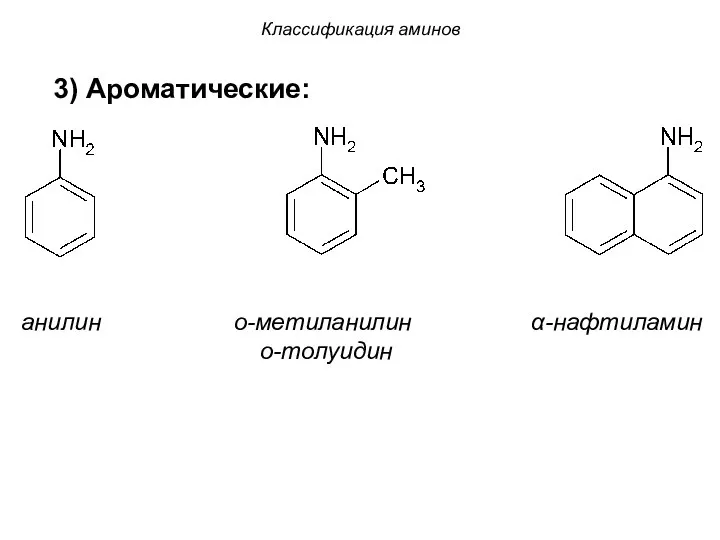
- 8. 3) Ароматические: анилин о-метиланилин α-нафтиламин о-толуидин Классификация аминов
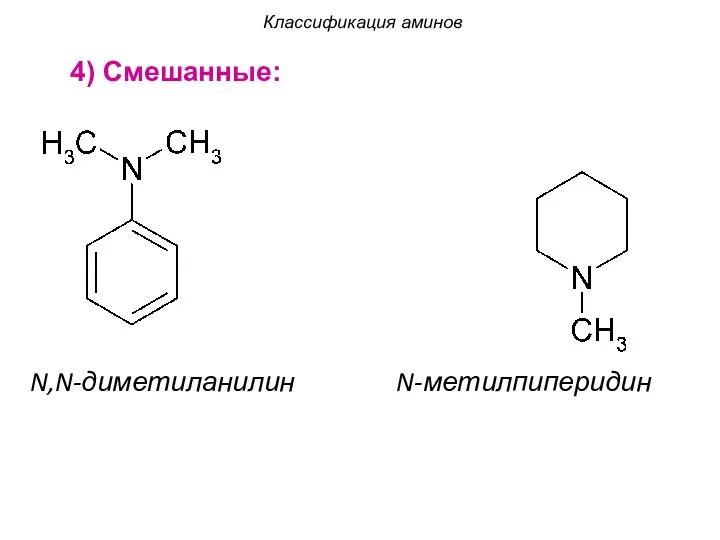
- 9. 4) Смешанные: N,N-диметиланилин N-метилпиперидин Классификация аминов
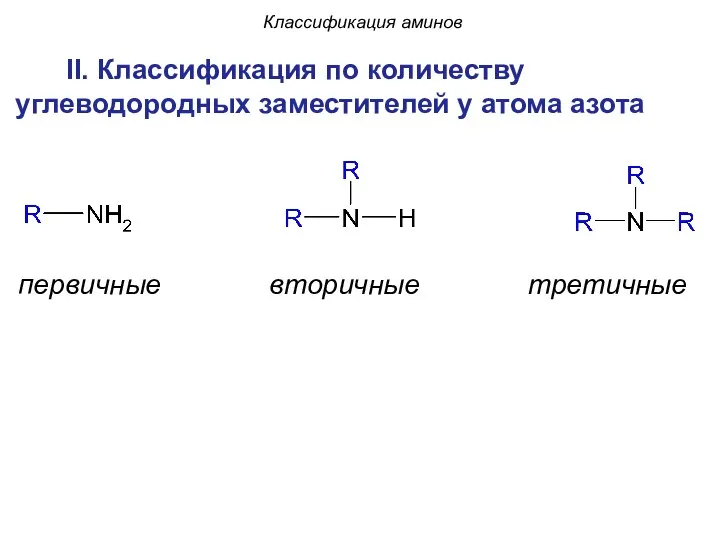
- 10. II. Классификация по количеству углеводородных заместителей у атома азота первичные вторичные третичные Классификация аминов
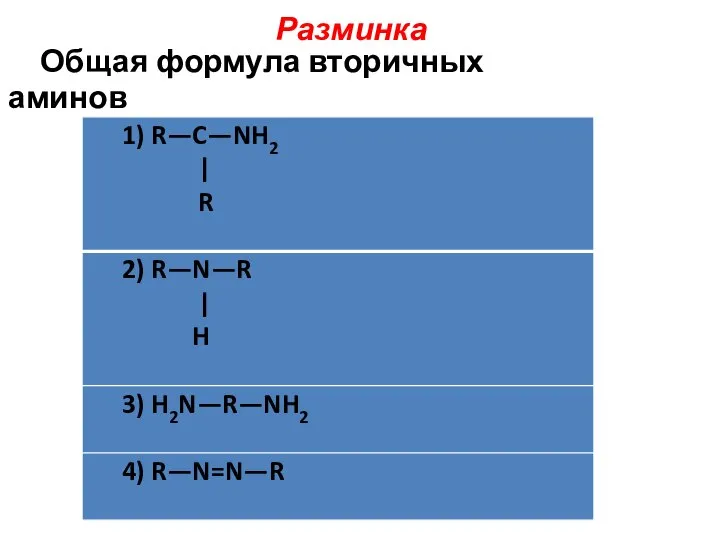
- 11. Разминка Общая формула вторичных аминов
- 12. I. Изомерия углеродного скелета II. Изомерия положения аминогруппы пентанамин-1 пентанамин-2 пентанамин-3 пентанамин -1 3-метилбутанамин-1 2-метилбутанмин-1 Структурная
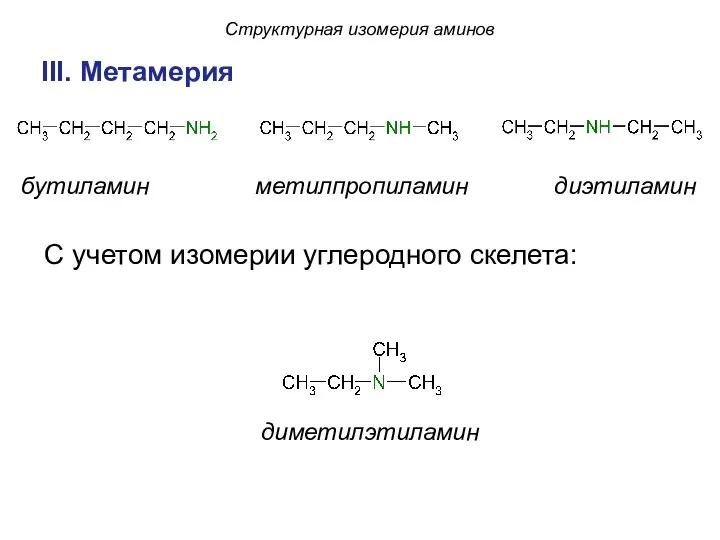
- 13. III. Метамерия бутиламин метилпропиламин диэтиламин диметилэтиламин С учетом изомерии углеродного скелета: Структурная изомерия аминов
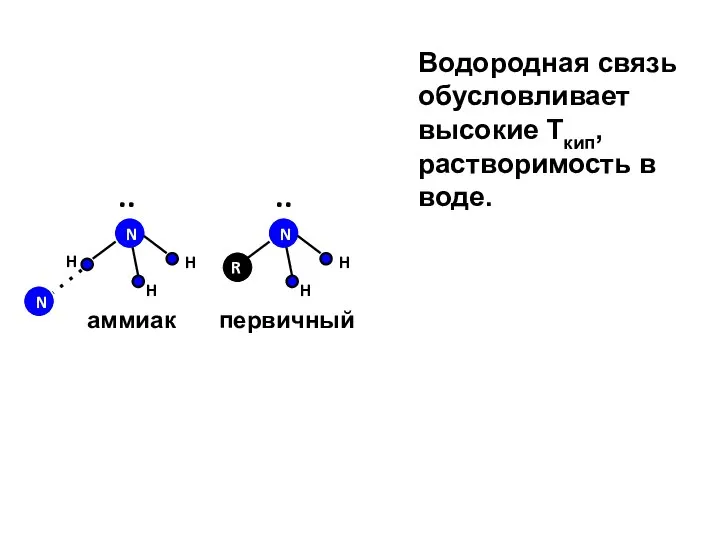
- 15. H H N .. H N R H H .. аммиак первичный N Водородная связь обусловливает
- 16. Анилин – простейший ароматический амин – бесцветная маслянистая жидкость, с характерным запахом, немного тяжелее воды и
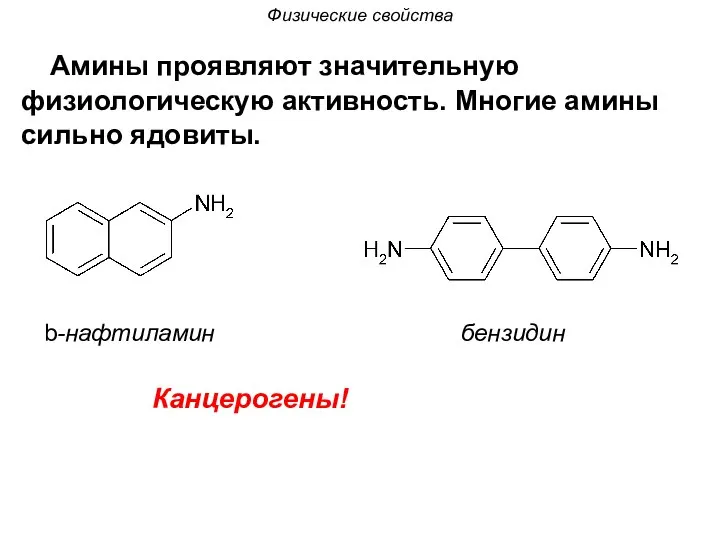
- 17. Амины проявляют значительную физиологическую активность. Многие амины сильно ядовиты. b-нафтиламин бензидин Канцерогены! Физические свойства
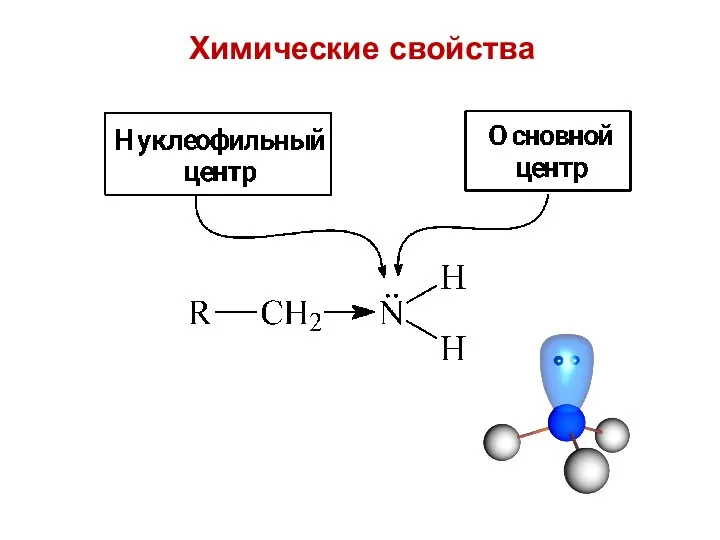
- 18. Химические свойства
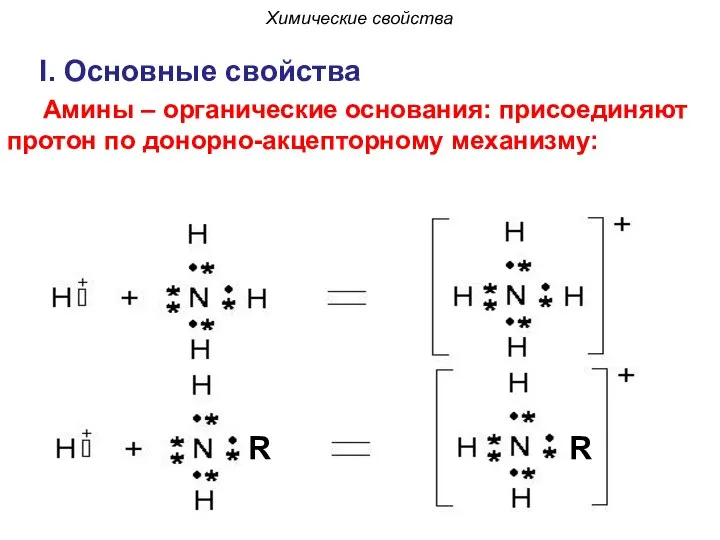
- 19. I. Основные свойства Амины – органические основания: присоединяют протон по донорно-акцепторному механизму: R R Химические свойства
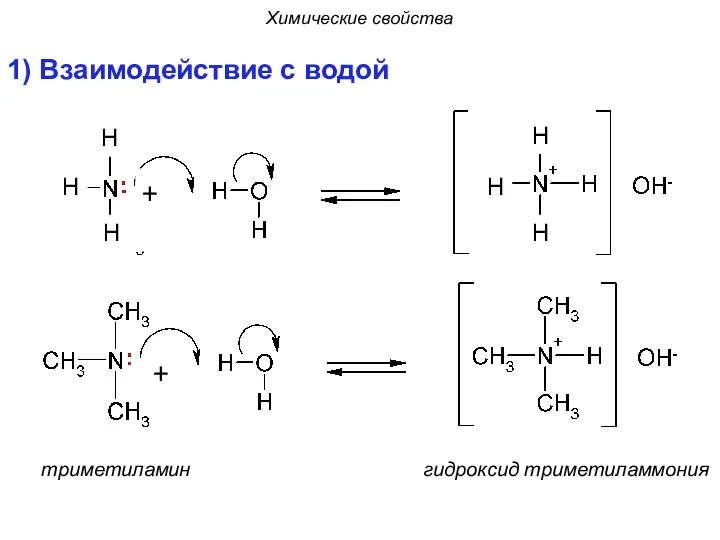
- 20. 1) Взаимодействие с водой триметиламин гидроксид триметиламмония Химические свойства H H H H H H H
- 21. Окраска индикаторов Химические свойства Амины окрашивают кислотно-основные индикаторы. В щелочной среде лакмус синий, метиловый оранжевый –
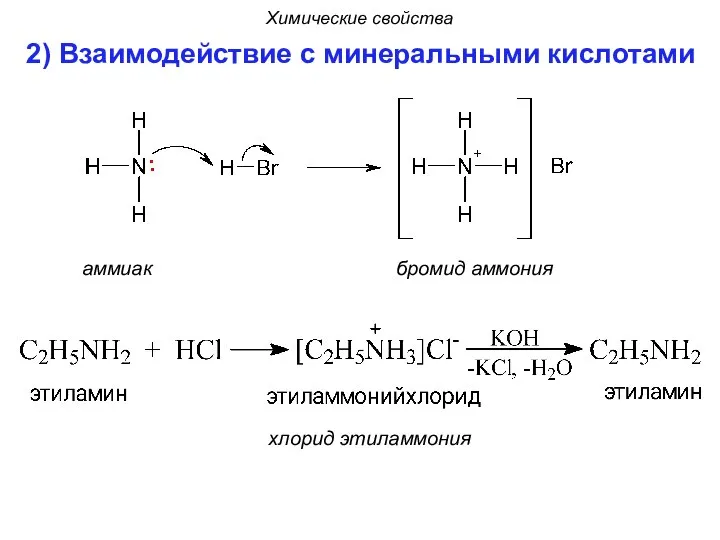
- 22. 2) Взаимодействие с минеральными кислотами Химические свойства аммиак бромид аммония хлорид этиламмония
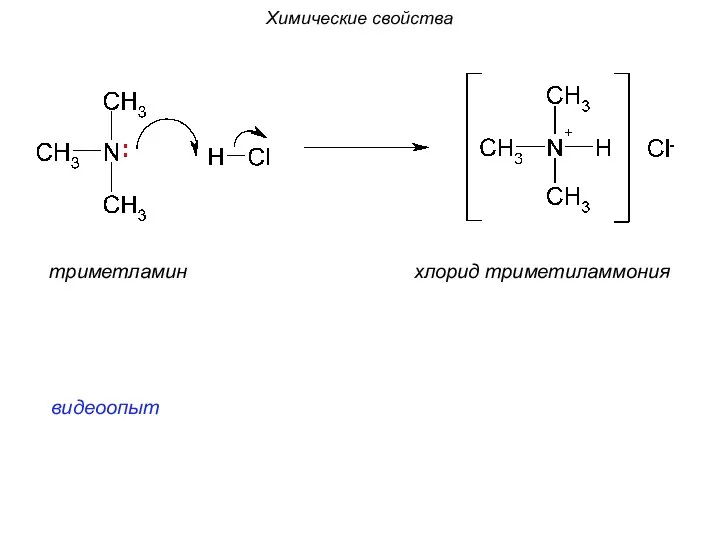
- 23. Химические свойства триметламин хлорид триметиламмония видеоопыт
- 24. Задание1. Напишите реакции образования сернокислых солей с метиламином и диэтиламином. Химические свойства Задание2. Напишите реакции взаимодействия
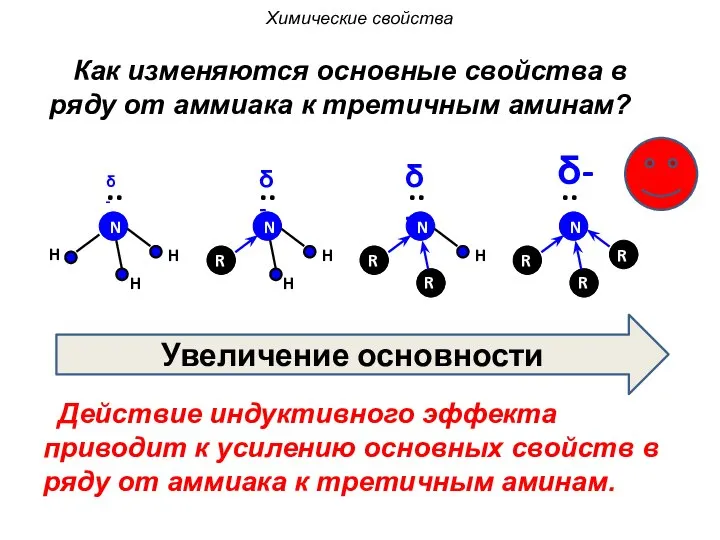
- 26. H H H N .. H N R H N H N R R R R
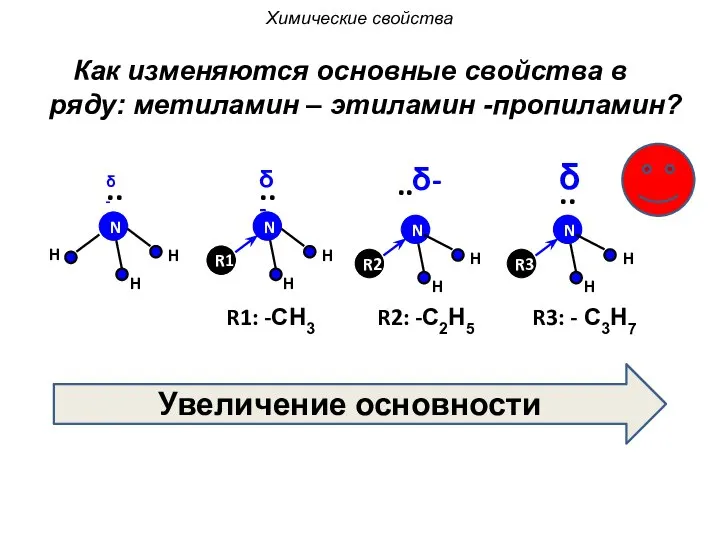
- 27. H H H N .. H N R1 H .. Как изменяются основные свойства в ряду:
- 28. Как изменяются основные свойства в ряду: аммиак – метиламин – диметиламин – триметиламин Тесты
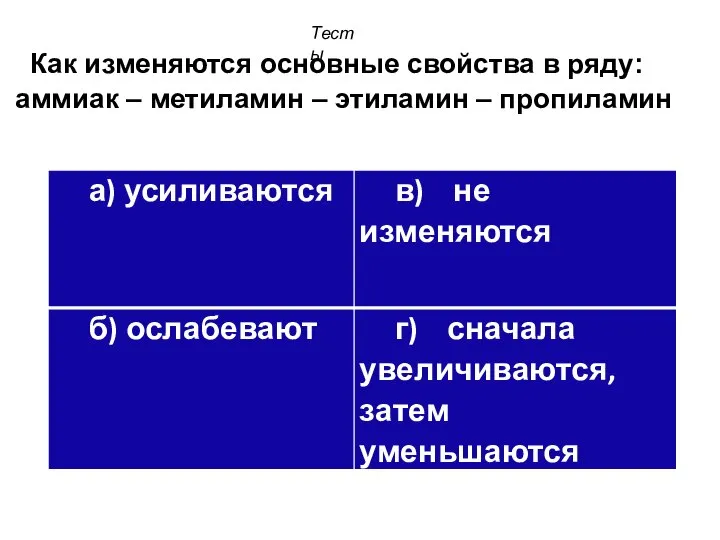
- 29. Как изменяются основные свойства в ряду: аммиак – метиламин – этиламин – пропиламин Тесты
- 30. Химические свойства II. Взаимодействие первичных аминов с азотистой кислотой СH3NH2 + HNO2 → CH3OH + N2
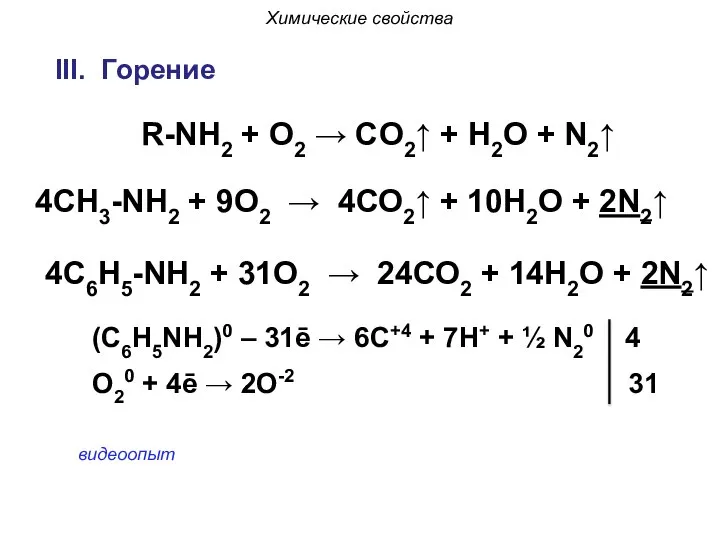
- 32. Химические свойства III. Горение R-NH2 + O2 → CO2↑ + H2O + N2↑ 4СН3-NH2 + 9О2
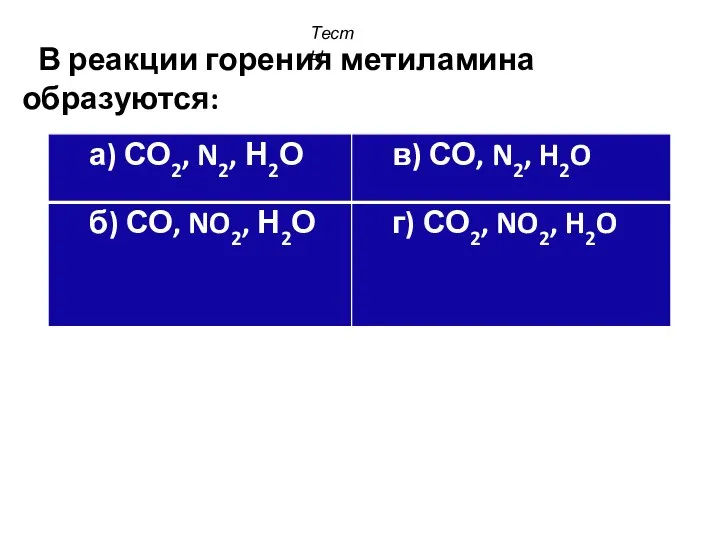
- 33. В реакции горения метиламина образуются: Тесты
- 34. Этиламин не взаимодействует с веществом, формула которого: Тесты
- 35. Окраска водного раствора амина в присутствии фенолфталеина: Тесты
- 36. Метиламин: Тесты Ответ .
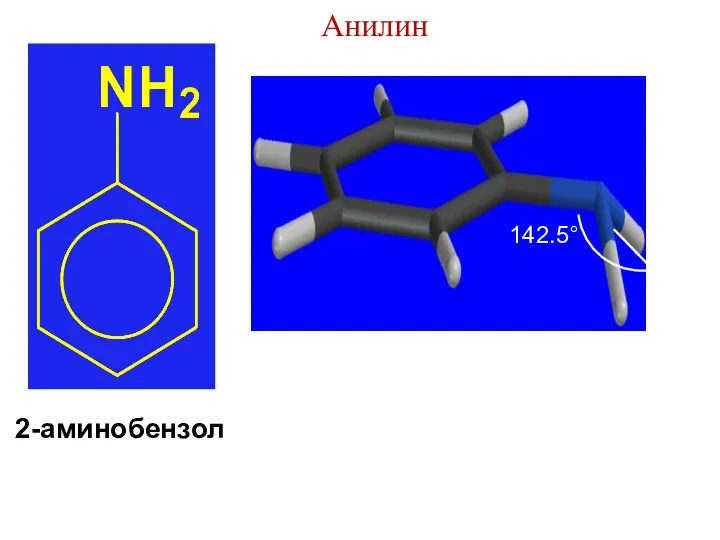
- 37. 142.5° Анилин 2-аминобензол
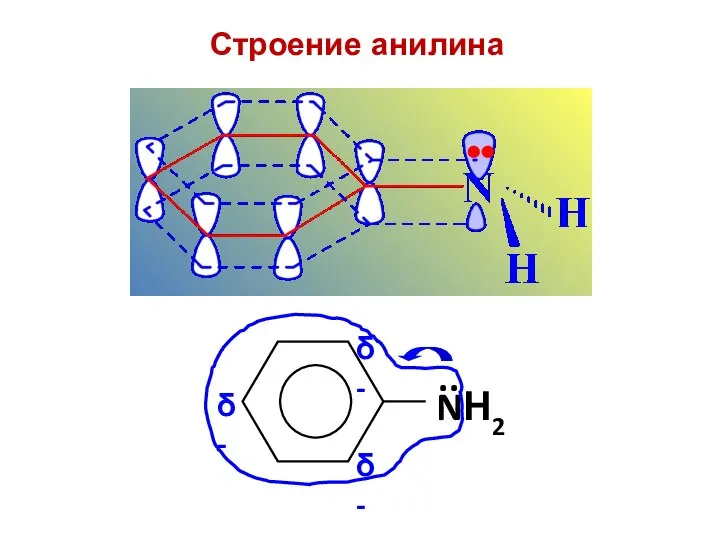
- 38. Строение анилина
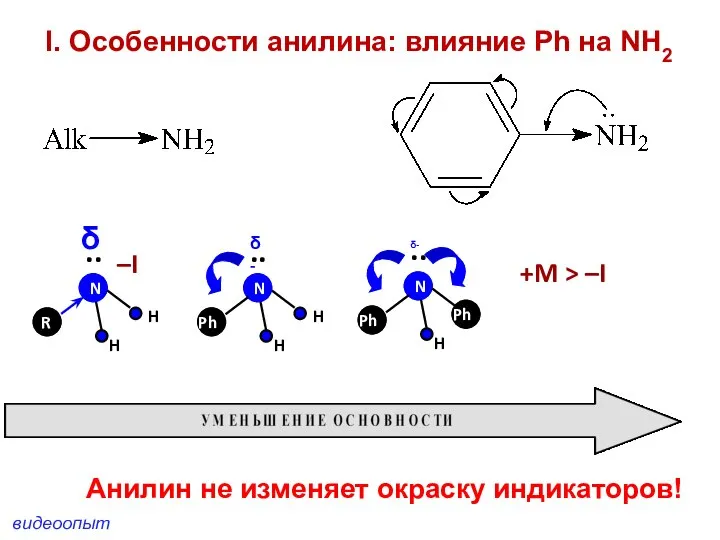
- 39. –I +M > –I I. Особенности анилина: влияние Ph на NH2 H H H Ph N
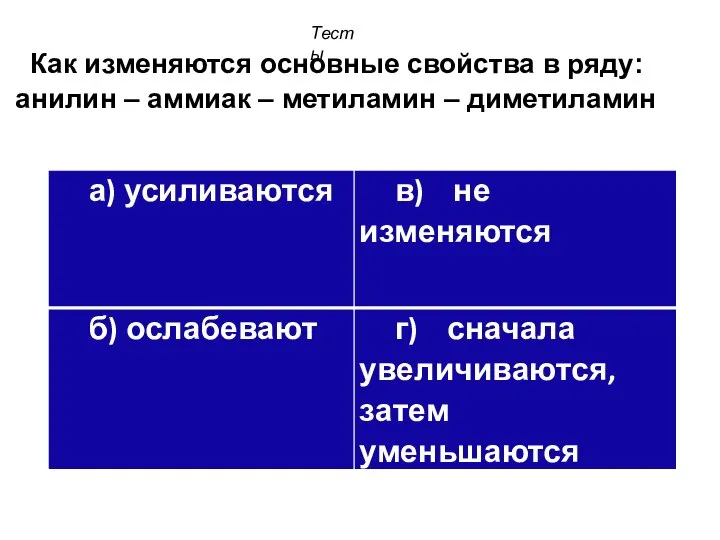
- 40. Как изменяются основные свойства в ряду: анилин – аммиак – метиламин – диметиламин Тесты
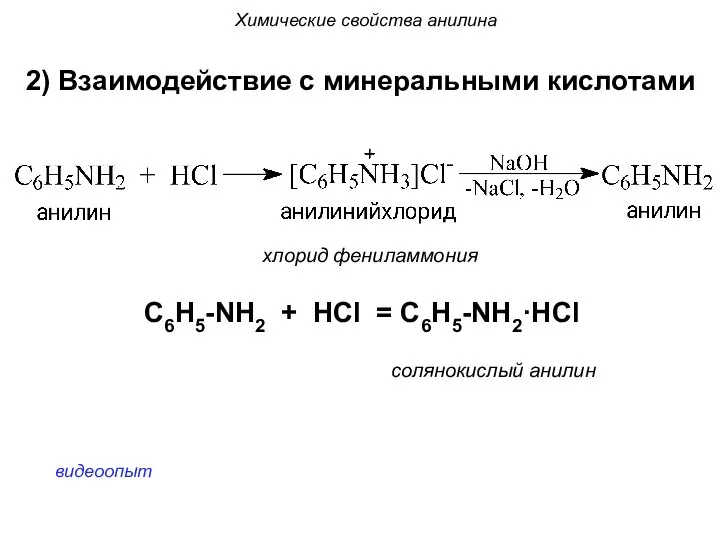
- 41. Химические свойства анилина 2) Взаимодействие с минеральными кислотами хлорид фениламмония С6Н5-NH2 + HCl = С6Н5-NH2·HCl солянокислый
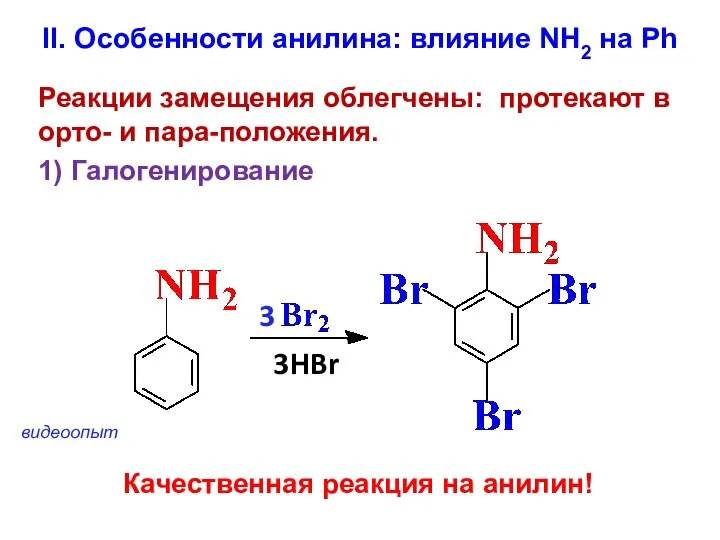
- 42. II. Особенности анилина: влияние NH2 на Ph Реакции замещения облегчены: протекают в орто- и пара-положения. 1)
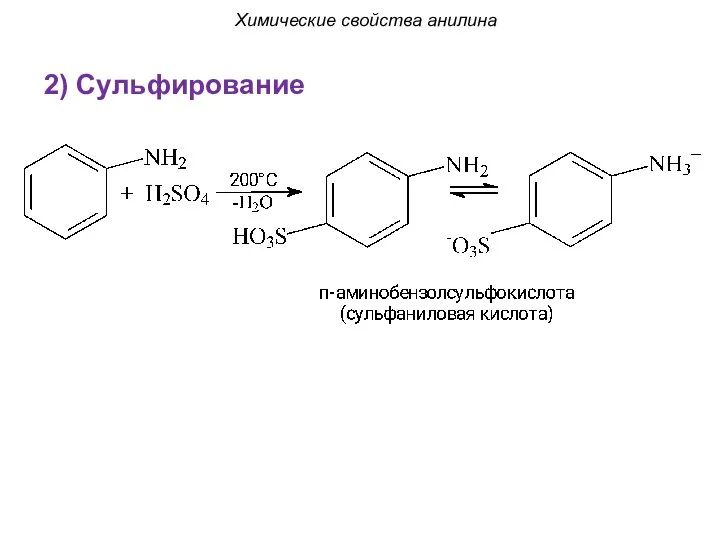
- 43. 2) Сульфирование Химические свойства анилина
- 45. Получение 1. Реакция Гофмана (1850) Гофман Фридрих
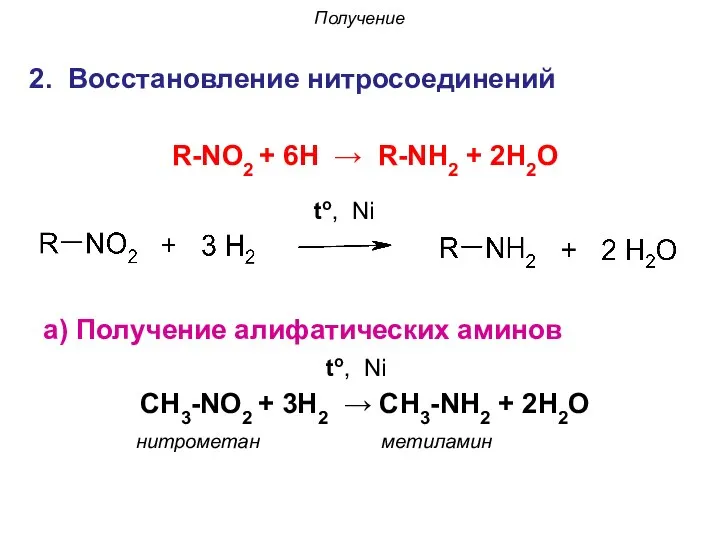
- 46. 2. Восстановление нитросоединений Получение to, Ni R-NO2 + 6H → R-NH2 + 2H2О а) Получение алифатических
- 47. ЗИНИН Николай Николаевич (25.VIII.1812–18.II.1880) Академик, возглавлял кафедру общей химии Медико-хирургической академии в Петербурге, организатор и первый
- 48. C6H5-NO2 +3 Fe+7HCl=C6H5-NH3Cl+3FeCl2+2H20 3Fe+6HCL=3FeCl2+3H2 Получение
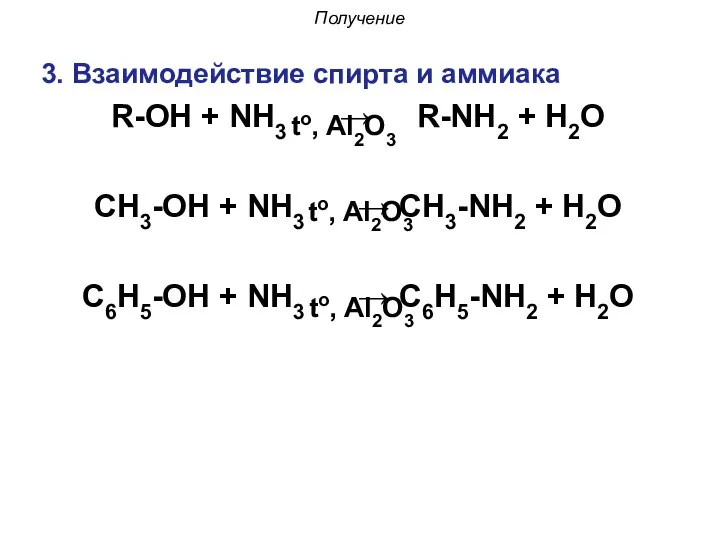
- 49. 3. Взаимодействие спирта и аммиака R-OH + NH3 → R-NH2 + H2O СH3-OH + NH3 →
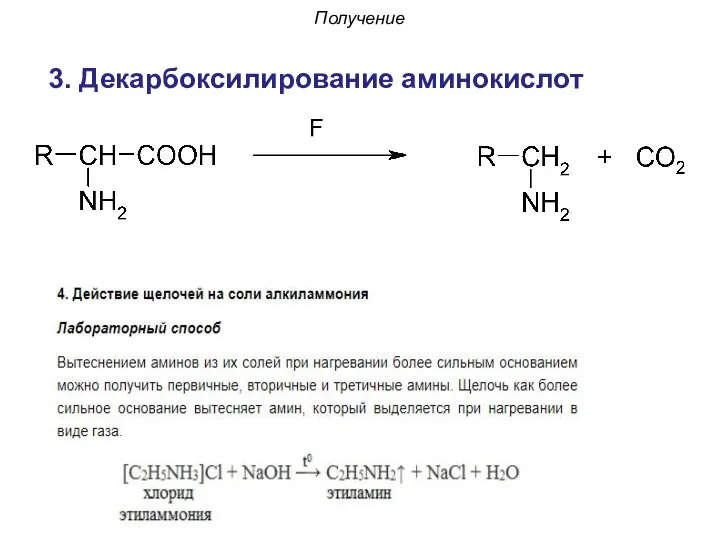
- 50. 3. Декарбоксилирование аминокислот Получение F
- 52. Анилин: Тесты Ответ .
- 53. Метиламин, в отличие от анилина: Тесты Ответ .
- 54. Анилин, в отличие от этиламина: Тесты Ответ .
- 61. Скачать презентацию























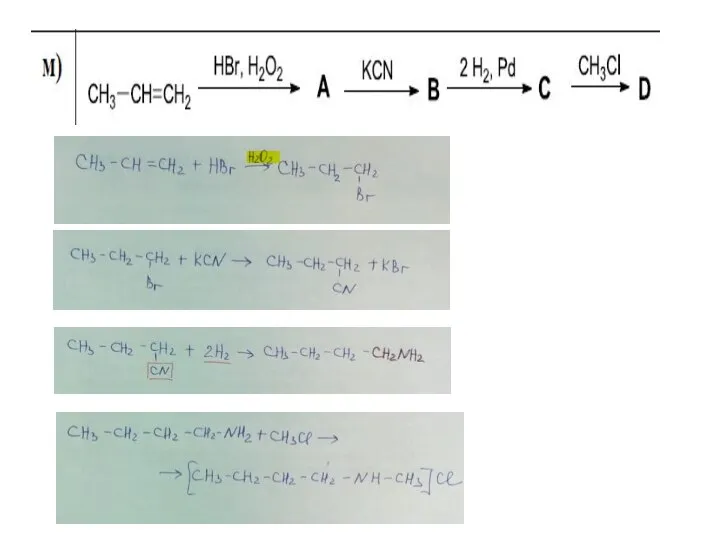
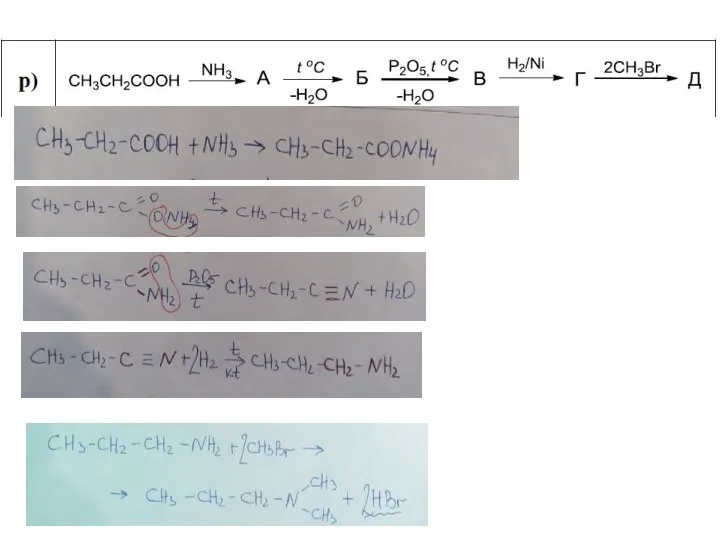

 Деятельностный подход в изучении химии
Деятельностный подход в изучении химии Презентация на тему Задачи на смеси и сплавы (9 класс)
Презентация на тему Задачи на смеси и сплавы (9 класс)  Закон сохранения массы и химические уравнения
Закон сохранения массы и химические уравнения Амины. Аминокислоты. Белки
Амины. Аминокислоты. Белки Облик и габитус кристаллов
Облик и габитус кристаллов Уравнение состояния идеального газа. Газовые законы. Изопроцессы
Уравнение состояния идеального газа. Газовые законы. Изопроцессы Вывод химических формул
Вывод химических формул Путешествие в мир кислот
Путешествие в мир кислот Хімія в стоматології
Хімія в стоматології Реактор гидроочистки дизельного топлива. Контроль и автоматизация
Реактор гидроочистки дизельного топлива. Контроль и автоматизация Разработка электронных образовательных ресурсов в естественнонаучном образовании бакалавров направления Химия
Разработка электронных образовательных ресурсов в естественнонаучном образовании бакалавров направления Химия Химическая кинетика и равновесие
Химическая кинетика и равновесие Зависимость знака заряда белка от pH
Зависимость знака заряда белка от pH Электрохимия
Электрохимия Аппаратурное оформление процесса гидроочистки нефтяных фракций
Аппаратурное оформление процесса гидроочистки нефтяных фракций Переваривание и всасывание липидов. Транспортные формы липидов в крови. Лекция № 7
Переваривание и всасывание липидов. Транспортные формы липидов в крови. Лекция № 7 Сокровища соляных дворцов
Сокровища соляных дворцов Материалы к уроку «Значение растворов» Автор: учитель СОШ № 4 Чурбакова Елена Васильевна
Материалы к уроку «Значение растворов» Автор: учитель СОШ № 4 Чурбакова Елена Васильевна Свойства кальция и магния. Жёсткость воды. Лекция №7
Свойства кальция и магния. Жёсткость воды. Лекция №7 Плазменное состояние вещества
Плазменное состояние вещества Спирты. К кроссворду
Спирты. К кроссворду Презентация на тему Алкины
Презентация на тему Алкины  Полімери. Пінополістирол
Полімери. Пінополістирол Химическая промышленность
Химическая промышленность Химия элементов IVA группы
Химия элементов IVA группы Зонная структура металлов, диэлектриков и полупроводников
Зонная структура металлов, диэлектриков и полупроводников Сложные эфиры. Жиры
Сложные эфиры. Жиры Предмет органической химии
Предмет органической химии