Содержание
- 2. ЦЕЛЬ УРОКА: сформировать представление о законе постоянства состава веществ, рассмотреть понятие химические формулы. ЗАДАЧИ УРОКА: -
- 3. (справедлив только для веществ молекулярного строения) Жозеф Луи Пруст (1754-1826) Каждое химически чистое вещество независимо от
- 4. Вода может быть получена в результате следующих химических реакций: 2Н2 + O2 = 2Н2O Cu(OH) =
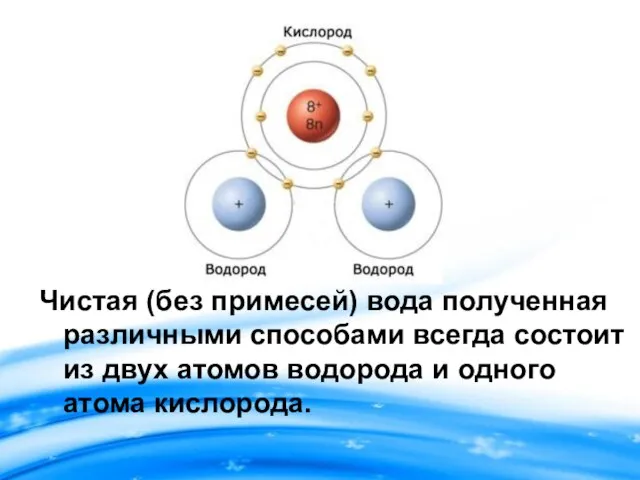
- 5. Чистая (без примесей) вода полученная различными способами всегда состоит из двух атомов водорода и одного атома
- 6. Из каких атомов состоит это вещество? FeS Найдите в ПСХЭ значение относительных атомных масс железа и
- 7. Ar (Fe) = 56 Ar (S) = 32 Соотношение масс: Ar (Fe) : Ar(S) = 56
- 8. Задание Сколько грамм железа нужно взять, чтобы прореагировало 2г серы?
- 9. Практикум Известно вещество, в котором на 2 атома меди приходится 1 атом серы. В каких массовых
- 10. Находим: 2 Ar(Cu)= 64 х 2 = 128 Ar(S) = 32 Медь и серу необходимо смешать
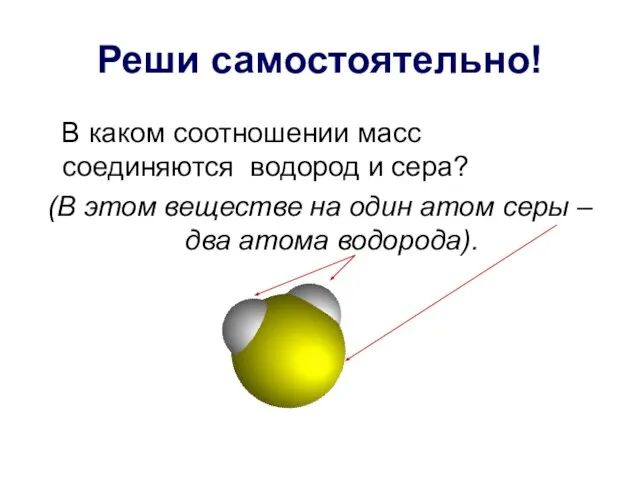
- 11. Реши самостоятельно! В каком соотношении масс соединяются водород и сера? (В этом веществе на один атом
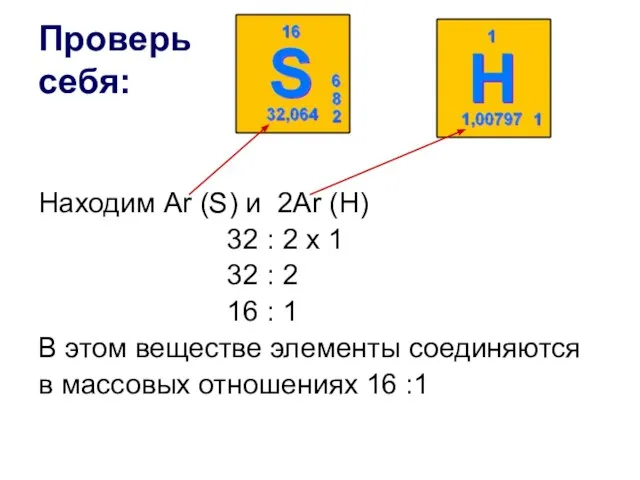
- 12. Проверь себя: Находим Ar (S) и 2Ar (H) 32 : 2 х 1 32 : 2
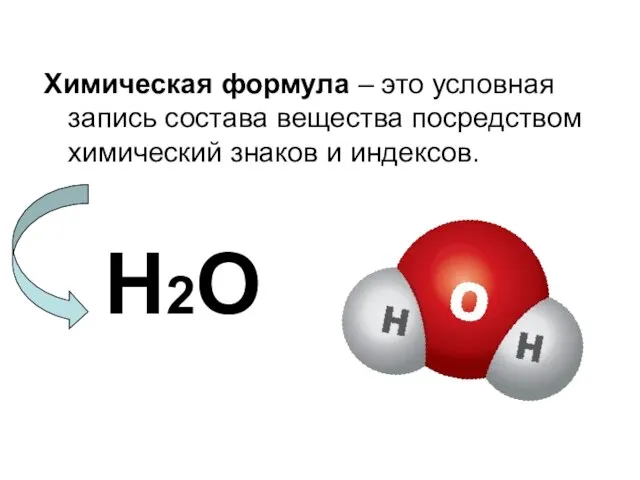
- 13. Химическая формула – это условная запись состава вещества посредством химический знаков и индексов. Н2О
- 14. ХИМИЧЕСКАЯ ФОРМУЛА ВОДЫ Н2О Индекс 2 (обозначает 2 атома водорода в составе молекулы воды). Индекс 1
- 15. ХИМИЧЕСКАЯ ФОРМУЛА ВОДЫ 2 Н2О Коэффициент 2 (показывает 2 молекулы воды). Коэффициент обозначает число молекул (или
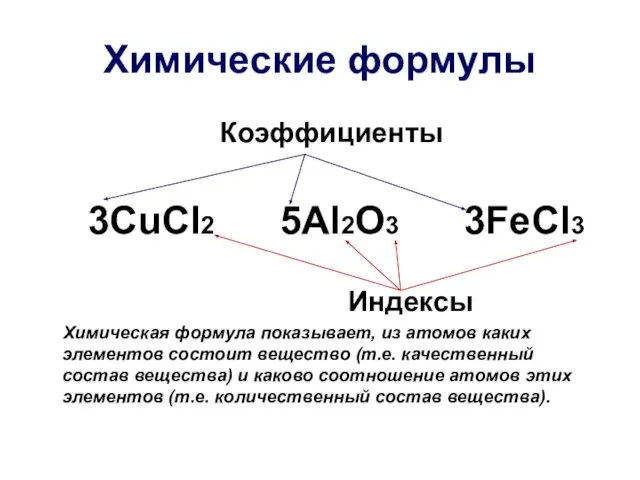
- 16. Химические формулы Коэффициенты 3CuCl2 5Al2O3 3FeCl3 Индексы Химическая формула показывает, из атомов каких элементов состоит вещество
- 17. Подумай, выполни, ответь… Что означают формулы? 3Н2О 5Fe Как читаются эти записи? Напишите следующую формулу: пять
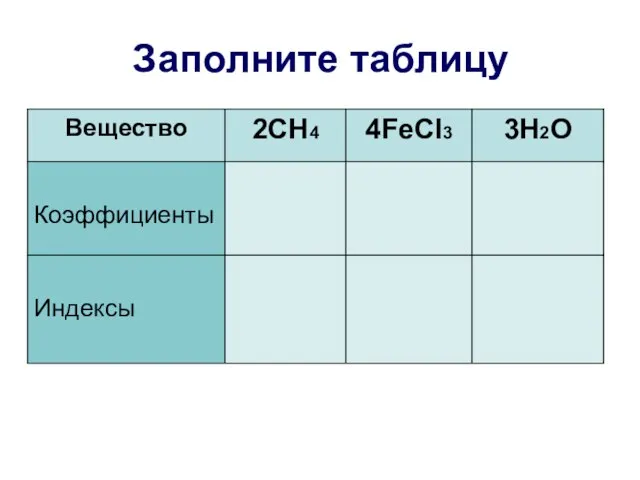
- 18. Заполните таблицу
- 19. РЕФЛЕКСИЯ
- 21. Скачать презентацию












 Стекло. История открытия. Самое древнее производство Эпохи фараонов
Стекло. История открытия. Самое древнее производство Эпохи фараонов Основи молекулярно-кінетичної теорії
Основи молекулярно-кінетичної теорії Кислородсодержащие органические соединения
Кислородсодержащие органические соединения Подготовка к ГИА по химии
Подготовка к ГИА по химии Презентация на тему Научная химическая лаборатория Ломоносова
Презентация на тему Научная химическая лаборатория Ломоносова  Гидроксиды металлов
Гидроксиды металлов Химические равновесия в растворах. Лекция 2 часть 2
Химические равновесия в растворах. Лекция 2 часть 2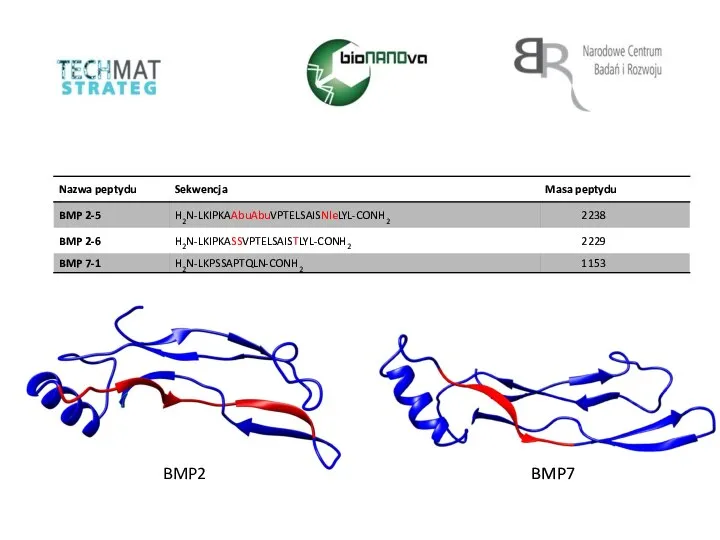 Nazwa peptydu. Sekwencja
Nazwa peptydu. Sekwencja Полімери. Пінополістирол
Полімери. Пінополістирол 5 группа элементов
5 группа элементов Химические свойства насыщенных альдегидов и кетонов (продолжение)
Химические свойства насыщенных альдегидов и кетонов (продолжение) Водородная химическая связь
Водородная химическая связь Коррозия. способы защиты от коррозии
Коррозия. способы защиты от коррозии Презентация на тему Спирты (9 класс)
Презентация на тему Спирты (9 класс)  Электролиз воды
Электролиз воды Генетические ряды углеводородов. Обобщение и систематизация знаний
Генетические ряды углеводородов. Обобщение и систематизация знаний Адсорбционные материалы. Цеолиты
Адсорбционные материалы. Цеолиты Химическая термодинамика
Химическая термодинамика Термодинамическое равновесие между фазами
Термодинамическое равновесие между фазами Физическая химия. Вводная лекция
Физическая химия. Вводная лекция Строение вещества. ОВР. Окислительно-восстановительные реакции
Строение вещества. ОВР. Окислительно-восстановительные реакции Материаловедение. Технология конструкционных материалов. Диаграмма состояния Fe-Fe3C
Материаловедение. Технология конструкционных материалов. Диаграмма состояния Fe-Fe3C Мыльная история
Мыльная история Оксиды. Классификация. Химические и физические свойства
Оксиды. Классификация. Химические и физические свойства алотропні модифікації неметалів
алотропні модифікації неметалів Презентация для заочников
Презентация для заочников Генетическая связь неорганических соединений
Генетическая связь неорганических соединений Алкины. Понятие об алкинах
Алкины. Понятие об алкинах