Содержание
- 2. Кристаллом (от греч. krystallos – «прозрачный лед») вначале называли прозрачный кварц (горный хрусталь), встречавшийся в Альпах.
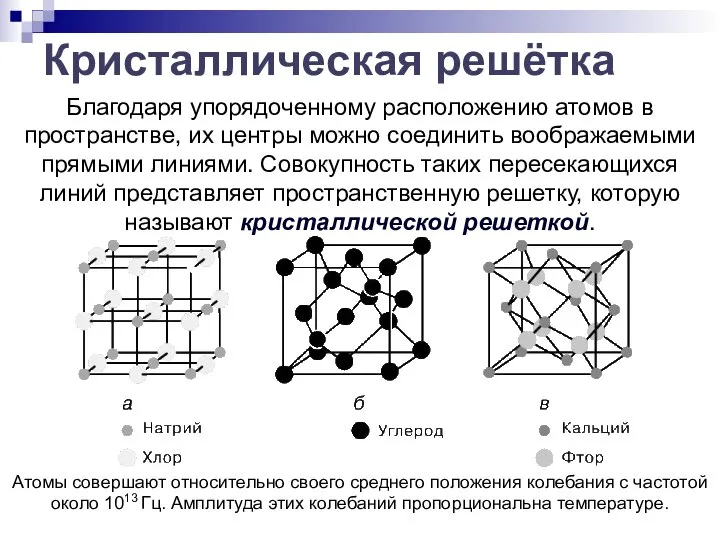
- 3. Благодаря упорядоченному расположению атомов в пространстве, их центры можно соединить воображаемыми прямыми линиями. Совокупность таких пересекающихся
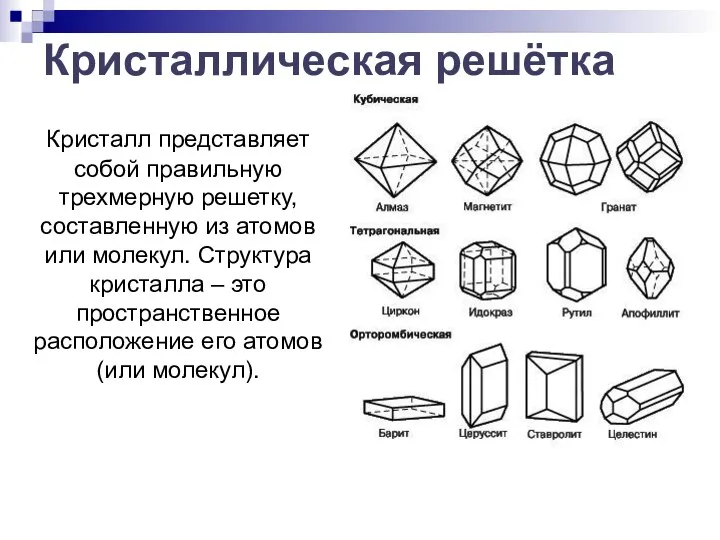
- 4. Кристалл представляет собой правильную трехмерную решетку, составленную из атомов или молекул. Структура кристалла – это пространственное
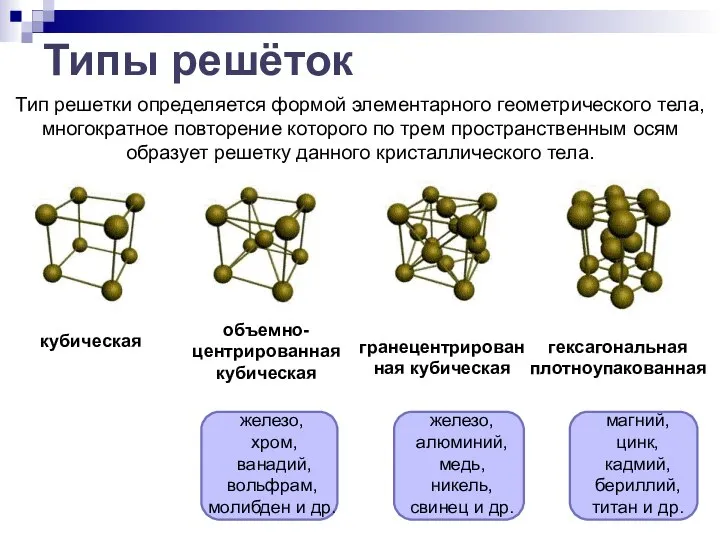
- 5. Типы решёток кубическая объемно-центрированная кубическая гранецентрированная кубическая гексагональная плотноупакованная железо, хром, ванадий, вольфрам, молибден и др.
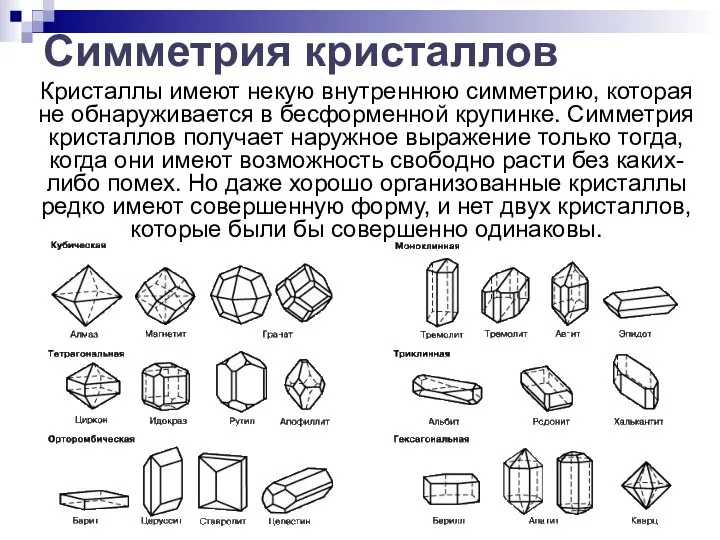
- 6. Кристаллы имеют некую внутреннюю симметрию, которая не обнаруживается в бесформенной крупинке. Симметрия кристаллов получает наружное выражение
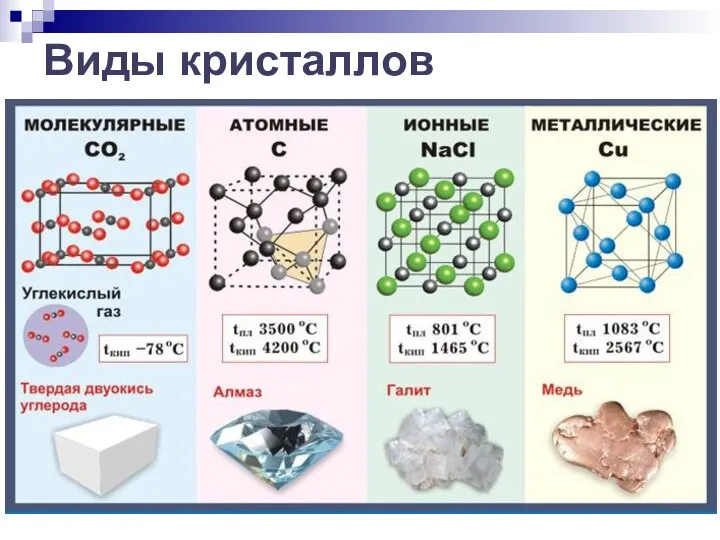
- 7. Виды кристаллов
- 8. Анизотропия Под анизотропией понимается неодинаковость механических и других свойств в кристаллических телах вдоль различных кристаллографических направлений.
- 9. Полиморфизм Некоторые кристаллы способны по достижении определенных температур изменять кристаллическое строение, т. е. изменять тип элементарной
- 10. Кристаллы образуются тремя путями: из расплава из раствора из паров Образование кристаллов Процесс кристаллизации требует определенного
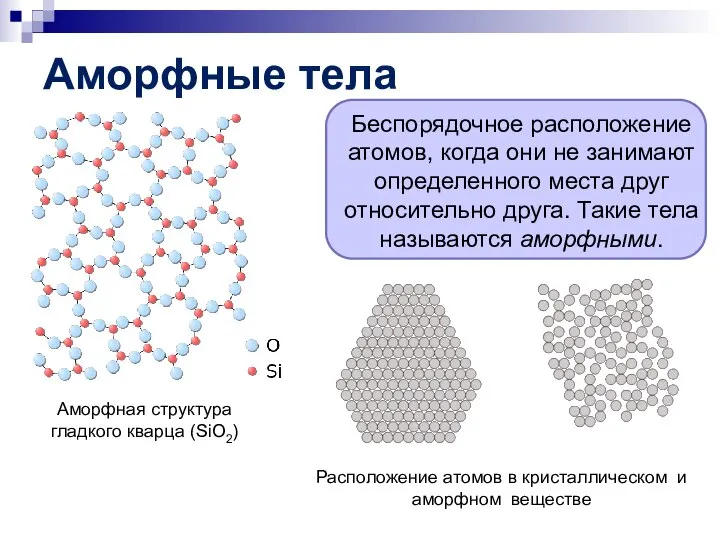
- 11. Аморфные тела Аморфная структура гладкого кварца (SiO2) Беспорядочное расположение атомов, когда они не занимают определенного места
- 12. Примеры аморфных тел
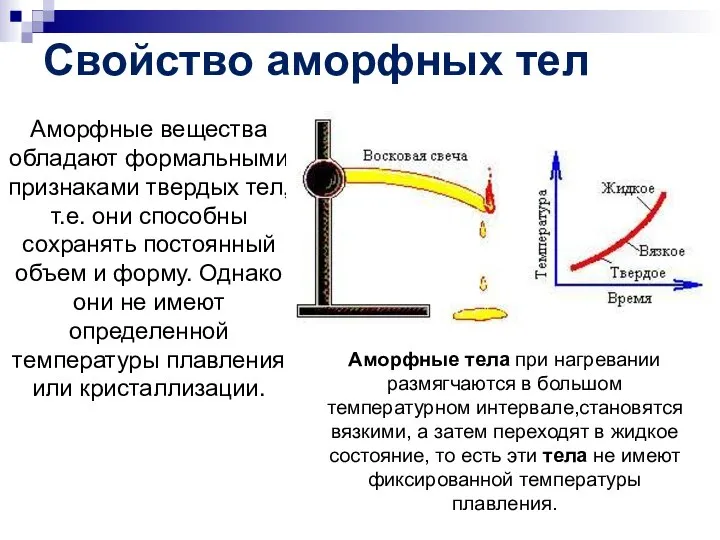
- 13. Свойство аморфных тел Аморфные вещества обладают формальными признаками твердых тел, т.е. они способны сохранять постоянный объем
- 14. В противоположность кристаллам, которые почти вечно сохраняют собственную форму, аморфные тела даже при невысоких температурах обладают
- 16. Скачать презентацию






 Слабые и сильные электролиты
Слабые и сильные электролиты Технология производства и свойства химических волокон и тканей из них
Технология производства и свойства химических волокон и тканей из них Физические свойства минералов
Физические свойства минералов Коррозия металлов
Коррозия металлов Модель атома
Модель атома Химические свойства металлов
Химические свойства металлов Выбор материала для изготовления зубчатых колес
Выбор материала для изготовления зубчатых колес Реакции ионного обмена. Электролитическая диссоциация
Реакции ионного обмена. Электролитическая диссоциация Альдегиды
Альдегиды Основы теории сплавов. Типы сплавов (твердые растворы, сплавы-смеси, сплавы- химические соединения. Диаграммы
Основы теории сплавов. Типы сплавов (твердые растворы, сплавы-смеси, сплавы- химические соединения. Диаграммы Многоатомные спирты
Многоатомные спирты Спирты
Спирты Кислородсодержащие органические соединения
Кислородсодержащие органические соединения Окислительно-восстановительные реакции
Окислительно-восстановительные реакции Водородные соединения неметаллов
Водородные соединения неметаллов Основные классы неорганических соединений
Основные классы неорганических соединений Презентация на тему Оксиды углерода
Презентация на тему Оксиды углерода  Кислородсодержащие органические вещества. Тест
Кислородсодержащие органические вещества. Тест Ниобий. Физиологическое действие
Ниобий. Физиологическое действие Характеристика элемента по его положению в периодической системе
Характеристика элемента по его положению в периодической системе Химия и производство
Химия и производство 8-29 класс (1)
8-29 класс (1) Виды оксидов азота
Виды оксидов азота Липиды. Состав липидов
Липиды. Состав липидов Характеристика химического элемента-неметалла на основании его положения в ПСХЭ Д.И.Менделеева. 9 класс
Характеристика химического элемента-неметалла на основании его положения в ПСХЭ Д.И.Менделеева. 9 класс Кислоты, их классификация и свойства
Кислоты, их классификация и свойства Пересчет данных анализа, выраженных в ионной форме
Пересчет данных анализа, выраженных в ионной форме Растворение. Экспериментальная работа с веществами
Растворение. Экспериментальная работа с веществами