Содержание
- 2. Атомы химических элементов изменяют степень окисления
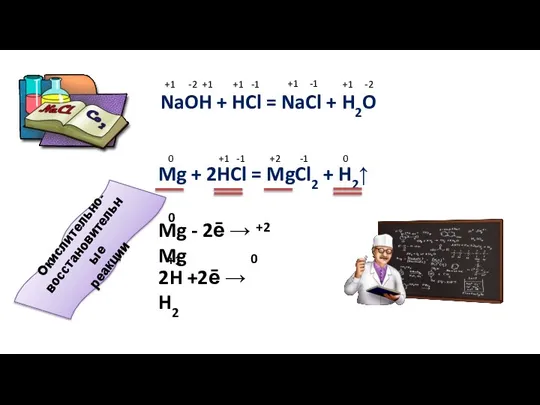
- 3. NaOH + HCl = NaCl + H2O -1 -2 +1 +1 -1 +1 -1 +1 -2
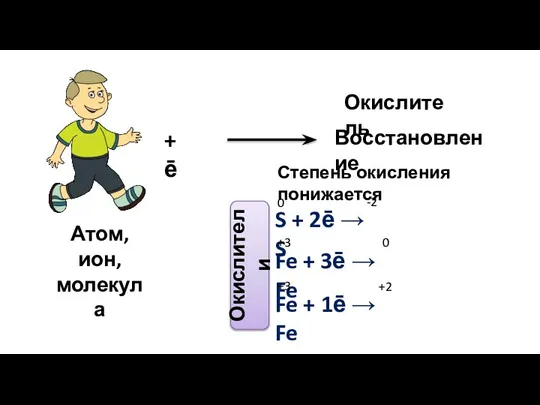
- 4. Атом, ион, молекула + ē Восстановление Степень окисления понижается S + 2ē → S 0 -2
- 5. Атом, ион, молекула - ē Окисление Степень окисления повышается Восстановитель Са - 2ē → Са 0
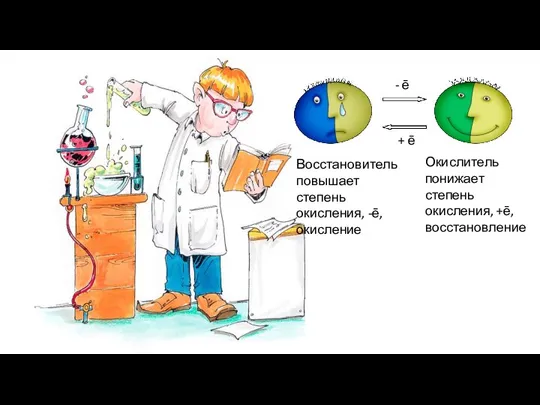
- 6. - ē + ē Восстановитель повышает степень окисления, -ē, окисление Окислитель понижает степень окисления, +ē, восстановление
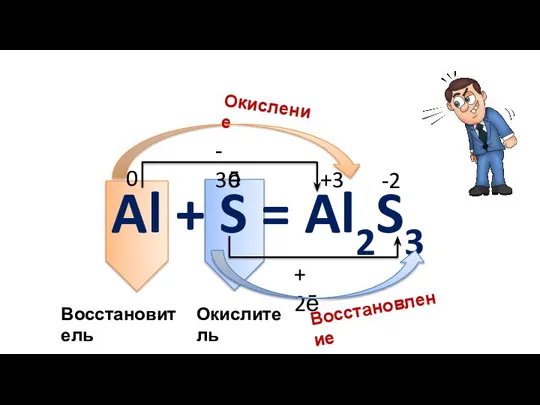
- 7. Al + S = Al2S3 0 +3 - 3ē Восстановитель Окисление 0 -2 + 2ē Окислитель
- 8. Al + S → Al2S3 0 0 +3 -2 Al - 3ē → Al 2 восстановитель;
- 9. Ag + HNO3 → AgNO3 + NO↑ + H2O 0 +1 +5 -2 +1 +5 -2
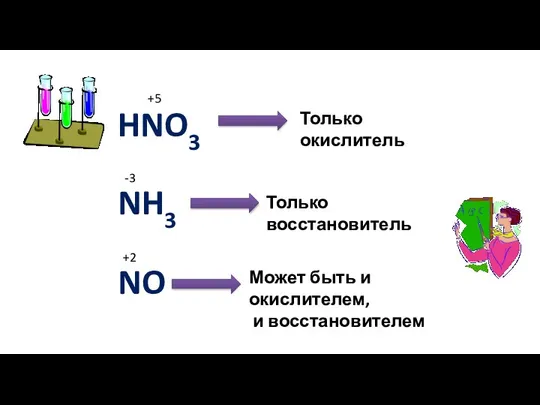
- 10. HNO3 +5 Только окислитель NH3 -3 Только восстановитель NO +2 Может быть и окислителем, и восстановителем
- 12. Скачать презентацию




 Пиримидин. Пиримидиновые основания
Пиримидин. Пиримидиновые основания Природный и попутные нефтяные газы
Природный и попутные нефтяные газы Железо 11 класс - Презентация_
Железо 11 класс - Презентация_ Презентация на тему Обобщение по типам химических реакций
Презентация на тему Обобщение по типам химических реакций 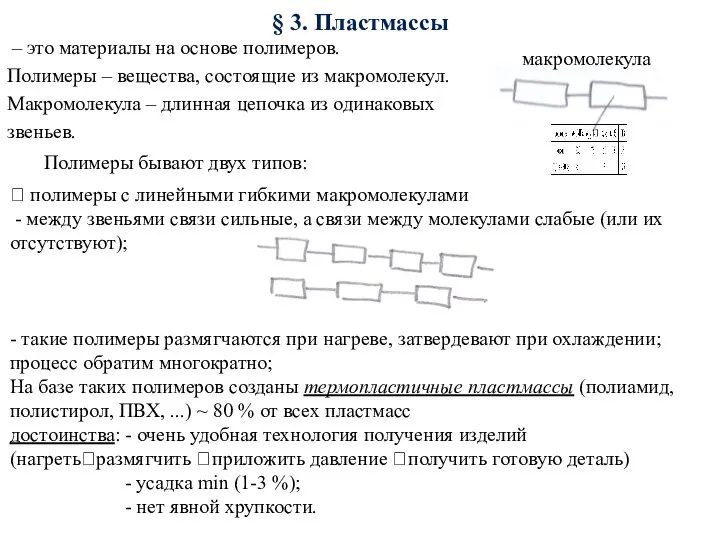 Пластмассы. Материалы, устойчивые против агрессивой среды
Пластмассы. Материалы, устойчивые против агрессивой среды Теория химического строения А. М. Бутлерова
Теория химического строения А. М. Бутлерова Химические методы количественного анализа веществ
Химические методы количественного анализа веществ Коррозия металлов
Коррозия металлов Методические рекомендации по преподаванию учебного предмета Химия в 2021-2022 учебном году
Методические рекомендации по преподаванию учебного предмета Химия в 2021-2022 учебном году Тренинг по решению задач разной степени сложности по теме Углеводороды
Тренинг по решению задач разной степени сложности по теме Углеводороды Органика в ЕГЭ (А)
Органика в ЕГЭ (А) Круговорот серы в природе
Круговорот серы в природе Химическая кинетика и равновесие
Химическая кинетика и равновесие Сырье, продукты, параметры гидроочистки
Сырье, продукты, параметры гидроочистки 01. Химический состав
01. Химический состав Синтетические органические соединения
Синтетические органические соединения Prezentatsia_lektsia_Reaktora_2_Materialny_balans
Prezentatsia_lektsia_Reaktora_2_Materialny_balans Подгруппа кислорода. Решение экспериментальных задач
Подгруппа кислорода. Решение экспериментальных задач Применение солей
Применение солей Лекция № 1
Лекция № 1 Презентация на тему Углеводороды (10 класс)
Презентация на тему Углеводороды (10 класс)  Характеристика d- элементов: Серебра, Цинка, Ртути
Характеристика d- элементов: Серебра, Цинка, Ртути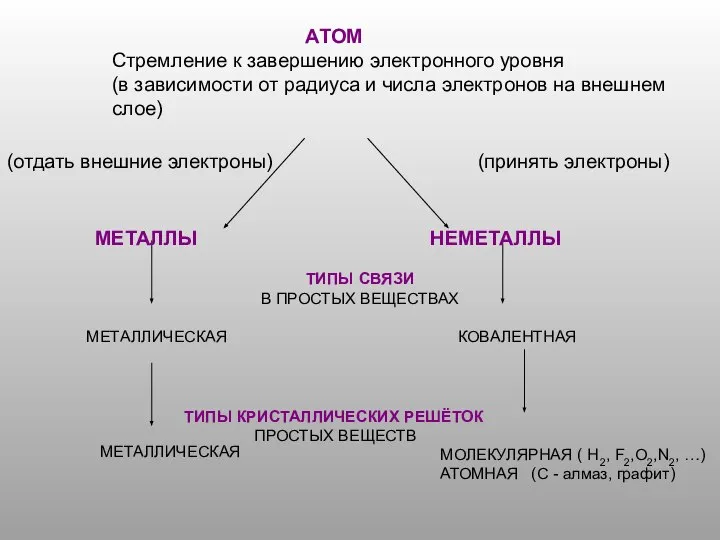 Атом. Стремление к завершению электронного уровня
Атом. Стремление к завершению электронного уровня Алкены
Алкены Растворы. Часть 2
Растворы. Часть 2 Количество вещества
Количество вещества Химический элемент калий
Химический элемент калий Полимеры. Пластмассы
Полимеры. Пластмассы