Содержание
- 2. ВСПОМНИТЕ! Чему равно общее количество электронов в атоме? Что такое энергетический уровень? Как определить число энергетических
- 3. Запомните! Электроны, расположенные на последней электронной оболочке, называются внешними. Число внешних электронов для химических элементов главных
- 4. Проверка домашнего задания
- 5. Проверьте себя и поставьте оценку, равную количеству правильных ответов Задание 1. Вариант 1. а) Al б)
- 6. ТЕМА УРОКА «Строение электронных оболочек атомов химических элементов №1-20».
- 7. Цель урока: научиться составлять электронные формулы атомов элементов первых трех периодов ПСХЭ; объяснять зависимость и закономерные
- 8. Электронная оболочка Совокупность всех электронов в атоме, окружающих ядро Каждый электрон имеет свою траекторию движения и
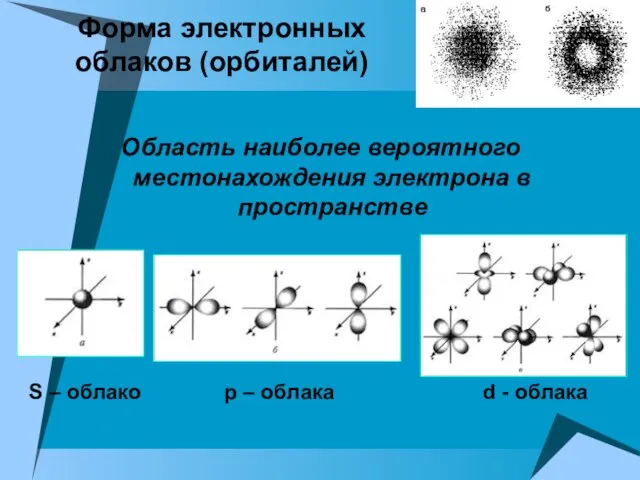
- 9. Форма электронных облаков (орбиталей) Область наиболее вероятного местонахождения электрона в пространстве S – облако р –
- 10. Алгоритм составления электронных формул. Записываем знак химического элемента и заряд ядра его атома – он равен
- 11. 1 период Н + 1 1 n=1 S 1 S1 Нe + 2 2 n=1 S
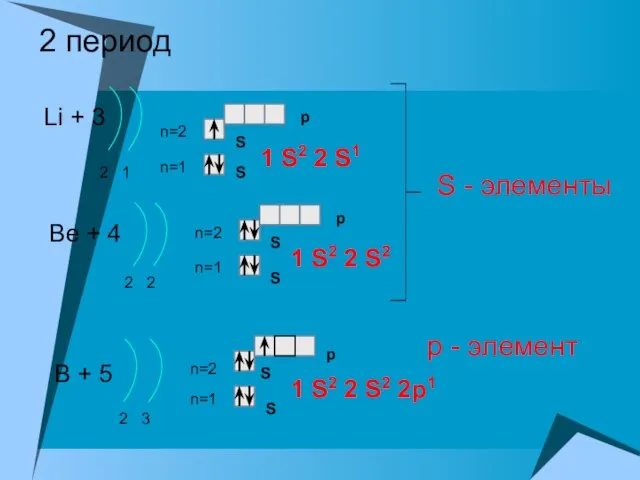
- 12. 2 период Li + 3 2 1 n=1 n=2 1 S2 2 S1 Be + 4
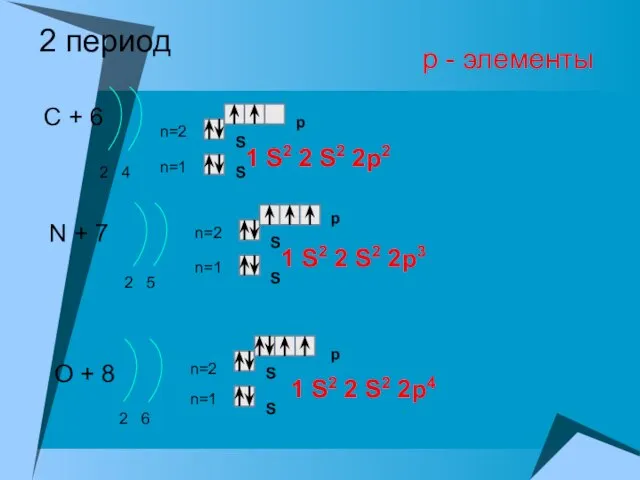
- 13. 2 период С + 6 2 4 n=1 n=2 N + 7 2 5 n=1 n=2
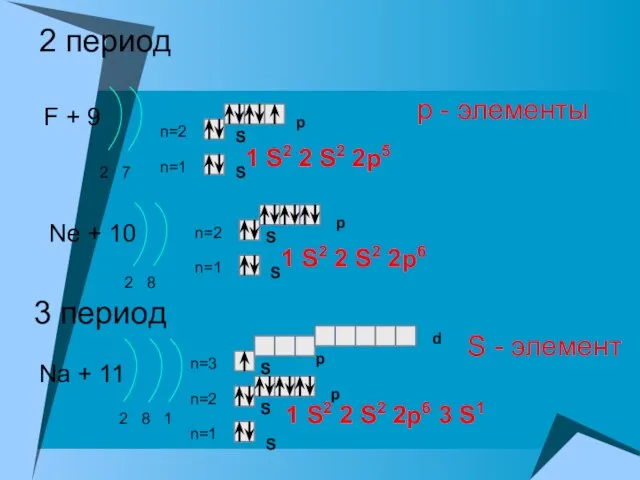
- 14. 2 период F + 9 2 7 n=1 n=2 Ne + 10 2 8 n=1 n=2
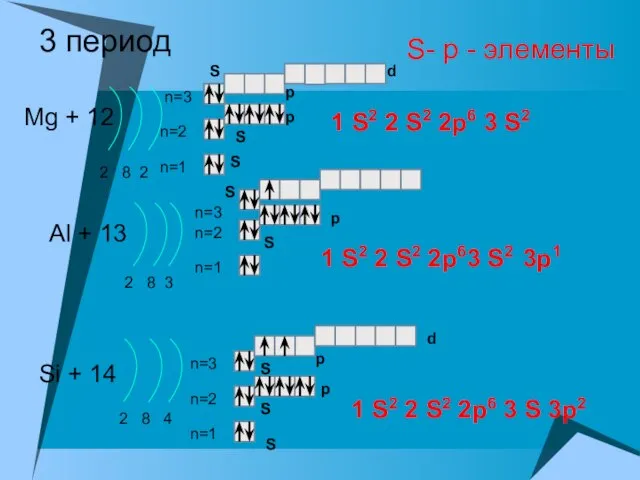
- 15. 3 период Mg + 12 2 8 2 n=1 n=2 Al + 13 2 8 3
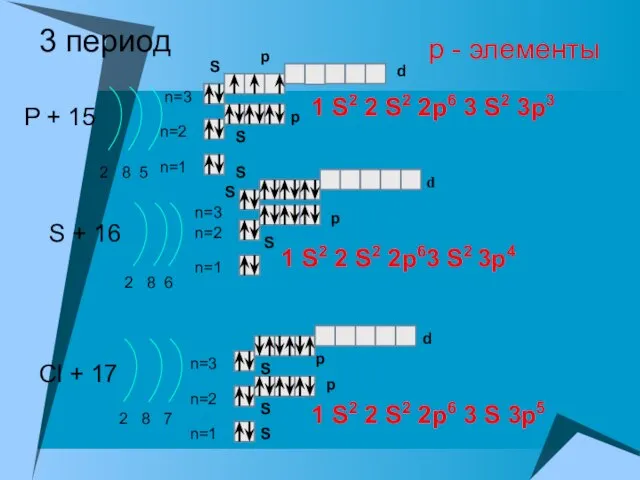
- 16. 3 период P + 15 2 8 5 n=1 n=2 S + 16 2 8 6
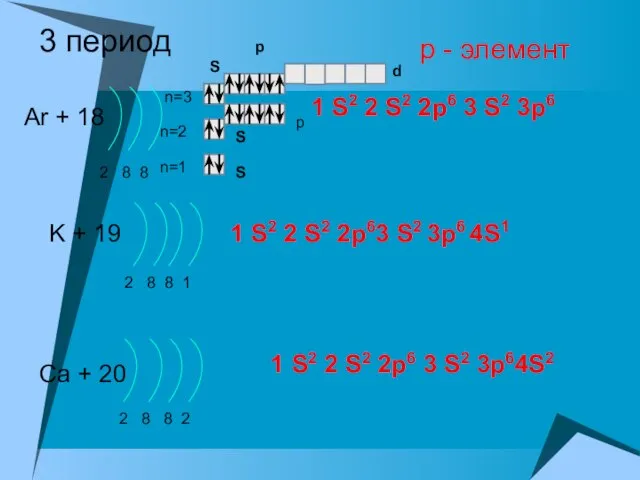
- 17. 3 период Ar + 18 2 8 8 n=1 n=2 K + 19 2 8 8
- 18. Физкультминутка Руки подняли и покачали – Это деревья в лесу. Руки согнули, кисти встряхнули – Ветер
- 19. Игра в «Крестики- нолики» выигрышный путь составляют : А)элементы одного периода
- 20. Игра в «Крестики- нолики» выигрышный путь составляют : б)элементы одной главной подгруппы
- 21. Игра в «Крестики- нолики» выигрышный путь составляют : в)элементы, расположенные рядом в ПСХЭ
- 22. Рефлексия Я все понял, могу объяснить другому По данной теме у меня остались вопросы Недостаточно понял
- 23. Ответьте на вопросы Какие данные об особенностях строения атома отражает электронная формула? В чем заключается причина
- 24. Выводы Причина сходства элементов заключается в одинаковом строении внешних энергетических уровней их атомов Одинаковое строение внешних
- 25. Домашнее задание Повторить основные понятия темы на странице 32-33 учебника Задание 3 письменно Выполнить индивидуальное задание
- 27. Скачать презентацию

















 Электронное и пространственное строение молекулы метана Учитель химии МБОУ СОШ № 9 МО ЩР станица Новощербиновская Степучева Ол
Электронное и пространственное строение молекулы метана Учитель химии МБОУ СОШ № 9 МО ЩР станица Новощербиновская Степучева Ол Презентация на тему Лекарства
Презентация на тему Лекарства  Презентация в 8 классе к уроку по химии на тему__
Презентация в 8 классе к уроку по химии на тему__ Металлы и их соединения
Металлы и их соединения Органическая химия
Органическая химия Лабораторно-практическое занятие № 5. Неметаллические материалы
Лабораторно-практическое занятие № 5. Неметаллические материалы Основания и их свойства
Основания и их свойства Аммиак
Аммиак Кислоты в химии
Кислоты в химии Химические свойства оснований
Химические свойства оснований Железо как химический элемент
Железо как химический элемент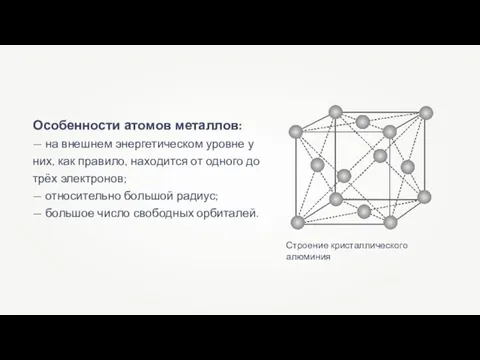 Металлическая химическая связь
Металлическая химическая связь Физическая химия растворов электролитов
Физическая химия растворов электролитов Окисники, відновники
Окисники, відновники Валентность
Валентность Сплавы, растворы, смеси
Сплавы, растворы, смеси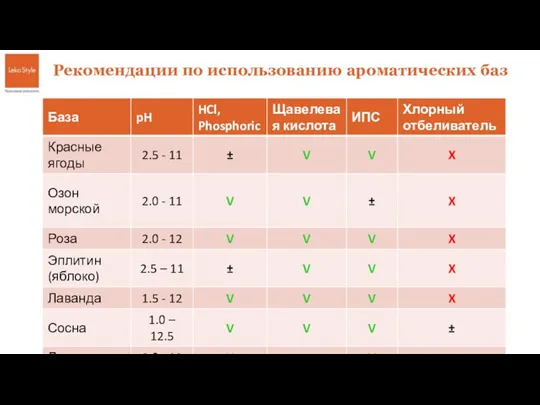 Базы для кислых и щелочных сред
Базы для кислых и щелочных сред Экстракция
Экстракция Презентация на тему Мусор
Презентация на тему Мусор  Химия и география. Викторина
Химия и география. Викторина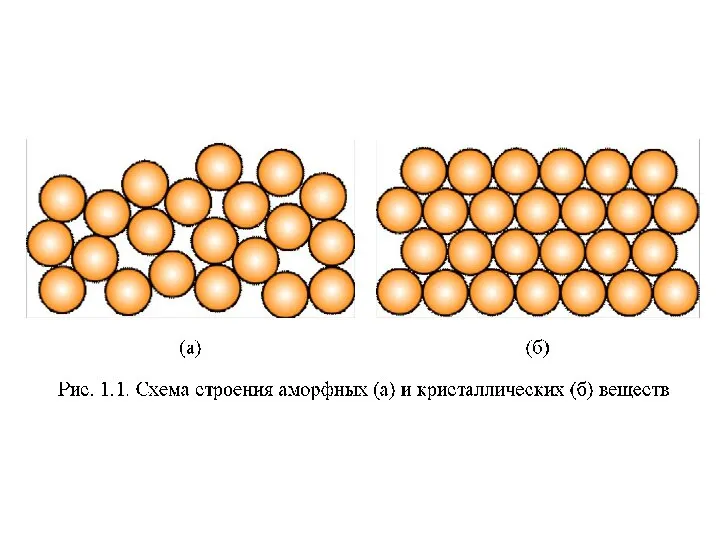 Материаловедение
Материаловедение Сероводород, сульфиды
Сероводород, сульфиды Пептиды, белки. Лабораторное занятие
Пептиды, белки. Лабораторное занятие Алкены
Алкены Получение и применение аренов
Получение и применение аренов Волокна
Волокна Электролитическая диссоциация веществ Реакции ионного обмена и условия их протекания
Электролитическая диссоциация веществ Реакции ионного обмена и условия их протекания Презентация на тему Химические свойства и применение алканов
Презентация на тему Химические свойства и применение алканов