Слайд 2Сложные вещества
Оксиды
Кислоты
Основания
Соли
Основные
Кислотные
Амфотерные
Бескислородные
Кислородсодержащие
Щелочи
Нерастворимые в воде
Средние
Кислые
Основные
Двойные

Слайд 3Закончите уравнения осуществимых реакций:
H2SO4 + Ba(OH)2
HNO3 + Fe2O3
HCl + AgNO3
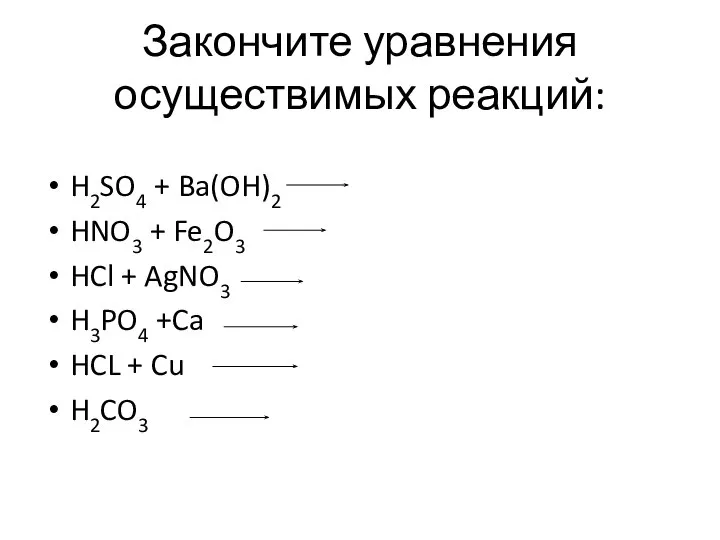
H3PO4 +Ca
HCL + Cu
H2CO3
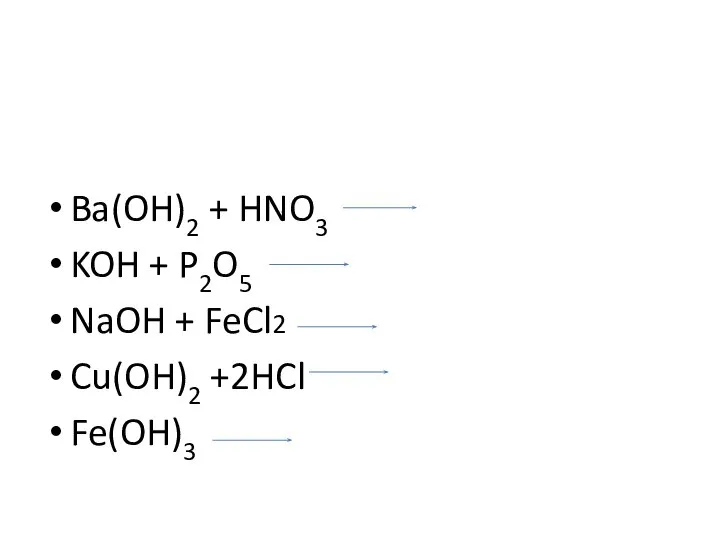
Слайд 4Ba(OH)2 + HNO3
KOH + P2O5
NaOH + FeCl2
Cu(OH)2 +2HCl
Fe(OH)3
Слайд 5ТЕСТ
1) Из предложенного перечня выберите основной оксид
а) K2O б) SO3 в)

CO2
2) В результате взаимодействия с водой Na2O образуется
а) основание б) кислота в) соль
3) Какая из веществ в быту называется поваренной солью
а) Na2CO3 б) NaNO3 в) NaCl г) Na3PO4
4) Какой металл не реагирует с соляной кислотой
а) Mg б) Ag в) Fe
5)Что из перечисленного подходит гидроксиду натрия
а) щелочь б) двухосновная в) нерастворима в воде
6) Вещества какой пары могут реагировать между собой
а) СO2 + HCl б) CaO + HCl в) CaO + NaOH




 Алкадиены
Алкадиены Обмен жиров в организме млекопитающего
Обмен жиров в организме млекопитающего Бинарные соединения – оксиды и летучие водородные соединения. 8 класс
Бинарные соединения – оксиды и летучие водородные соединения. 8 класс Научно-познавательное шоу Юный химик
Научно-познавательное шоу Юный химик Расчет по химическим уравнениям
Расчет по химическим уравнениям Презентация на тему Влияние пищевых добавок на здоровье человека
Презентация на тему Влияние пищевых добавок на здоровье человека  Презентация на тему Биография Д. И. Менделеева
Презентация на тему Биография Д. И. Менделеева  Изучение микроклимата коровника с целью создания системы очистки воздуха от аммиака
Изучение микроклимата коровника с целью создания системы очистки воздуха от аммиака Окислительно-восстановительные реакции (ОВР). Лекция 1
Окислительно-восстановительные реакции (ОВР). Лекция 1 Химия жиров (липидов)
Химия жиров (липидов) Основи масообміну
Основи масообміну География. Уральские самоцветы
География. Уральские самоцветы Общие химические свойства неметаллов
Общие химические свойства неметаллов Кислоты. Строение, классификации и свойства неорганических кислот
Кислоты. Строение, классификации и свойства неорганических кислот Химическая лаборатория
Химическая лаборатория Анилин (амидобензол, аминобензол, фениламин)
Анилин (амидобензол, аминобензол, фениламин) Возможности модернизации совместного производства фенола и ацетона кумольным способом
Возможности модернизации совместного производства фенола и ацетона кумольным способом Карбоновые кислоты
Карбоновые кислоты Предельные углеводороды. Урок №4
Предельные углеводороды. Урок №4 Химическая коррозия
Химическая коррозия Общие способы получения металлов
Общие способы получения металлов 11 типы связей
11 типы связей Соединения азота
Соединения азота Биохимия крови
Биохимия крови Презентация по Химии "Использование исследовательских и информационно-коммуникационных технологий в обучении химии" - скача
Презентация по Химии "Использование исследовательских и информационно-коммуникационных технологий в обучении химии" - скача Гидролиз солей
Гидролиз солей Самородные металлы
Самородные металлы Презентация на тему Алканы
Презентация на тему Алканы