Содержание
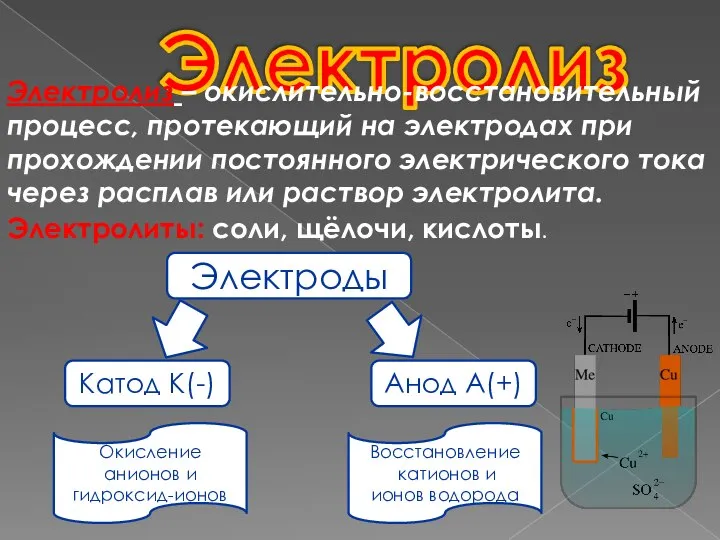
- 2. Электролиз Электролиз – окислительно-восстановительный процесс, протекающий на электродах при прохождении постоянного электрического тока через расплав или
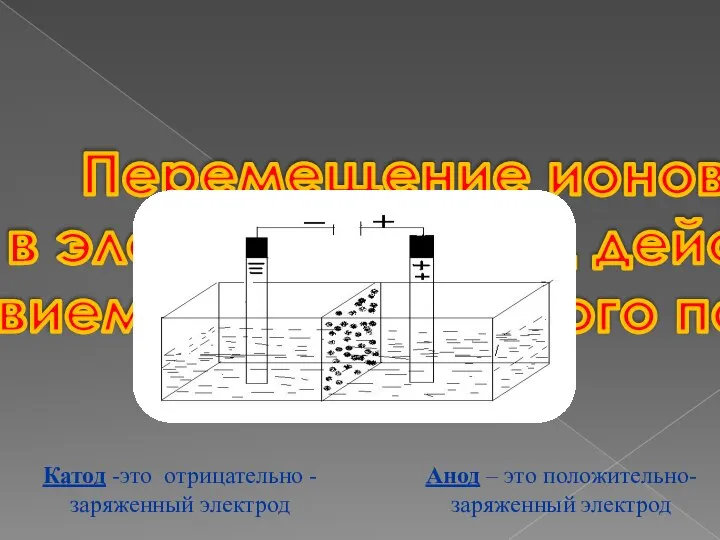
- 3. Перемещение ионов в электролите под дейст- вием электрического поля Анод – это положительно- заряженный электрод Катод
- 4. Процесс на катоде Если в растворе ионы Н+ - они разряжаются до Н2 Металлы правее Н:
- 5. Процесс на аноде если анод растворяется (железо, цинк, медь, серебро и все металлы, которые окисляются в
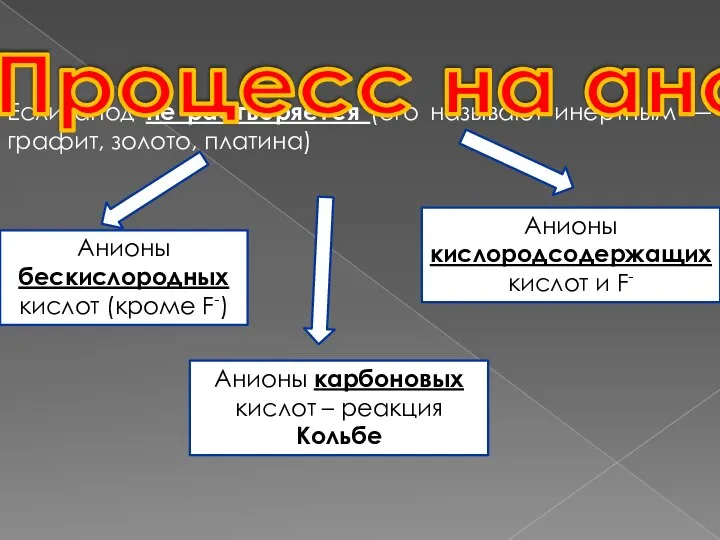
- 6. Если анод не растворяется (его называют инертным — графит, золото, платина) Процесс на аноде Анионы бескислородных
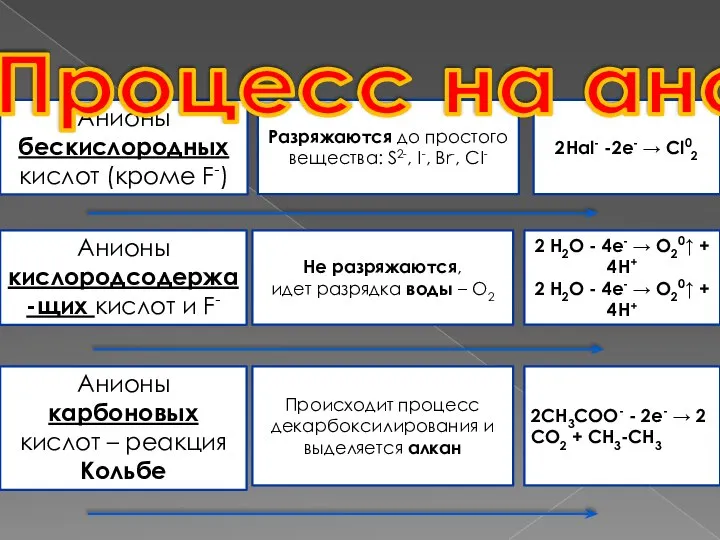
- 7. Анионы бескислородных кислот (кроме F-) Разряжаются до простого вещества: S2-, I-, Br-, СI- 2Hal- -2e- →
- 8. Закон электролиза Законы Фарадея. Масса веществ, выделившегося на электроде при электролизе, пропорциональна количеству электричества, прошедшее через
- 9. Применение электролиза Для получения щёлочных, щёлочноземельных металлов, алюминия, лантаноидов Для получения точных металлических копий, что называется
- 11. Скачать презентацию




 Закономерности управления каталитическими процессами. Катализ
Закономерности управления каталитическими процессами. Катализ Количество вещества. Моль. Молярная масса
Количество вещества. Моль. Молярная масса Химические свойства металлов
Химические свойства металлов Строение атома
Строение атома Шоу Юный химик
Шоу Юный химик Химические свойства
Химические свойства Анилин. Строение и свойства анилина
Анилин. Строение и свойства анилина Indikatori. R. Boila eksperiments
Indikatori. R. Boila eksperiments VVEDENIE_V_OGRANIChESKUYu_KhIMIYu
VVEDENIE_V_OGRANIChESKUYu_KhIMIYu Презентация
Презентация Химическая кинетика и равновесие
Химическая кинетика и равновесие Генетическая связь веществ. Виды реакций
Генетическая связь веществ. Виды реакций Строение атома. Планетарная модель атома Резерфорда
Строение атома. Планетарная модель атома Резерфорда ОГЭ химия. Основной государственный экзамен
ОГЭ химия. Основной государственный экзамен Уравнения химических реакций
Уравнения химических реакций Вспоминаем химию
Вспоминаем химию Презентация на тему Степень окисления 8 класс
Презентация на тему Степень окисления 8 класс  Углеводороды. Урок-игра
Углеводороды. Урок-игра Ситалл – искусственный поликристаллический материал
Ситалл – искусственный поликристаллический материал Презентация на тему Предельные одноатомные спирты
Презентация на тему Предельные одноатомные спирты  Определение воды по Фишеру. Кислотное число, число омыления. Определение аминного азота
Определение воды по Фишеру. Кислотное число, число омыления. Определение аминного азота Вещество и тело. Чистые вещества и смеси
Вещество и тело. Чистые вещества и смеси Кислоты. Классификация. Номенклатура
Кислоты. Классификация. Номенклатура Растворы. Квалификации химических веществ:
Растворы. Квалификации химических веществ: Исследование воздействия плазмы метана на свойства оксида графена
Исследование воздействия плазмы метана на свойства оксида графена Азот
Азот Изомерия, её виды
Изомерия, её виды Гидролиз солей – частный случай РИО
Гидролиз солей – частный случай РИО