Слайд 2
С точки зрения теории электролитической диссоциации:
Элекролиты – это вещества, растворы

и/или
расплавы которых проводят электрический ток
( кислоты, основания, соли).
Электролиты в растворах и расплавах подвергаются процессу электролитической диссоциации- распаду молекул на ионы.
Слайд 3 Количественной характеристикой способности электролита распадаться на ионы является величина
степени диссоциации

электролита (α),
которая показывает отношение числа молекул, распавшихся на ионы, к общему числу растворенных молекул электролита
α = Nион | N раств
Слайд 4 По величине α электролиты классифицируют на :
Сильные электролиты: α ˃ 0,3

(больше 30 %)
2. Средней силы электролиты 0,3 ˃ α ˃ 0,03
(от 3 до 30 %)
3. Слабые электролиты α ˂ 0,03 (меньше 3%)
Слайд 5 Константа диссоциации электролита определяется законом действующих масс: К А ↔ К+ +
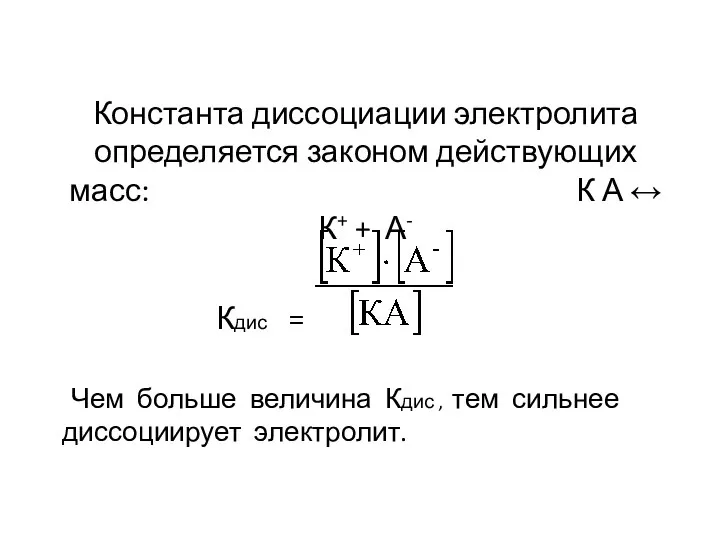
А-
Кдис =
Чем больше величина Кдис , тем сильнее диссоциирует электролит.
Слайд 6 Для оценки концентрационных эффектов в растворах сильных электролитов вводится величина
активности

электролита - а(Х)
Под активностью электролита Х понимают эффективную концентрацию электролита, в соответствии с которой он участвует в различных процессах.
Слайд 7Активность связана с истинной концентрацией растворенного вещества соотношением:
а (х) = f(х)·

С (х)
С(х)- концентрация электролита, моль/л
а(х)- активность электролита, моль/л
f(х)- коэффициент активности; выражает отклонение свойств раствора с концентрацией С(х) от свойств идеального бесконечно разбавленного раствора данного электролита. Принимает значения от 0 до 1.
Слайд 8
Ионной силой раствора (I ) называют величину, равную полусумме произведения

моляльной концентрации находящихся в растворе ионов на квадрат заряда каждого иона.
- моляльная концентрация ионов данного вида;
показывает содержание количества (моль) ионов в килограмме растворителя; моль/кг
– ионная сила раствора; характеризует суммарную активность ионов в растворе с учетом сил межионного взаимодействия; моль/кг
– заряд иона
Слайд 9 Для биологических систем in vivo:
Iфиз = 0,15 моль/кг
Растворы, применяемые

в медицинской практике и имеющие ионную силу равную 0,15 моль/кг называются физиологическими растворами.
Слайд 10Ионное произведение воды.
Водородный показатель среды растворов.

Слайд 11
Н2 О↔Н + + ОН-
Н2 О + Н + ↔ Н3
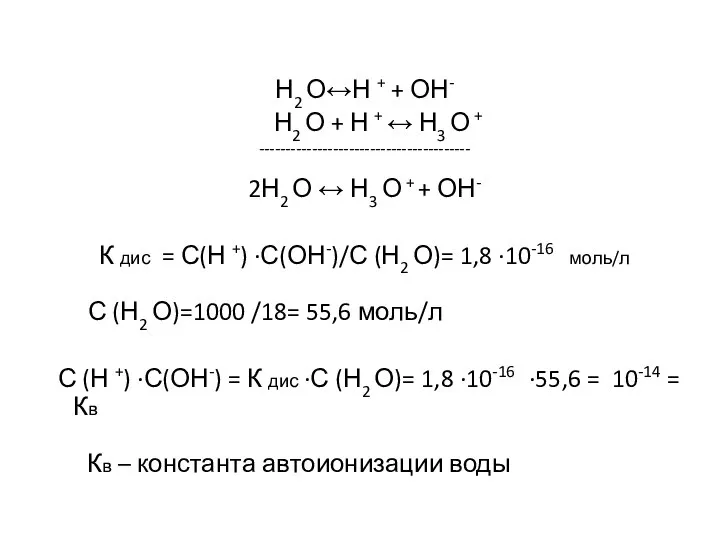
О +
----------------------------------------
2Н2 О ↔ Н3 О + + ОН-
К дис = С(Н +) ·С(ОН-)/С (Н2 О)= 1,8 ·10-16 моль/л
С (Н2 О)=1000 /18= 55,6 моль/л
С (Н +) ·С(ОН-) = К дис ·С (Н2 О)= 1,8 ·10-16 ·55,6 = 10-14 = Кв
Кв – константа автоионизации воды
Слайд 12Уравнение ионного произведения воды имеет вид:
Кв = С(Н +) ·С(ОН-)= 10-14 при

298 К
в чистой воде и растворе любого электролита при данной температуре произведение концентрации (активности) ионов водорода и гидроксид-ионов
есть величина постоянная, называемая константой автоионизации воды.
Слайд 13 В чистой дистилированной воде:
С(Н +) = С(ОН-) = 10-14 =

10-7 моль/л
По величине С(Н +) определяют реакцию среды раствора:
Нейтральная среда: С(Н +) =10-7 моль/л
Кислая среда: С(Н +) ˃ 10-7 моль/л (10-6 и т.д.)
3. Щелочная среда: С(Н +) ˂ 10-7 моль/л(10-8 и т.д.)
Слайд 14Водородный показатель среды раствора ( рН ) –
численно равен отрицательному десятичному

логарифму концентрации (активности) ионов водорода в растворе.
рН = - lg С(Н+)
Гидроксильный показатель среды раствора (рОН)-
численно равен отрицательному десятичному логарифму концентрации (активности) гидроксид-ионов в в растворе.
рОН = - lg С(ОН-)
Слайд 15
Величина рН раствора указывает на реакцию среды раствора:
Нейтральная среда: рН = 7
2.

Кислая среда: рН ˂ 7
3. Щелочная среда: рН ˃ 7
Слайд 16 Если взять отрицательный десятичный логарифм выражения ионного произведения воды, то уравнение

принимает вид:
- lg [С(Н +) ·С(ОН-) ] = - lg 10-14
[- lg С(Н +) ] + [- lg С(ОН-) ] = 14
получаем:
рН + рОН = 14















 Атом
Атом Презентация 1
Презентация 1 Виды нагрева и материалы резистивных нагревателей, их стойкость к температуре, ростовой атмосфере и расплаву
Виды нагрева и материалы резистивных нагревателей, их стойкость к температуре, ростовой атмосфере и расплаву Получение аминов
Получение аминов Расчеты по уравнениям химических реакций
Расчеты по уравнениям химических реакций Оксиды, их классификация и химические свойства. 8 класс
Оксиды, их классификация и химические свойства. 8 класс Строение вещества
Строение вещества Виды химической связи. Обобщение и систематизация знаний
Виды химической связи. Обобщение и систематизация знаний Химические реакции
Химические реакции Морфологогия минералов
Морфологогия минералов Природа и типы химических связей
Природа и типы химических связей Презентация на тему Вещества и их свойства
Презентация на тему Вещества и их свойства  ВКР: Определение показателей качества мясной и колбасной продукции различных производителей
ВКР: Определение показателей качества мясной и колбасной продукции различных производителей Презентация на тему Физические и химические явления 8 класс
Презентация на тему Физические и химические явления 8 класс  Изомерия. Виды изомерии
Изомерия. Виды изомерии Презентация на тему Халькогены
Презентация на тему Халькогены  Азотная кислота
Азотная кислота Метелёва И.Е. учитель химии
Метелёва И.Е. учитель химии Решение заданий ОГЭ по химии (1 - 15)
Решение заданий ОГЭ по химии (1 - 15) Химия и производство
Химия и производство Алканы
Алканы Анализ воды природных источников посёлков Фруктовая и Красная Пойма городского округа Луховицы
Анализ воды природных источников посёлков Фруктовая и Красная Пойма городского округа Луховицы Салициловая кислота
Салициловая кислота Масляная кислота
Масляная кислота Кумарон - индендық полимерлер
Кумарон - индендық полимерлер Классификация химических реакций
Классификация химических реакций Нефть
Нефть Водородная химическая связь
Водородная химическая связь