Слайд 2Вспомним о водороде.
Химический знак водорода. Его положение в ПСХЭ.
Распространение водорода.
Способы получения

и определения.
Физические свойства.
Химические свойства. Чем является водород в ХР?
Применение.
Слайд 3Запишем д/з:
§14 прочитать, составить кроссворд из 10 любых химических терминов.

Слайд 4Нахождение в природе
Кислород самый распространенный на Земле элемент.
1. В атмосфере около 21%

по V;
2. В литосфере (твердой оболочке Земли) -47% по m - (он входит в состав большинства горных пород и более чем 1000 минералов);
3. В гидросфере (водной оболочке нашей планеты) -почти 86% по m.
Образуется в ходе процесса фотосинтеза
СО2 + Н2О → С6Н12О6 +О2 ↑
Уравните ХР
Слайд 5Открытие кислорода
Официально открытие принадлежит Джозефу Присли.
(1 августа 1774 году путём разложения оксида

ртути в герметично закрытом сосуде. Пристли направлял на это соединение солнечные лучи с помощью мощной линзы).
HgO=Hg +O2 уравнить
В 1775 году Антуан Лавуазье установил, что кислород является составной частью воздуха, кислот и содержится во многих веществах.
В 1771 году кислород получил шведский химик Карл Шееле.
Слайд 6АЛЛОТРОПИЯ КИСЛОРОДА: элементу-О соответствуют 2 простых вещества
Газ кислород -О2
Газ озон - О3

образуется из кислорода под действием УФ или эл.разряда 3О2↔2О3
Слайд 7Физические свойства
1.Кислород-газ без цвета, запаха и вкуса, мало растворим в воде, тяжелее

воздуха, Ткип.=-183 0С; Тпл.=-218,8 0С
2. Озон-газ синего цвета с характерным запахом, в жидком виде -фиолетового цвета (при Т=-1110С), в твердом виде- черного цвета (при Т=-2510С), в 10 раз лучше растворяется в воде, чем кислород, гораздо тяжелее воздуха
Слайд 8Получение кислорода
KMnO4 →K2MnO4+MnO2 +O2
KNO3 →KNO2 +O2
H2O2 →H2O + O2
Уравнить

Слайд 9Химические свойства кислорода

Слайд 10
Горение железа.
Fe + О2 → Fe2O3
уравнить

Слайд 11 Горение фосфора.
Р + О2 → Р2O5
уравнить

Слайд 12Горение серы.
S + О2 → SO2
уравнить

Слайд 13ПРАВИЛА ДОПИСЫВАНИЯ УРАВНЕНИЙ РЕАКЦИЙ СОЕДИНЕНИЯ.
1.Записать элементы вместе.
2.Поставить с.о. элементов. Снести их крест-накрест,

если, надо- сократить.
3.Определить индексы.
4.Расставить коэффициенты.
Слайд 14Дописать и уравнить:
1. Ca + O2 →
2. H2 + O2

→
3. Si + O2 →
4. N2 + O2 →
5. С2H6 + O2 →
Слайд 15Угадать пропущенное вещество
… + O2 → As2O3
Li + O2 →…
Mg + …

→ MgO
… + O2 → NO
Be + O2 → …
Слайд 16Применение
1.Медицина
Абсолютно необходимый элемент системы жизнеобеспечения любой больницы. Применяется при анестезии, для

работы ИВЛ, физиотерапии.
2.Ветеринария
При анестезии животных, озонировании для дезинфекции.
3.Косметология, спорт и фитнес
Оксигенотерапия в косметологии, оздоровительные процедуры в виде кислородных коктейлей и ароматерапии.
4.Металлургия
Кислород в больших объемах используется при производстве черных и цветных металлов.
5.Газовая сварка, резка и пайка металлов
Одно из самых важных и распространенных областей применения кислорода.
6.Стекольная промышленность.В стекловаренных печах для повышения температуры.
7.Химическая и нефтехимическая промышленность
Широко используется для окисления исходных реагентов.
8.Озонирование для водоподготовки, очистки сточных вод, отбеливания целлюлозы и т. д.
9.Рыборазведение.Способствует увеличению выхода мальков, сокращению срока инкубации и т. д.
10.Утилизация отходов в мусоросжигательных печах.
Слайд 17Итог (рассшифруйте слова-основное предназначение кислорода.Ключ к разгадке- по порядковый номер элемента) :

O
4 50 45 63 28 53 63 53 105 Ы 108 13 28 53 63

















 Химическое равновесие
Химическое равновесие Химия и география. Блиц-опрос. 7 класс
Химия и география. Блиц-опрос. 7 класс Амилаза. Строение амилазы
Амилаза. Строение амилазы Моющие и чистящие средства
Моющие и чистящие средства Основные химические законы
Основные химические законы Соли: получение
Соли: получение Синтетическое моторное масло. Маркировка моторных масел
Синтетическое моторное масло. Маркировка моторных масел Khim_8
Khim_8 Химические реакции
Химические реакции Систематизация знаний по периодической системе химических элементов
Систематизация знаний по периодической системе химических элементов химия
химия Nevarne snovi
Nevarne snovi Основания. Классификация
Основания. Классификация Стелс-материалы
Стелс-материалы Тип кристаллической решетки у белого фосфора…. Тест
Тип кристаллической решетки у белого фосфора…. Тест Классификация и свойства кислот
Классификация и свойства кислот Сeквенирование нуклеиновых кислот
Сeквенирование нуклеиновых кислот Набор для выращивания монокристалла. Защита проекта
Набор для выращивания монокристалла. Защита проекта Алканы. Строение, номенклатура, изомерия, физические свойства
Алканы. Строение, номенклатура, изомерия, физические свойства Реакции разложения и соединения
Реакции разложения и соединения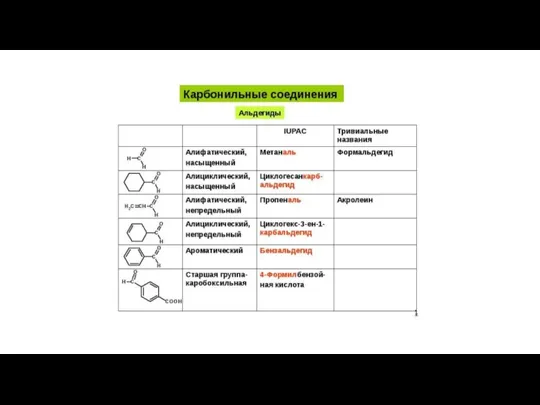 Карбонильные соединения (альдегиды)
Карбонильные соединения (альдегиды) карбоновые кислоты
карбоновые кислоты Вуглеводи. Групи
Вуглеводи. Групи Вычисление температур стеклования полимера при различных степенях отверждения смолы
Вычисление температур стеклования полимера при различных степенях отверждения смолы Сера
Сера Валенттілік. Атом-молекулалы ілім
Валенттілік. Атом-молекулалы ілім Классификация органических соединений
Классификация органических соединений Метанол. Краткая характеристика
Метанол. Краткая характеристика