Слайд 2Ответить на вопросы
Какие вещества называют восстановителями? Что происходит с их степенью окисления?
Приведите

примеры важнейших восстановителей, из простых веществ и сложных веществ.
Отчего зависит восстановительные способности веществ?
Слайд 3Ответить на вопросы
Какие вещества называют окислителями? Что происходит с их степенью окисления

при химических реакциях?
Какие вещества проявляют окислительные свойства? Приведите примеры.
От чего зависят окислительные свойства ?
Слайд 4Ответить на вопросы
Назовите основные типы окислительно-восстановительных реакций.
Приведите примеры реакций:
а) межмолекулярные,

б) внутримолекулярные,
в) диспропорционирования
Слайд 5Выполнить упражнения
Выбрать из реакций окислительно-восстановительные, расставить степени окисления всех элементов, определить

тип окислительно - восстановительной реакции, указать окислитель и восстановитель.
Cu(OH)2 → CuO + H2O
Cu(NO3)2 → CuO + NO2 + O2
HNO2 → NO + NO2 + H2O
P + CI2 → PCI5
H2O + SO2 → H2SO3
Ca(OH)2 +CO2 → CaCO3 + H2O
Слайд 6Электролиз
- это окислительно-восстановительный процесс, протекающий на электродах при прохождении электрического тока через
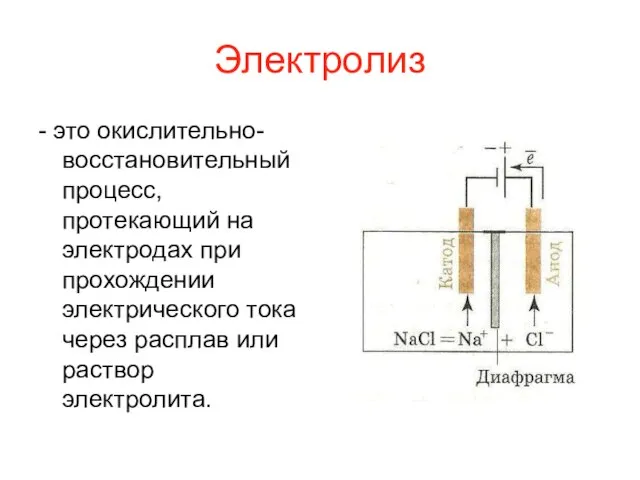
расплав или раствор электролита.
Слайд 7Электролиз расплавов
Подвергаются: щелочи, термически устойчивые соли, оксиды металлов.

Слайд 9Электролиз растворов
Порядок разрядки анионов
В первую очередь разряжаются бескислородные ионы: S2-, I-, Br-,

CI- и анионы органических кислот 2RCOO- - 2e→ 2CO2 + R-R.
Во вторую очередь разряжается гидроксид-ион (в щелочной среде): 4OH- - 4e → O2 + 2H2O или вода (в кислой и нейтральной среде) 2H2O – 4e → O2 + 4H+.
В растворе не разряжаются анионы кислородсодержащих кислотных остатков и фторид-ион.
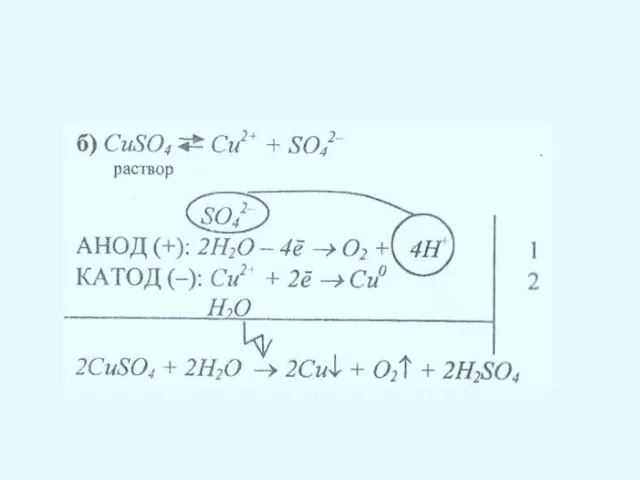
Слайд 10Электролиз раствора
Порядок разрядки катионов
В первую очередь на катоде разряжаются катионы металлов, стоящих

в ряду напряжений металлов после водорода.
Во вторую очередь в кислотной среде разряжаются катионы водорода: 2H+ + 2e → H2 или вода (в нейтральной и щелочной среде) 2H2O+2e → H2+OH-
Одновременно с водой могут разряжаться катионы металлов стоящих в ряду напряжений от алюминия до водорода.
В растворах никогда не разряжаются катионы металлов, стоящих в ряду напряжений до алюминия (включительно).











 Химические средства защиты растений
Химические средства защиты растений Уровень С1 в ГИА
Уровень С1 в ГИА Получение дисперсных систем. Метод конденсации. Метод диспергирования. Эффект Ребиндера. Лекция 11
Получение дисперсных систем. Метод конденсации. Метод диспергирования. Эффект Ребиндера. Лекция 11 Окислительно-восстановительные реакции (1)
Окислительно-восстановительные реакции (1) Фенол
Фенол Гравиметрический анализ (ГА) - метод количественного химического анализа, основанный на точном измерении массы определяемого
Гравиметрический анализ (ГА) - метод количественного химического анализа, основанный на точном измерении массы определяемого Коагуляция в дисперсных системах
Коагуляция в дисперсных системах Презентация на тему Полимеры и их получение
Презентация на тему Полимеры и их получение  Общие физические и химические свойства металлов. 9 класс
Общие физические и химические свойства металлов. 9 класс Основы химической термодинамики и термохимии. Лекция 3
Основы химической термодинамики и термохимии. Лекция 3 Коллоидные растворы
Коллоидные растворы Основи масообміну
Основи масообміну Презентация на тему Электролиз: что полезно знать
Презентация на тему Электролиз: что полезно знать  Комплексное изучение системы NiO-ZnO-CoO с целью модифицирования свойств исходной матрицы никель-цинкового феррита xZnxFe2O4
Комплексное изучение системы NiO-ZnO-CoO с целью модифицирования свойств исходной матрицы никель-цинкового феррита xZnxFe2O4 Химические свойства щелочей (тема 6)
Химические свойства щелочей (тема 6) Химическая связь
Химическая связь Хром. Элемент vi группы
Хром. Элемент vi группы Периодический закон и периодическая система химических элементов Д. И. Менделеева. Строение атома
Периодический закон и периодическая система химических элементов Д. И. Менделеева. Строение атома Азотсодержащие органические соединения
Азотсодержащие органические соединения Химические свойства кислорода. Применение кислорода
Химические свойства кислорода. Применение кислорода Карбоновые кислоты
Карбоновые кислоты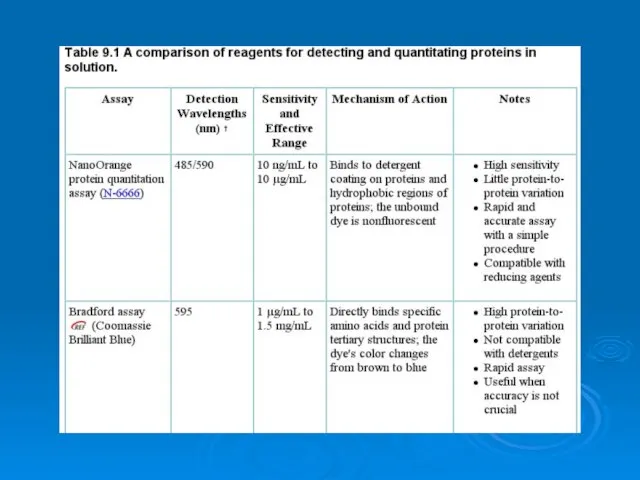 Analysis of proteins
Analysis of proteins Презентация на тему Подгруппа углерода
Презентация на тему Подгруппа углерода  Насыщенные жирные кислоты
Насыщенные жирные кислоты Блок колонн на установке замедленного коксования производительностью 730000 тонн/год гудрона (поз.к-1, кх-1)
Блок колонн на установке замедленного коксования производительностью 730000 тонн/год гудрона (поз.к-1, кх-1) Вдоль по радуге
Вдоль по радуге Презентация на тему Природные источники углеводородов
Презентация на тему Природные источники углеводородов  кремний и его соединения
кремний и его соединения