Содержание
- 2. Цель урока: Задачи урока: Расширить и углубить знания об этиленовых углеводородах. показать различия между классами алканов
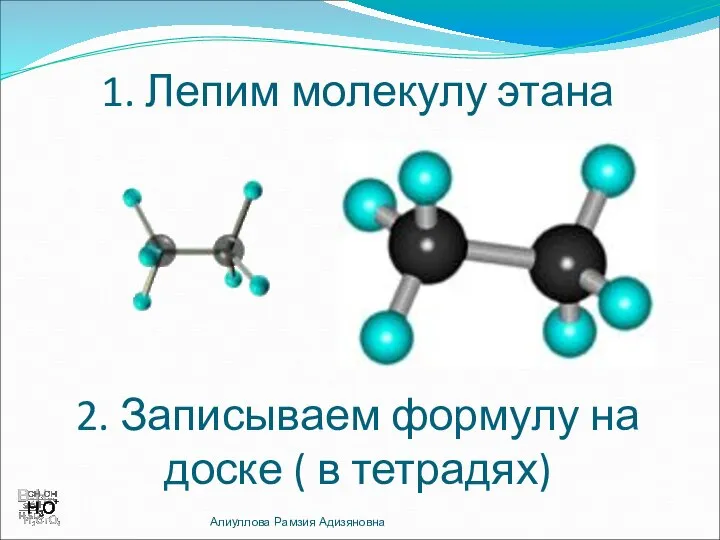
- 3. 1. Лепим молекулу этана 2. Записываем формулу на доске ( в тетрадях) Алиуллова Рамзия Адизяновна
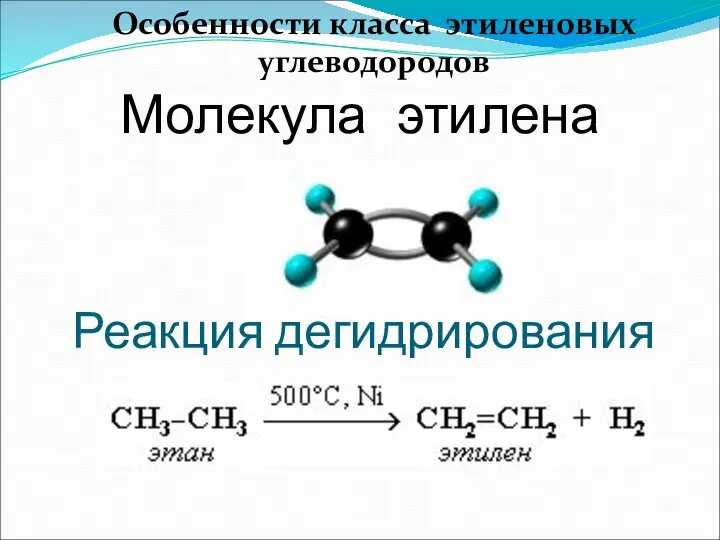
- 4. Молекула этилена Реакция дегидрирования Особенности класса этиленовых углеводородов
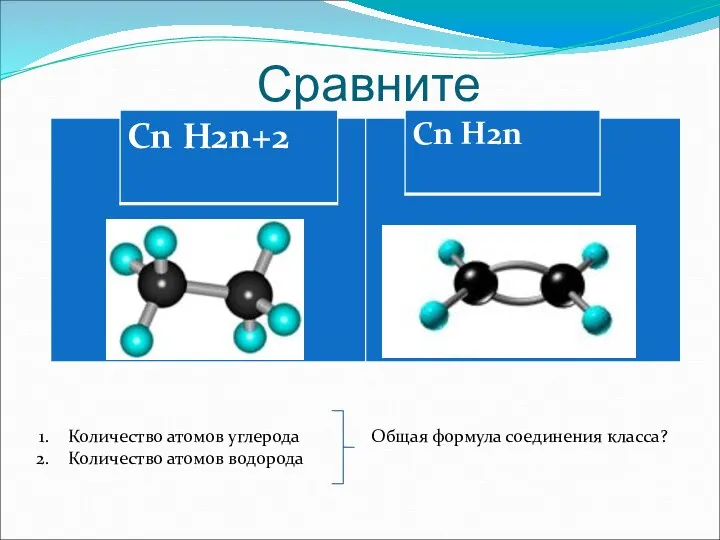
- 5. Сравните Количество атомов углерода Общая формула соединения класса? Количество атомов водорода
- 6. Алкены (этиленовые углеводороды) - непредельные углеводороды, содержащие в молекуле , кроме одинарных связей, одну двойную углерод
- 7. Задание на закрепление общей формулы: Какие из приведенных углеводородов относятся к алкенам? C4H8, C8H18, C6H6, C3H6,
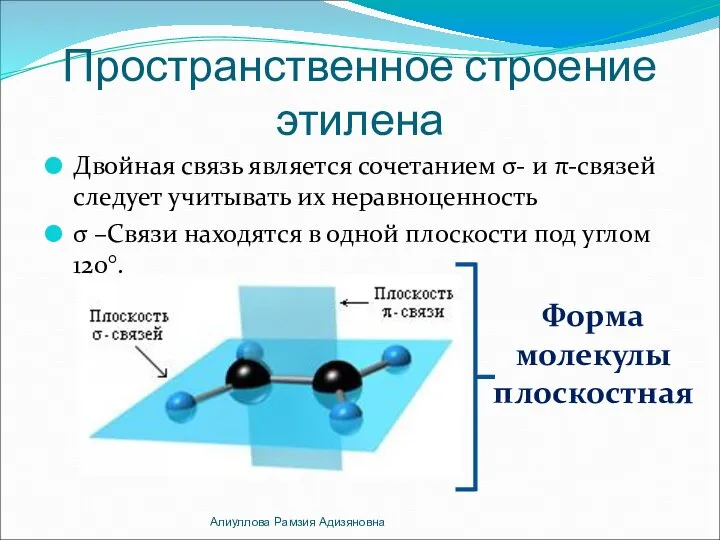
- 8. Пространственное строение этилена Двойная связь является сочетанием σ- и π-связей следует учитывать их неравноценность σ –Связи
- 9. Номенклатура алкенов По систематической номенклатуре названия алкенов производят от названий соответствующих алканов (с тем же числом
- 10. Назовите вещества
- 11. Структурная изомерия алкенов 1. Изомерия углеродного скелета (начиная с С4Н8): 2. Изомерия положения двойной связи (начиная
- 12. Замените на модели молекулы этилена два атома водорода на два атомы хлора у каждого атома углерода
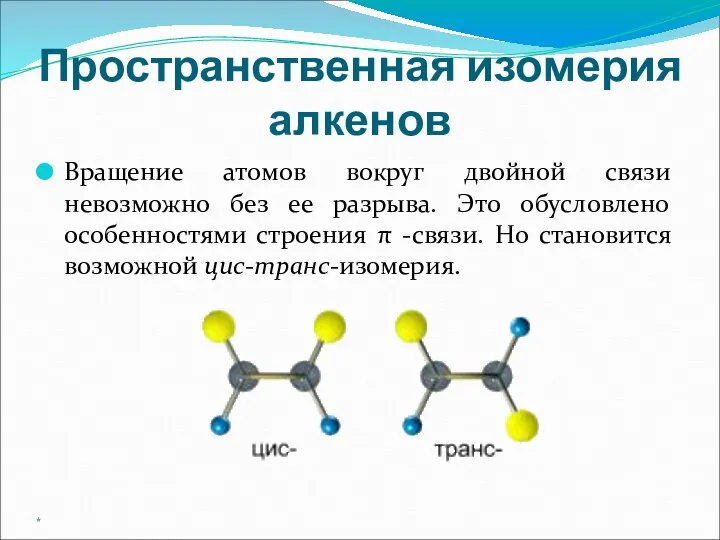
- 13. Пространственная изомерия алкенов Вращение атомов вокруг двойной связи невозможно без ее разрыва. Это обусловлено особенностями строения
- 14. Физические свойства алкенов Закономерно изменяются в гомологическом ряду: от С2Н4 до С4Н8 – газы, с С5Н10
- 15. Физкультминутка Красноперова Оксана Викторовна *
- 16. Химические свойства алкенов Определяются строением и свойствами двойной связи С=С. 1. Реакция присоединения
- 17. Правило Марковникова Русский химик-органик. В реакциях присоединения полярных молекул к несимметричным алкенам водород присоединяется к более
- 18. 2. Реакция полимеризации
- 19. Реакция окисления Мягкое окисление алкенов водным раствором перманганата калия приводит к образованию двухатомных спиртов (реакция Вагнера):
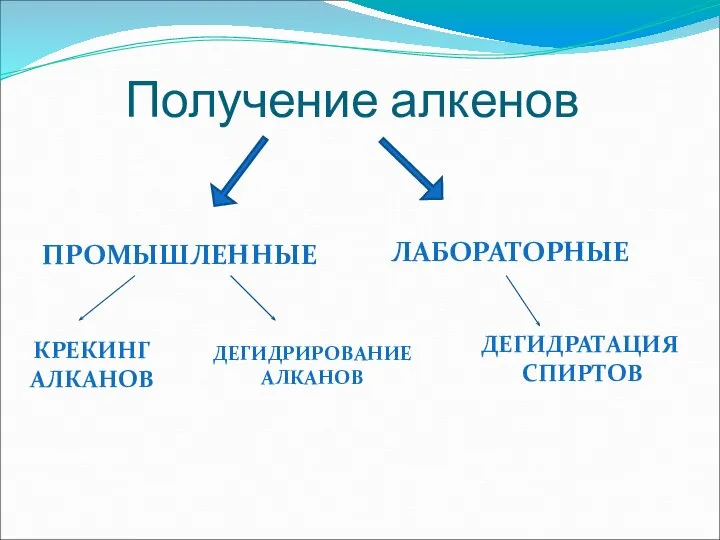
- 20. Получение алкенов ПРОМЫШЛЕННЫЕ ЛАБОРАТОРНЫЕ КРЕКИНГ АЛКАНОВ ДЕГИДРИРОВАНИЕ АЛКАНОВ ДЕГИДРАТАЦИЯ СПИРТОВ
- 22. Скачать презентацию













 Спирты. Тест
Спирты. Тест Металлы. Общие свойства
Металлы. Общие свойства Презентация на тему Химические свойства алкенов
Презентация на тему Химические свойства алкенов  Презентация на тему Алкадиены: строение, номенклатура, гомологи, изомерия
Презентация на тему Алкадиены: строение, номенклатура, гомологи, изомерия  Химия цвета
Химия цвета Зола. Свойства щёлока
Зола. Свойства щёлока Вещества в окружающей природе и в технике
Вещества в окружающей природе и в технике Относительная атомная масса элементов
Относительная атомная масса элементов Известняк. Разновидности известняка. Области применения
Известняк. Разновидности известняка. Области применения Полимерные материалы
Полимерные материалы Аммиак. Состав вещества
Аммиак. Состав вещества Подгруппа алюминия
Подгруппа алюминия Углеводороды
Углеводороды Опыты по теме Свойства основных классов неорганических соединений
Опыты по теме Свойства основных классов неорганических соединений Атомы, молекулы и ионы
Атомы, молекулы и ионы Алмазы
Алмазы Альдегиды, их химические и физические свойства. Получение и применение альдегидов
Альдегиды, их химические и физические свойства. Получение и применение альдегидов Описание молекул
Описание молекул Химия и повседневная жизнь человека
Химия и повседневная жизнь человека Химическое равновесие в гомогенных системах
Химическое равновесие в гомогенных системах Щелочные металлы
Щелочные металлы Составление ионных уравнений
Составление ионных уравнений Строение атома. Связь основных характеристик атома с его положением в таблице Д.И. Менделеева. Способы изображения строения
Строение атома. Связь основных характеристик атома с его положением в таблице Д.И. Менделеева. Способы изображения строения teoriya_elektroliticheskoy_dissotsiatsii
teoriya_elektroliticheskoy_dissotsiatsii Семь доисторических металлов
Семь доисторических металлов Презентация на тему Применение спиртов
Презентация на тему Применение спиртов  Белки. Структуры белков
Белки. Структуры белков Обобщающий урок по теме «Соединения химических элементов» 8 класс.
Обобщающий урок по теме «Соединения химических элементов» 8 класс.