Содержание
- 2. Розчинність речовин. Двадцять друге вересня Класна робота
- 3. І. Розчинність речовин. 1. Розчинність – це фізична величина, що показує, яку масу певної речовини можна
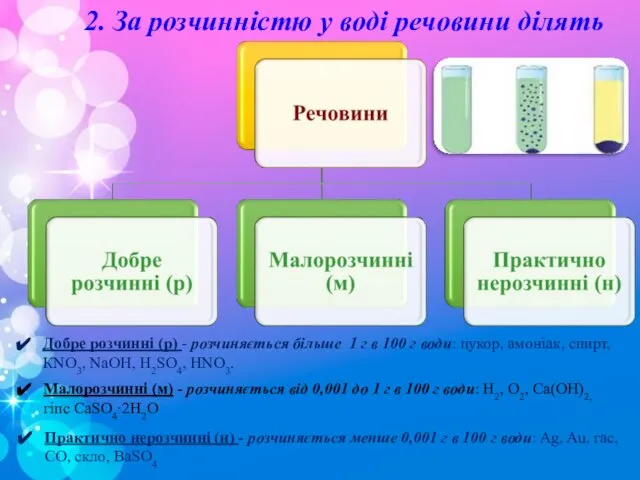
- 4. 2. За розчинністю у воді речовини ділять Добре розчинні (р) - розчиняється більше 1 г в
- 5. Речовини необмежено розчинні у воді Добре розчинні, їх розчинність перевищує 10 грам на 100 грам розчинника
- 6. Розчинні – розчинність від 1 до 10 грам речовини на 100 грам розчинника Малорозчинні - розчинність
- 7. 3. Природа розчинника і розчиненої речовини «Подібне розчиняється в подібному!» Цукор Олія Олія Н2О Н2О Бензин
- 8. 4. Чинники, що впливають на розчинність речовин:
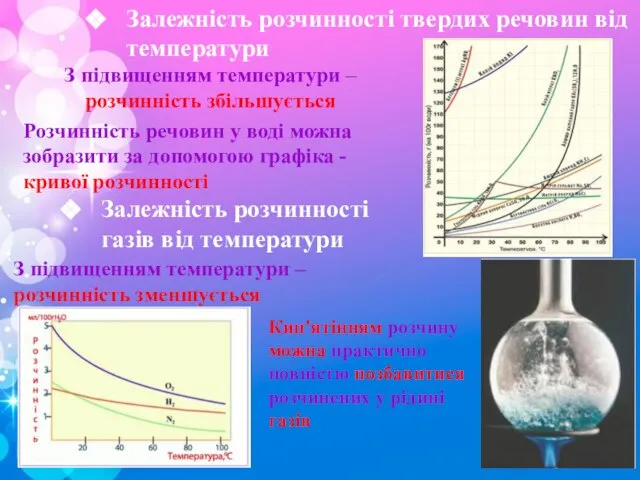
- 9. Залежність розчинності твердих речовин від температури З підвищенням температури –розчинність збільшується Розчинність речовин у воді можна
- 10. Залежність розчинності газів від тиску Розчинність газу прямо пропорційна тиску, чим вищий тиск, тим більша розчинність.
- 11. 5. За вмістом розчиненої речовини розчини поділяються
- 12. Насичений розчин, у якому розчинена речовина більше не розчиняється за даної температури. Ненасичений розчин, у якому
- 13. - Як можна з насиченого розчину зробити ненасичений? Не обов’язково, щоб насичений розчин був концентрованим, а
- 15. Скачать презентацию










 alkany
alkany Титриметрический анализ
Титриметрический анализ Циклоалканы
Циклоалканы Классификация неорганических веществ
Классификация неорганических веществ Химическая связь
Химическая связь Презентация на тему Железо и его соединения (9 класс)
Презентация на тему Железо и его соединения (9 класс)  Галогены и их соединения
Галогены и их соединения Атом. Ядро и электронная оболочка. Изотопы. Строение электронных оболочек атома. Понятие об орбиталях
Атом. Ядро и электронная оболочка. Изотопы. Строение электронных оболочек атома. Понятие об орбиталях Генетические ряды неорганических веществ
Генетические ряды неорганических веществ Закон сохранения массы веществ. Типы химических реакций
Закон сохранения массы веществ. Типы химических реакций Теория электролитической диссоциации
Теория электролитической диссоциации Электролиз
Электролиз Азотная кислота
Азотная кислота Ковалентная неполярная связь
Ковалентная неполярная связь Выполнил ученик 9-го класса Сенов Виктор 2007-2008уч.год
Выполнил ученик 9-го класса Сенов Виктор 2007-2008уч.год Положение металлов в периодической системе Д.И. Менделеева и особенности строения их атомов
Положение металлов в периодической системе Д.И. Менделеева и особенности строения их атомов Карбоновые кислоты
Карбоновые кислоты Лакокрасочные материалы
Лакокрасочные материалы Химия. Спирты
Химия. Спирты Ogļūdeņražu karboksilatvasinājumi
Ogļūdeņražu karboksilatvasinājumi Химия в моей специальности
Химия в моей специальности Производство серной кислоты
Производство серной кислоты Очистка поваренной соли методом кристаллизации в домашних условиях
Очистка поваренной соли методом кристаллизации в домашних условиях Химическая термодинамика
Химическая термодинамика Презентация по Химии "Алмаз"
Презентация по Химии "Алмаз"  Классы неорганических соединений
Классы неорганических соединений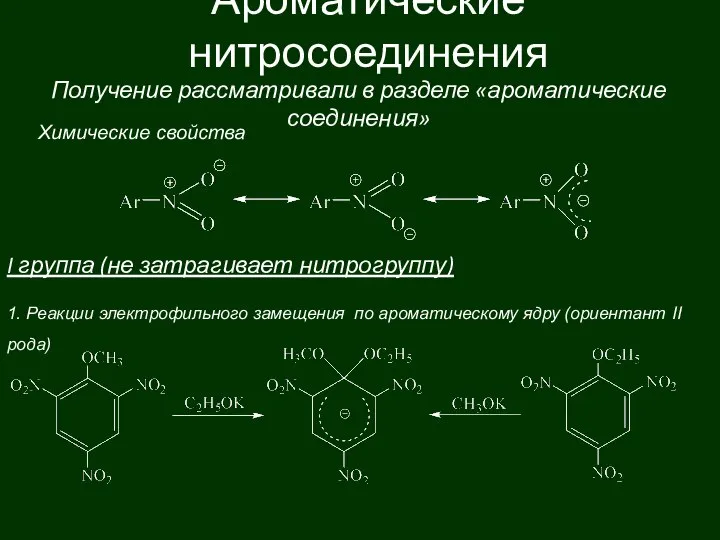 Ароматические нитросоединения
Ароматические нитросоединения Полимеры. Пластмассы
Полимеры. Пластмассы