Содержание
- 2. МАГНИЙ и КАЛЬЦИЙ Са Mg
- 3. Цель урока Сформировать у учащихся основные представления о магний и кальций, как о химических элементах и
- 4. Кальций открыт В 1808 году английским ученым Г . Деви и назван кальцием от латинского слова
- 5. ПРИРОДНЫЕ СОЕДИНЕНИЯ. ПО распространенности в земной коре занимает 5 место и встречается только в виде соединений:
- 6. КАЛЬЦИЙ в природе. Кальций - важнейший строительный материал природы. Из его соединений образованы пещеры с колоннам
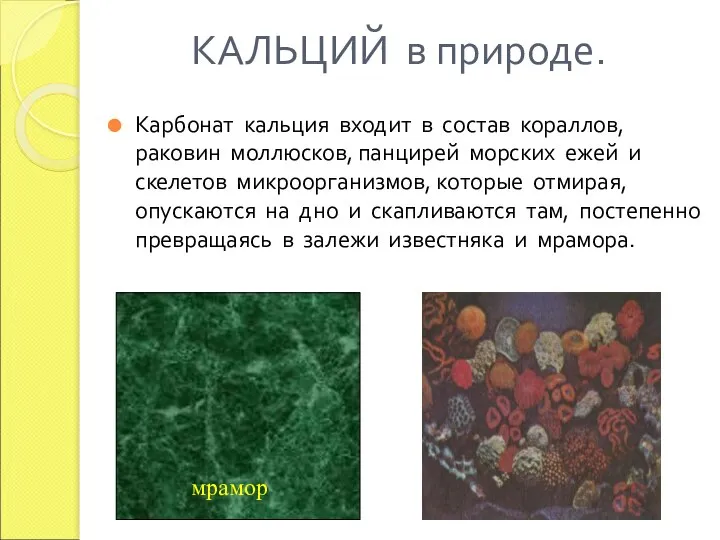
- 7. КАЛЬЦИЙ в природе. Карбонат кальция входит в состав кораллов, раковин моллюсков, панцирей морских ежей и скелетов
- 8. В солончаках и соленых озерах часто накапливается гипс Ca SO4*2H2O
- 9. Реки приносят в океан много кальция (0,04%), который концентрируется в скелетах организмов.
- 10. Он присутствует во всех тканях и жидкостях живых организмов.
- 11. Залежи кальция - в соляных наплывах
- 12. Содержание кальция в организме человека достигает 2 %.
- 13. Бетон – важнейший строительный материал наших дней, одной из составных частей которого является кальций.
- 14. Физические свойства. Кальций-металл серебристо-белого цвета, очень легкий, довольно твердый t0пл8510С. Летучие соли кальция окрашивают пламя в
- 15. Химические свойства Кальций в результате реакции отдает 2 электрона, т.е. окисляется: Ca2+ – 2е → Caо
- 16. Трудно вступают в реакцию с азотом и фосфором: ЗСа + N2 = Са3N2 (нитрид магния) ЗСа
- 18. Скачать презентацию













 Презентация на тему Обобщение знание и умений и предельных и непредельных углеводородах
Презентация на тему Обобщение знание и умений и предельных и непредельных углеводородах  Vvedenie_v_khimiyu
Vvedenie_v_khimiyu Цезій
Цезій Повторение по химии (8 класс)
Повторение по химии (8 класс) Презентация на тему Занимательная химия
Презентация на тему Занимательная химия  Щелочные металлы
Щелочные металлы Строение вещества
Строение вещества Химия крови. Состав и функции крови
Химия крови. Состав и функции крови Строение вещества
Строение вещества Этанол. Химические свойства этанола
Этанол. Химические свойства этанола Кислород
Кислород Закон постоянства состава веществ. Химические формулы. (8 класс)
Закон постоянства состава веществ. Химические формулы. (8 класс) Коррозия металлов. Способы защиты от коррозии
Коррозия металлов. Способы защиты от коррозии Повторение пройденного
Повторение пройденного Пластмассы
Пластмассы Кислоты. Что нас объединяет?
Кислоты. Что нас объединяет? Физико-химия поверхностных явлений в функционировании живых систем
Физико-химия поверхностных явлений в функционировании живых систем Какую воду мы пьем
Какую воду мы пьем Строение молекул. Метод валентных связей. Лекция 5
Строение молекул. Метод валентных связей. Лекция 5 Лекарственные средства – производные пиримидина
Лекарственные средства – производные пиримидина Презентация на тему Моющие средства
Презентация на тему Моющие средства  Углеводороды. Урок-игра
Углеводороды. Урок-игра Кислоты, их классификация и свойства
Кислоты, их классификация и свойства Практическая работа. Решение экспериментальных задач по неорганической химии с использованием виртуальной лаборатории
Практическая работа. Решение экспериментальных задач по неорганической химии с использованием виртуальной лаборатории Переваривание и всасывание липидов. Транспортные формы липидов в крови. Лекция № 7
Переваривание и всасывание липидов. Транспортные формы липидов в крови. Лекция № 7 Как меняется термическая устойчивость и реакционная способность связей Э-C и Э-O-Э в ряду Э=Si, Ge, Sn, Pb
Как меняется термическая устойчивость и реакционная способность связей Э-C и Э-O-Э в ряду Э=Si, Ge, Sn, Pb Обобщение металлов
Обобщение металлов Ð_еÑ_еÑ_огенное Ñ_авн (1)
Ð_еÑ_еÑ_огенное Ñ_авн (1)