Содержание
- 2. Химические названия С формальной точки зрения вода имеет несколько различных корректных химических названий: Оксид водорода: бинарное
- 3. Агрегатные состояния: «Твёрдое» — лёд «Жидкое» — вода «Газообразное» — водяной пар При нормальном атмосферном давлении
- 4. Изотопные модификации воды И кислород, и водород имеют природные и искусственные изотопы. В зависимости от типа
- 5. Химические свойства Вода является наиболее распространённым растворителем на планете Земля. Большая часть химии, при её зарождении
- 6. Вода в природе В атмосфере нашей планеты вода находится в виде капель малого размера, в облаках
- 7. Вода за пределами Земли Вода — чрезвычайно распространённое вещество в космосе, однако из-за высокого внутрижидкостного давления
- 8. Биологическая роль воды Вода играет уникальную роль как вещество, определяющее возможность существования и саму жизнь всех
- 9. Питьё и приготовление пищи Живое человеческое тело содержит от 50 % до 75 % воды, в
- 10. Всемирный день водных ресурсов отмечается ежегодно 23 марта. Этот Всемирный день объявлен Генеральной Ассамблеей ООН в
- 11. Novec 1230 (Фторкетон ФК-5-1-12) — жидкость без цвета и запаха, иногда называемая «сухой водой». Химическая формула
- 12. КИСЛОРОД ФТОР УГЛЕРОД
- 13. Свойства Визуально похоже на чистую воду, но является диэлектриком (не проводит электрический ток), слабо смачивает и
- 15. Скачать презентацию
Слайд 2Химические названия
С формальной точки зрения вода имеет несколько различных корректных химических названий:
Оксид
Химические названия
С формальной точки зрения вода имеет несколько различных корректных химических названий:
Оксид

Монооксид дигидрогена
Гидроксид водорода: соединение гидроксильной группы OH- и катиона (H+)
Гидроксильная кислота: воду можно рассматривать как соединение катиона H+, который может быть замещён металлом, и «кислотного остатка» OH-
Оксидан
Дигидромонооксид
Слайд 3Агрегатные состояния:
«Твёрдое» — лёд
«Жидкое» — вода
«Газообразное» — водяной пар
При нормальном атмосферном
Агрегатные состояния:
«Твёрдое» — лёд
«Жидкое» — вода
«Газообразное» — водяной пар
При нормальном атмосферном

При снижении давления температура таяния (плавления) льда медленно растёт, а температура кипения воды — падает. При давлении в 611,73 Па (около 0,006 атм) температура кипения и плавления совпадает и становится равной 0,01 °C. Такие давление и температура называются тройной точкой воды. При более низком давлении вода не может находиться в жидком состоянии, и лёд превращается непосредственно в пар.
Слайд 4Изотопные модификации воды
И кислород, и водород имеют природные и искусственные изотопы. В
Изотопные модификации воды
И кислород, и водород имеют природные и искусственные изотопы. В

Лёгкая вода (основная составляющая привычной людям воды) . H2O
Тяжёлая вода (дейтериевая) . D2O
Сверхтяжёлая вода (тритиевая) . T2O
тритий-дейтериевая вода
тритий-протиевая вода
дейтерий-протиевая вода
Последние три вида возможны, так как молекула воды содержит два атома водорода. Протий — самый легкий изотоп водорода, дейтерий имеет атомную массу 2,0141017778 а.е.м., тритий — самый тяжелый, атомная масса 3,0160492777 а.е.м. В воде из-под крана тяжелокислородной воды (H2O17 и H2O18) содержится больше, чем воды D2O16: их содержание, соответственно, 1,8 кг и 0,15 кг на тонну[11].
Хотя тяжёлая вода часто считается мёртвой водой, так как живые организмы в ней жить не могут, некоторые микроорганизмы могут быть приучены к существованию в ней.
По стабильным изотопам кислорода 16O, 17O и 18O существуют три разновидности молекул воды. Таким образом, по изотопному составу существуют 18 различных молекул воды. В действительности любая вода содержит все разновидности молекул.
Слайд 5Химические свойства
Вода является наиболее распространённым растворителем на планете Земля. Большая часть химии,
Химические свойства
Вода является наиболее распространённым растворителем на планете Земля. Большая часть химии,

Вода — химически активное вещество. Сильно полярные молекулы воды сольватируют ионы и молекулы, образуют гидраты и кристаллогидраты.
Слайд 6Вода в природе
В атмосфере нашей планеты вода находится в виде капель малого
Вода в природе
В атмосфере нашей планеты вода находится в виде капель малого

Мировой океан содержит более 97,54 % земной воды, подземные воды — около 0,63 %, ледники — 1,81 %, реки и озера — 0,009 %, материковые соленые воды — 0,007 %, атмосфера — 0,001 %[6].
Слайд 7Вода за пределами Земли
Вода — чрезвычайно распространённое вещество в космосе, однако из-за
Вода за пределами Земли
Вода — чрезвычайно распространённое вещество в космосе, однако из-за

Одним из наиболее важных вопросов, связанных с освоением космоса человеком и возможности возникновения жизни на других планетах, является вопрос о наличии воды за пределами Земли в достаточно большой концентрации. Известно, что некоторые кометы более, чем на 50 % состоят из водяного льда. Не стоит, впрочем, забывать, что не любая водная среда пригодна для жизни.
В результате бомбардировки лунного кратера, проведённой 9 октября 2009 года НАСА с использованием космического аппарата LCROSS, впервые были получены достоверные свидетельства наличия на спутнике Земли водяного льда в больших объёмах.
Вода широко распространена в Солнечной системе. Наличие воды (в основном в виде льда) подтверждено на многих спутниках Юпитера и Сатурна: Энцеладе, Тефии, Европе, Ганимеде и др. Вода присутствует в составе всех комет и многих астероидов. Учёными предполагается, что многие транснептуновые объекты имеют в своём составе воду.
Вода в виде паров содержится в атмосфере Солнца (следы), атмосферах Меркурия (3,4 %), также большие количества воды обнаружены в экзосфере Меркурия)[25], Венеры (0,002 %), Луны, Марса (0,03 %), Юпитера (0,0004 %), Сатурна, Урана (следы) и Нептуна.
Кроме того, вода обнаружена на экзопланетах, например HD 189733 b[34], HD 209458 b[35] и GJ 1214 b[36].
Слайд 8Биологическая роль воды
Вода играет уникальную роль как вещество, определяющее возможность существования и
Биологическая роль воды
Вода играет уникальную роль как вещество, определяющее возможность существования и

Благодаря водородной связи, вода остаётся жидкой в широком диапазоне температур, причём именно в том, который широко представлен на планете Земля в настоящее время.
Поскольку у льда плотность меньше, чем у жидкой воды, вода в водоемах замерзает сверху, а не снизу. Образовавшийся слой льда препятствует дальнейшему промерзанию водоема, это позволяет его обитателям выжить.
Слайд 9Питьё и приготовление пищи
Живое человеческое тело содержит от 50 % до 75
Питьё и приготовление пищи
Живое человеческое тело содержит от 50 % до 75

Питьевая вода представляет собой воду из какого-либо источника, очищенную от микроорганизмов и вредных примесей. Пригодность воды для питья при её обеззараживании перед подачей в водопровод оценивается по количеству кишечных палочек на литр воды, поскольку кишечные палочки распространены и достаточно устойчивы к антибактериальным средствам, и если кишечных палочек будет мало, то будет мало и других микробов. Если кишечных палочек не больше, чем 3 на литр, вода считается пригодной для питья.
Слайд 10Всемирный день водных ресурсов отмечается ежегодно 23 марта.
Этот Всемирный день объявлен
Всемирный день водных ресурсов отмечается ежегодно 23 марта.
Этот Всемирный день объявлен

В резолюции Генеральной Ассамблеи предложено государствам проводить в этот день мероприятия, посвящённые сохранению и освоению водных ресурсов. Генеральная Ассамблея попросила Генерального секретаря ООН сосредоточивать ежегодные соответствующие мероприятия ООН на одной конкретной теме.
В 2003 году Генеральная Ассамблея в своей резолюции № A/RES/58/217 объявила период 2005-2015 гг, начиная с Международного дня водных ресурсов 22 марта 2005 года, Международным десятилетием действий «Вода для жизни».
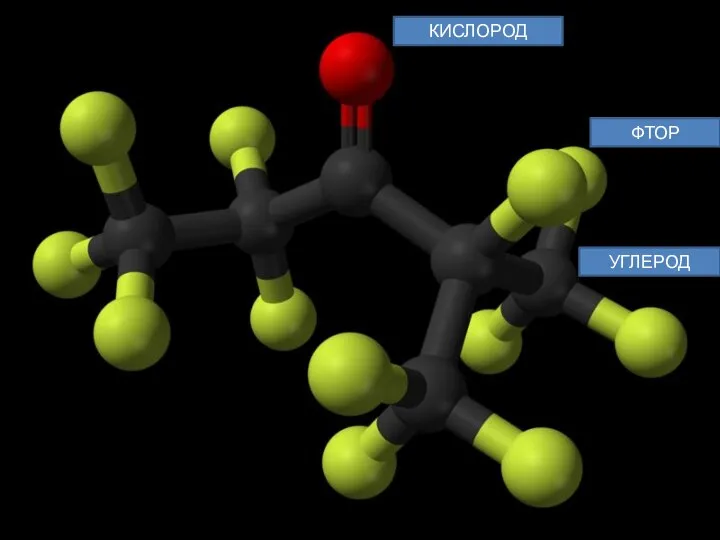
Слайд 11Novec 1230 (Фторкетон ФК-5-1-12) — жидкость без цвета и запаха, иногда называемая
Novec 1230 (Фторкетон ФК-5-1-12) — жидкость без цвета и запаха, иногда называемая

Химическая формула — CF3CF2C(O)CF(CF3)2 (перфтор(этил-изопропилкетон), шестиуглеродное вещество, разряд фторированный кетон (названия кетонов R1—CO—R2 по правилам радикально-функциональной номенклатуры строят, перечисляя названия радикалов R1 и R2 в алфавитном порядке перед словом «кетон»).
Запатентован в качестве хладагента в ходе изысканий по замене хладона 114 (1,1,2,2-тетрафтордихлорэтана), применение которого наряду с другими хлорсодержащими фреонами, было ограничено Монреальским протоколом 1993 года. Впервые продемонстрирован в 2004 году.
Слайд 12КИСЛОРОД
ФТОР
УГЛЕРОД
КИСЛОРОД
ФТОР
УГЛЕРОД
Слайд 13Свойства
Визуально похоже на чистую воду, но является диэлектриком (не проводит электрический ток),
Свойства
Визуально похоже на чистую воду, но является диэлектриком (не проводит электрический ток),

Не влияет на работающую электронику, не разрушает бумажные документы и художественные произведения. Эти свойства обеспечили применимость Novec 1230 в системах пожаротушения для серверных помещений и другой электроники, библиотек, музеев, архивов.
 Химические средства защиты растений
Химические средства защиты растений Степень окисления
Степень окисления Презентация на тему Стронций
Презентация на тему Стронций  углеводы (1)
углеводы (1) Протолитические буферные системы. Буферные системы организма, их взаимодействие
Протолитические буферные системы. Буферные системы организма, их взаимодействие Общая характеристика элементов подгруппы углерода. Углерод – его строение и свойства
Общая характеристика элементов подгруппы углерода. Углерод – его строение и свойства Коферменты. Промышленное получение и применение ферментов
Коферменты. Промышленное получение и применение ферментов Лиофильные и лиофобные дисперсные системы. Свойства лиофильных систем. Лекция 12
Лиофильные и лиофобные дисперсные системы. Свойства лиофильных систем. Лекция 12 Презентация на тему Альдегиды
Презентация на тему Альдегиды  Кислород
Кислород Классификация химических реакций
Классификация химических реакций Dereglarea metabolismului
Dereglarea metabolismului Окислительно-восстановительные реакции. Типы химических реакций
Окислительно-восстановительные реакции. Типы химических реакций Термокаталитические процессы переработки нефтяных фракций
Термокаталитические процессы переработки нефтяных фракций 175 – летию со дня рождения Дмитрия Ивановича Менделеева посвящается… АВТОР ПРЕЗЕНТАЦИИ: учитель химии МОУ СОШ №2 города Ртищево Саратовской области ПОПКОВА Е.Г.
175 – летию со дня рождения Дмитрия Ивановича Менделеева посвящается… АВТОР ПРЕЗЕНТАЦИИ: учитель химии МОУ СОШ №2 города Ртищево Саратовской области ПОПКОВА Е.Г. SHOT.шампуни. Состав. Компоненты
SHOT.шампуни. Состав. Компоненты Презентация на тему Количество вещества. Молярная масса
Презентация на тему Количество вещества. Молярная масса  Органическая химия. Теория строения органических соединений
Органическая химия. Теория строения органических соединений Характеристика кислорода и серы
Характеристика кислорода и серы Reactivi444
Reactivi444 Процессы в растворах: электролитическая диссоциация (ЭД)
Процессы в растворах: электролитическая диссоциация (ЭД) (Bu4N)2[Mo6I8(OOCCH3)6]. Синтез
(Bu4N)2[Mo6I8(OOCCH3)6]. Синтез Общая характеристика элементов главной подгруппы VI группы (подгруппы кислорода)
Общая характеристика элементов главной подгруппы VI группы (подгруппы кислорода) Классификация органических соединений. Предельные углеводороды (УВ)
Классификация органических соединений. Предельные углеводороды (УВ) Расчеты по химическим уравнениям
Расчеты по химическим уравнениям Закон сохранения массы веществ
Закон сохранения массы веществ Молярная масса вещества
Молярная масса вещества Свойства кислорода. Оксиды
Свойства кислорода. Оксиды