Содержание
- 2. Качественные реакции
- 3. Признаки, по которым одно вещество отличается от другого: Внешний вид. Характерный запах. Цвет. Плотность. Растворимость в
- 4. Признаки химических реакций: Изменение цвета. Выделение газа. Выпадение осадка. Растворение осадка. Появление запаха. Характерный звук. Выделение
- 5. Распознавание веществ, не имеющих запаха, невидимых. Как Вы думаете? Как узнать, в каком сосуде находятся кислород
- 6. Качественные реакции – это химические превращения, сопровождающиеся характерными признаками, с помощью которых проводят распознавание веществ. Явления
- 7. РЕАКТИВ. Вещество, с помощью которого проводят качественную реакцию, называется реактивом на определяемое вещество. Известковая вода –
- 8. Аналитический сигнал на определённый реактив должен появляться только при взаимодействии с одним или, по крайней мере
- 9. Определение состава пищевых продуктов проводят с помощью качественных реакций. Наличие кислот – с помощью веществ –
- 10. Реактив на крахмал. Наличие крахмала в продуктах определяют реактивом на крахмал - раствором йода.
- 11. Лабораторный опыт. С помощью йодной настойки из аптечки проведите обнаружение крахмала в картофеле, хлебе, макаронных изделиях.
- 12. Где же применяются качественные реакции? В медицине: при приготовлении лекарств, проведении анализов на содержание различных веществ
- 13. ТИТРИМЕТРИЧЕСКИЙ МЕТОД АНАЛИЗА
- 14. Основные понятия и их суть: Титриметрический метод анализа – метод количественного анализа, основанный на точном измерении
- 15. Основные понятия и их суть: Титрование - медленное прибавление (небольшими порциями) титрованного (стандартного, титранта, рабочего) раствора
- 16. Основные понятия и их суть: Конечная точка титрования (КТТ) - это точка (момент) титрования устанавливаемая экспериментально
- 17. Основные понятия и их суть: Аликвотная доля (аликвота) − точно известная часть анализируемого раствора, взятая для
- 18. Требования к реакции в титриметрии: 1) Вещества, которые вступают в реакцию, должны реагировать в строго определенных
- 19. Способы титрования Метод отдельных навесок взвешивают на аналитических весах точную навеску m(A) стандартного вещества А, переносят
- 20. Метод пипетирования - в мерной колбе готовят раствор стандартного вещества с известной концентрацией (по точной навеске
- 21. Оптические методы анализа
- 22. Оптические методы анализа основаны на способности атомов и молекул вещества испускать, поглощать или рассеивать электромагнитное излучение.
- 23. Оптические методы 1. Молекулярно-абсорбционный спектральный анализ. 2. Атомная спектроскопия. 3. Рефрактометрический анализ. 4. Люминесцентный анализ. 5.
- 24. Основана на измерении поглощения света окрашенными растворами в видимой части спектра. Используют химические реагенты, которые образуют
- 25. Визуальная колориметрия Проводится измерение интенсивности окраски раствора. Сравнение интенсивности окрашивания растворов проводят невооруженным глазом.
- 26. Визуальные колориметрические методы 1. Метод стандартных серий; 2. Метод колориметрического титрования; 3. Метод уравнивания; 4. Метод
- 27. 1. Метод стандартных серий (метод цветной шкалы) Сравнивают интенсивность полученной окраски исследуемого и стандартных растворов. Визуальные
- 28. 2. Метод колориметрического титрования (метод дублирования). По совпадению интенсивности окрасок стандартного и исследуемого растворов определяют содержание
- 29. 3. Метод уравнивания Основан на том, что, изменяя толщину слоя двух растворов с различной концентрацией одного
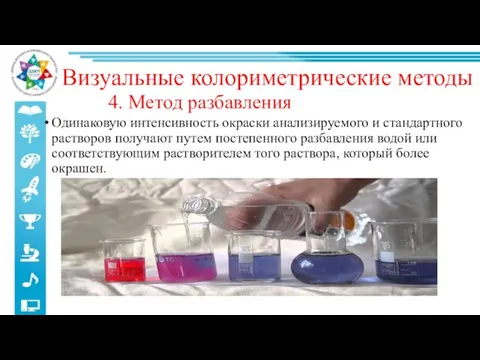
- 30. 4. Метод разбавления Одинаковую интенсивность окраски анализируемого и стандартного растворов получают путем постепенного разбавления водой или
- 32. Скачать презентацию




























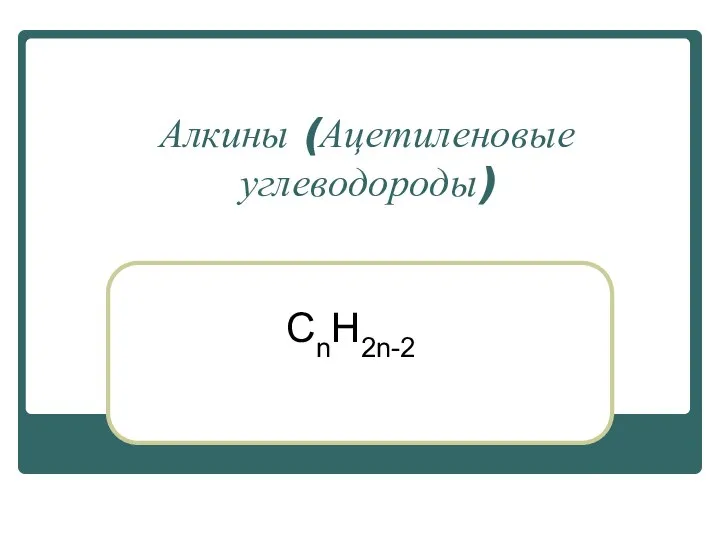 Алкины (Ацетиленовые углеводороды)
Алкины (Ацетиленовые углеводороды) Соли как производные кислот и оснований
Соли как производные кислот и оснований Диссоциация. Уравнения диссоциации
Диссоциация. Уравнения диссоциации Состав и значение воздуха
Состав и значение воздуха Решение задач на нахождение молекулярной формулы газообразного алкана
Решение задач на нахождение молекулярной формулы газообразного алкана Реакционная система. Схема химической реакции. Закон сохранения массы веществ в химической реакции
Реакционная система. Схема химической реакции. Закон сохранения массы веществ в химической реакции Образование раствора
Образование раствора Горные породы
Горные породы Структура и функции нуклеиновых кислот
Структура и функции нуклеиновых кислот Органическая химия. Пищевые добавки
Органическая химия. Пищевые добавки Строение и химические свойства галогенов
Строение и химические свойства галогенов Жиры. Классификация жиров
Жиры. Классификация жиров Хлор. Распространение хлора в природе
Хлор. Распространение хлора в природе Свойства воды
Свойства воды Презентация на тему Глюкоза (10 класс)
Презентация на тему Глюкоза (10 класс)  Инструкция по самостоятельной подготовке к ЕГЭ (ЕРЭ) по химии 2022
Инструкция по самостоятельной подготовке к ЕГЭ (ЕРЭ) по химии 2022 Бер нигезле чикле карбон кислоталары
Бер нигезле чикле карбон кислоталары Составление уравнений окислительно-восстановительных реакций
Составление уравнений окислительно-восстановительных реакций Алкадиены
Алкадиены Аминокислоты. Пептиды. Белки. Тема 2
Аминокислоты. Пептиды. Белки. Тема 2 Презентация по Химии "Строении атомов. Химическая связь"
Презентация по Химии "Строении атомов. Химическая связь"  Периодическая система Д.И.Менделеева
Периодическая система Д.И.Менделеева Электролитическая диссоциация
Электролитическая диссоциация Получение и свойства полиэтилена
Получение и свойства полиэтилена Строение атома
Строение атома Прогнозирование возможности и направления протекания самопроизвольных процессов
Прогнозирование возможности и направления протекания самопроизвольных процессов rastvory_-_kopia
rastvory_-_kopia Технологические процессы получения кислорода
Технологические процессы получения кислорода