Содержание
- 2. Химические свойства спиртов: 1. Горение 2. Взаимодействие с акт.металлами и бромоводородом 3. Дегидратация А) внутримолекулярная Б)
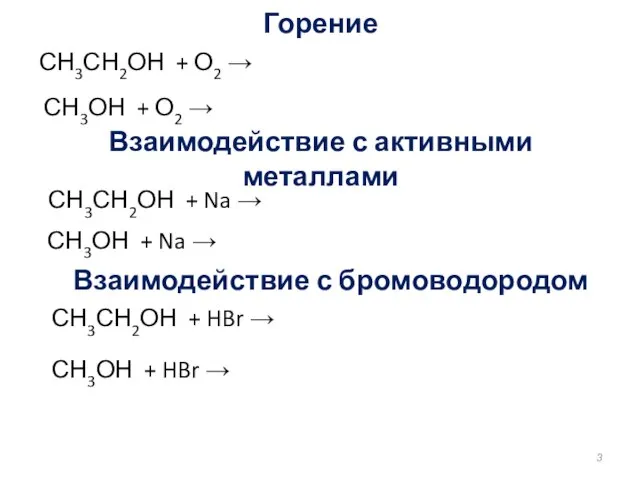
- 3. Горение СН3СН2ОН + О2 → СН3ОН + О2 → Взаимодействие с активными металлами СН3СН2ОН + Na
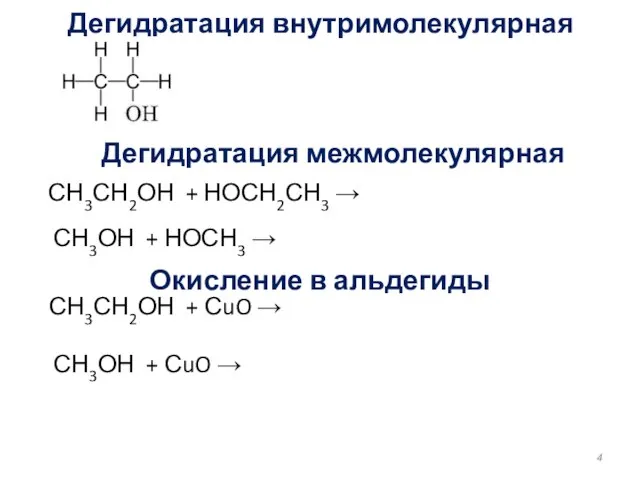
- 4. Дегидратация внутримолекулярная СН3СН2ОН + НОСН2СН3 → Окисление в альдегиды СН3СН2ОН + СuO → СН3ОН + СuO
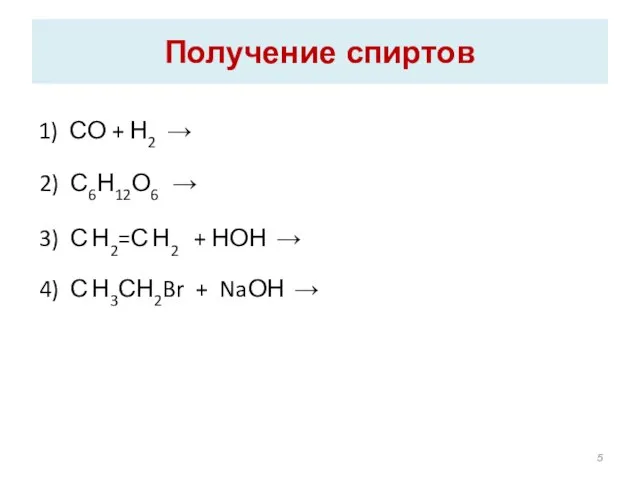
- 5. Получение спиртов 1) СО + Н2 → 2) С6Н12О6 → 3) С Н2=С Н2 + НОН
- 6. Применение спиртов
- 8. Скачать презентацию


 Неделя химии в МБОУ (викторина)
Неделя химии в МБОУ (викторина) Свойства основных липопротеинов (ЛП) плазмы крови
Свойства основных липопротеинов (ЛП) плазмы крови Углеводы
Углеводы Топология кристаллических структур. Топологические типы. Программы и базы данных для анализа топологии. Лекция 9
Топология кристаллических структур. Топологические типы. Программы и базы данных для анализа топологии. Лекция 9 Электролитическая диссоциация. Электролиты и неэлектролиты
Электролитическая диссоциация. Электролиты и неэлектролиты Неметаллы в ПСХЭ
Неметаллы в ПСХЭ Органическая химия. Теория строения органических веществ
Органическая химия. Теория строения органических веществ Строение атома
Строение атома Презентация 1
Презентация 1 Теория активированного комплекса
Теория активированного комплекса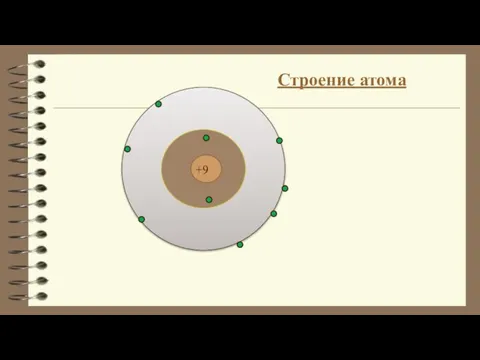 Строение атома
Строение атома Кислоты в химии
Кислоты в химии Природные источники углеводородов
Природные источники углеводородов Природные кислоты и щелочи. Индикаторы
Природные кислоты и щелочи. Индикаторы Закалка и отпуск стали. Ознакомление со структурами серого и белого чугуна. Распознавание руд железа
Закалка и отпуск стали. Ознакомление со структурами серого и белого чугуна. Распознавание руд железа Химическая технология. Структура ВКР
Химическая технология. Структура ВКР Интеллектуальная игра по химии «Металлы»
Интеллектуальная игра по химии «Металлы» Аминокислоты и их применение
Аминокислоты и их применение Углеволокно (карбон)
Углеволокно (карбон) Спирты (алканолы)
Спирты (алканолы) Дисперсные системы в пищевой промышленности
Дисперсные системы в пищевой промышленности Фосфор
Фосфор Пересчет данных анализа, выраженных в ионной форме
Пересчет данных анализа, выраженных в ионной форме Степень окисления. Составление формул бинарных соединений
Степень окисления. Составление формул бинарных соединений Металлы тоже воевали… 8 класс
Металлы тоже воевали… 8 класс Презентация на тему Серебро
Презентация на тему Серебро  Классификация химических реакций
Классификация химических реакций Sinteticheskie_Materialy_I_Ikh_Rol_1
Sinteticheskie_Materialy_I_Ikh_Rol_1