Содержание
- 2. ВОПРОСЫ Какие вещества называются электролитами? . Какие вещества называются неэлектролитами? Что называется ионом? Что называется электролитической
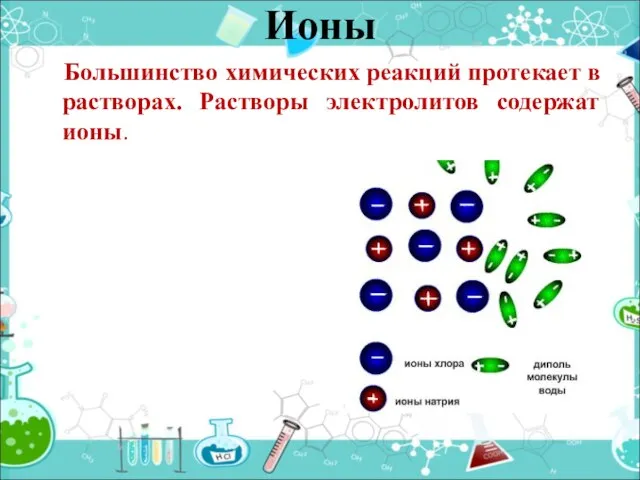
- 3. Большинство химических реакций протекает в растворах. Растворы электролитов содержат ионы. Ионы
- 4. НСl + AgNO3 → AgCl + НNO3
- 5. Реакции ионного обмена записывают тремя уравнениями: молекулярное полное ионно-молекулярное сокращенное ионно-молекулярное .
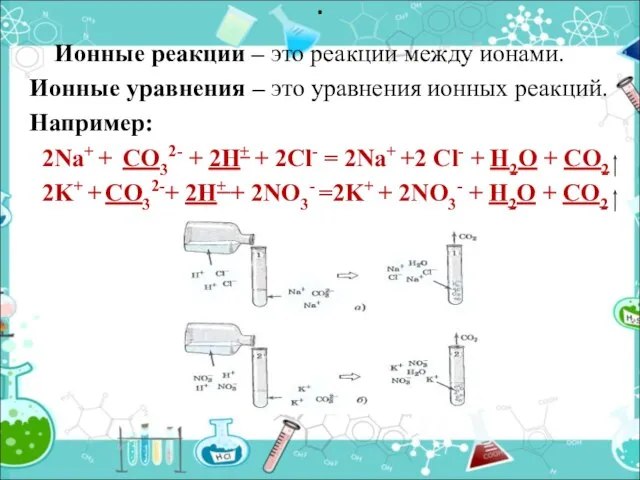
- 6. Ионные реакции – это реакции между ионами. Ионные уравнения – это уравнения ионных реакций. Например: 2Na+
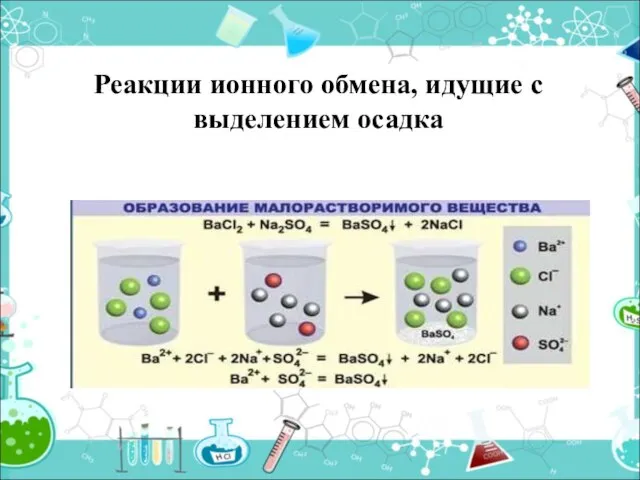
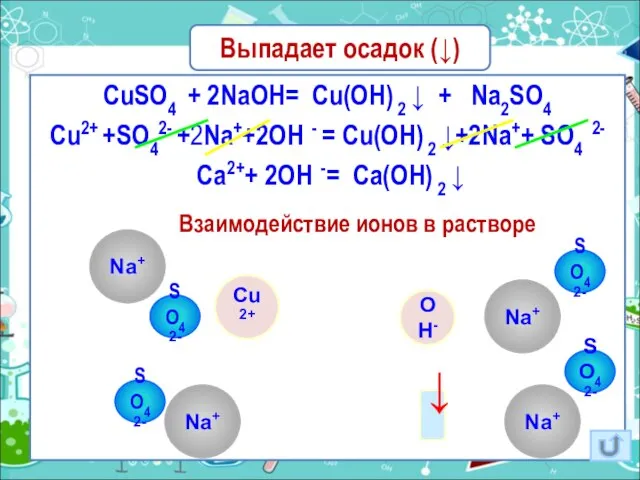
- 7. Реакции ионного обмена, идущие с выделением осадка
- 8. Выпадает осадок (↓) CuSO4 + 2NaOH= Cu(OH) 2 ↓ + Na2SO4 Cu2+ +SO42- +2Na++2OH - =
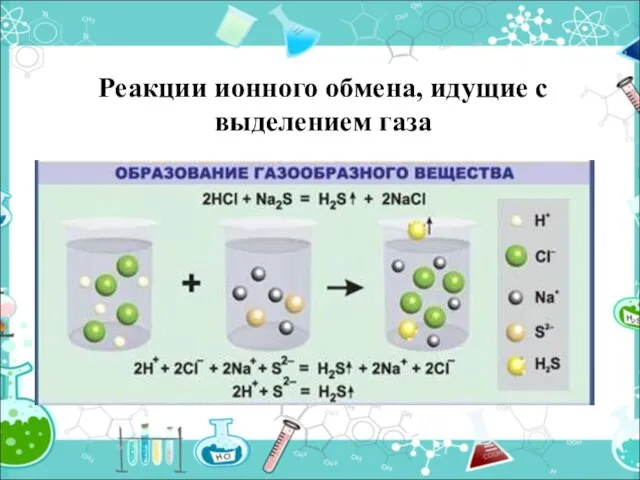
- 9. Реакции ионного обмена, идущие с выделением газа
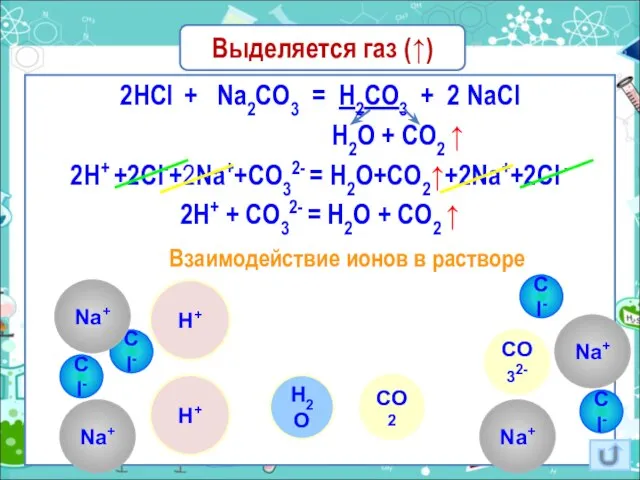
- 10. Выделяется газ (↑) 2HCl + Na2CO3 = H2CO3 + 2 NaCl H2O + CO2 ↑ 2H+
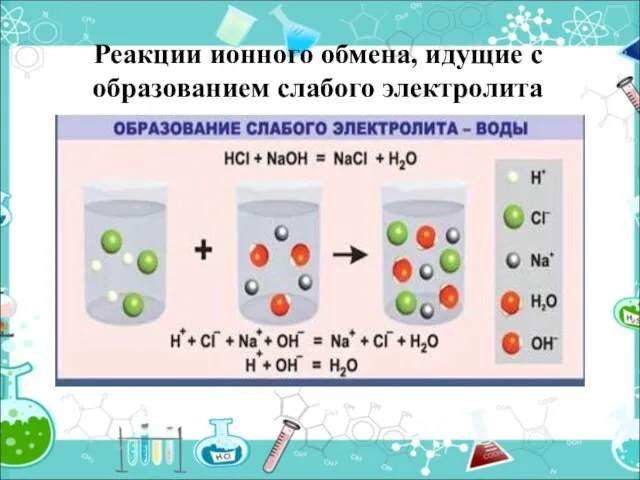
- 11. Реакции ионного обмена, идущие с образованием слабого электролита
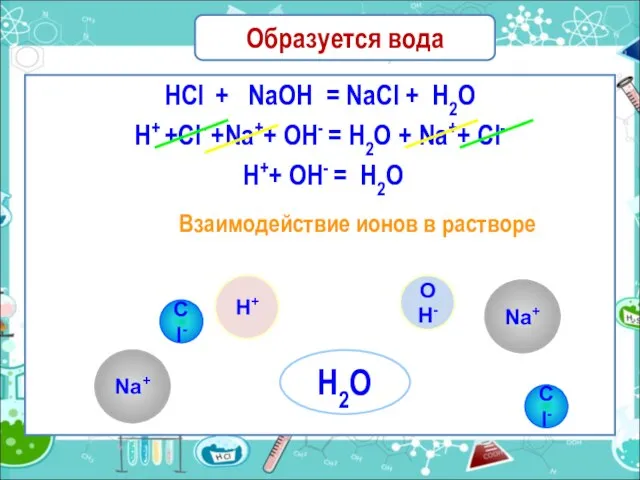
- 12. Образуется вода HCl + NaOH = NaCl + H2O H+ +Cl- +Na++ OH- = H2O +
- 13. Na2SO4 + KI Na+ SO42- K+ I- 1.Нет осадка 2.Не выделяется газ 3.Не образуется слабый электролит
- 14. В соответствии с правилом Бертолле ионные реакции протекают практически необратимо: I случай II случай III случай
- 16. Скачать презентацию




 Аттестационная работа. Музей минералов и горных пород
Аттестационная работа. Музей минералов и горных пород Спирт и его влияние на организм человека
Спирт и его влияние на организм человека Гликоген. Синтез гликогена
Гликоген. Синтез гликогена Презентация на тему Химические свойства металлов
Презентация на тему Химические свойства металлов  Минерал дунит
Минерал дунит Химические реакции в органике
Химические реакции в органике Производство серной кислоты
Производство серной кислоты Периодический закон и периодическая система химических элементов Д.И. Менделеева
Периодический закон и периодическая система химических элементов Д.И. Менделеева Соединения Ca и Mg, представителей элементов II группы главной подгруппы
Соединения Ca и Mg, представителей элементов II группы главной подгруппы Реакции неполного окисления в органике
Реакции неполного окисления в органике Презентация на тему Элементы таблицы Менделеева
Презентация на тему Элементы таблицы Менделеева  Основные классы неорганических соединений
Основные классы неорганических соединений Презентация на тему Жесткость воды
Презентация на тему Жесткость воды  Ковалентная связь. Электроотрицательность
Ковалентная связь. Электроотрицательность Физико-химическая механика и реология дисперсных структур. Лекция 15
Физико-химическая механика и реология дисперсных структур. Лекция 15 Развитие энергетики и проблемы изменения структуры использования углеводородного сырья
Развитие энергетики и проблемы изменения структуры использования углеводородного сырья Строение электронных оболочек атомов элементов
Строение электронных оболочек атомов элементов Явления
Явления Кристаллическое состояние воды - лёд
Кристаллическое состояние воды - лёд Коррозия металлов
Коррозия металлов Презентация на тему Подгруппа азота
Презентация на тему Подгруппа азота  897386 (2)
897386 (2) Разработка методов синтеза гомогенных катализаторов оксосинтеза бутиловых спиртов
Разработка методов синтеза гомогенных катализаторов оксосинтеза бутиловых спиртов Template biosynthesis
Template biosynthesis Молярный объем
Молярный объем 10_kl_klas-ya
10_kl_klas-ya Лекция 26. Химическое (водородное) и электрохимическое аккумулирование энергии
Лекция 26. Химическое (водородное) и электрохимическое аккумулирование энергии Научно-исследовательская деятельность учащихся в процессе изучения химии
Научно-исследовательская деятельность учащихся в процессе изучения химии