Содержание
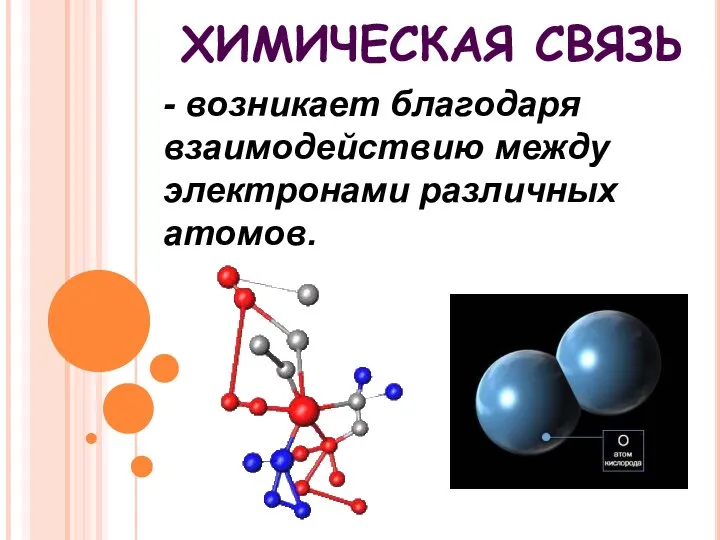
- 2. - возникает благодаря взаимодействию между электронами различных атомов. ХИМИЧЕСКАЯ СВЯЗЬ
- 3. Электроотрицательность. Виды химической связи. Э.О. – свойство атомов данного элемента оттягивать на себя электроны от атомов
- 4. ИЗМЕНЕНИЕ ЭО АТОМОВ ХИМИЧЕСКИХ ЭЛЕМЕНТОВ ПО ПЕРИОДУ ПО ГРУППЕ По периоду слева направо ЭО возрастает. Т.к.
- 5. ВИДЫ ХИМИЧЕСКИХ СВЯЗЕЙ Ионная (И.С.) Металлическая (Ме.С.) Образуется между Ме и неМе Образована атомами Ме Ковалентная
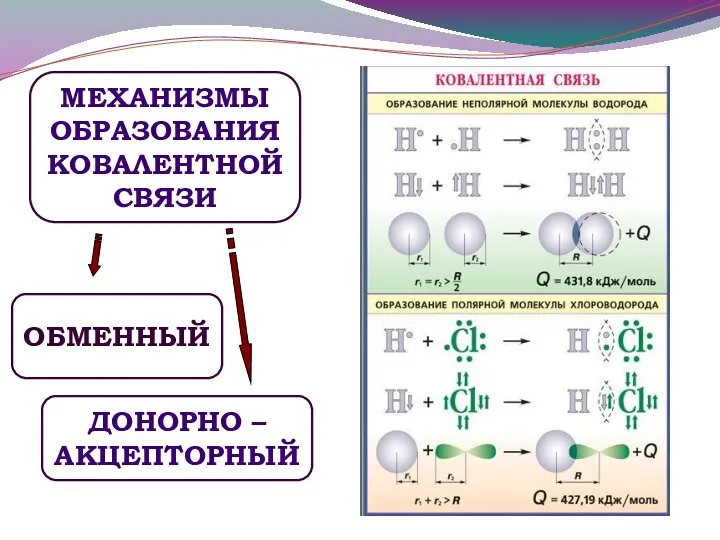
- 6. МЕХАНИЗМЫ ОБРАЗОВАНИЯ КОВАЛЕНТНОЙ СВЯЗИ ОБМЕННЫЙ ДОНОРНО – АКЦЕПТОРНЫЙ
- 7. Образование КНС
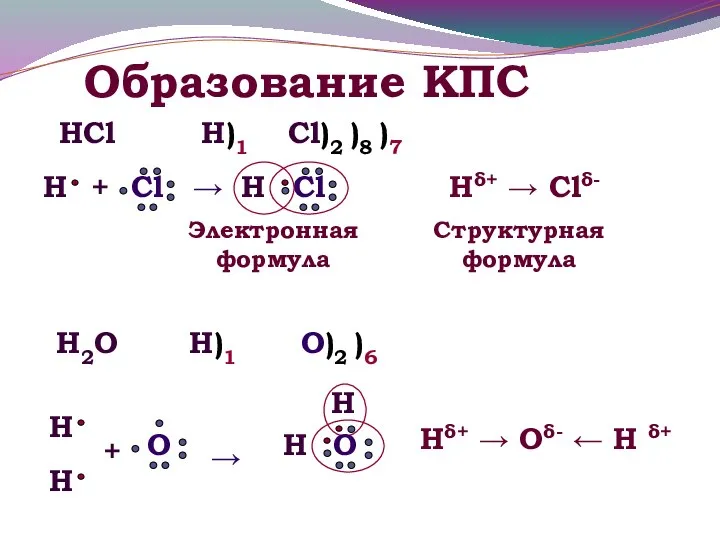
- 8. Образование КПС HCl Н)1 Hδ+ → Clδ- Электронная формула Структурная формула Cl)2 )8 )7 H2O Н)1
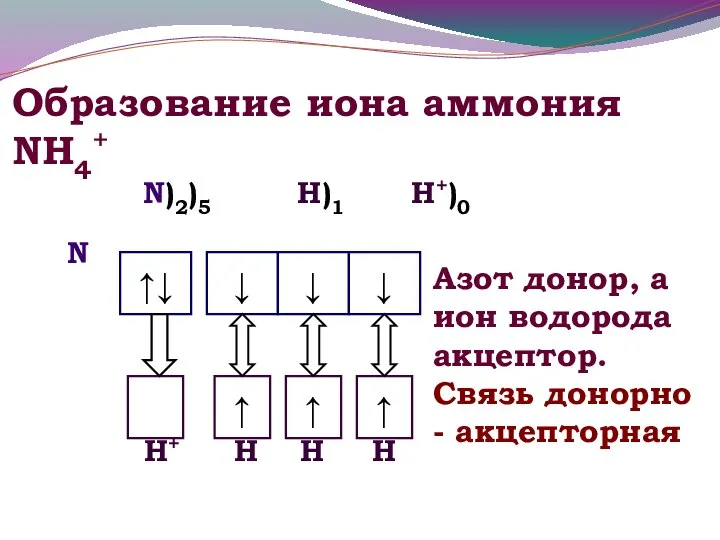
- 9. Образование иона аммония NH4+ Н+ N Н Н Н N)2)5 Н)1 Н+)0 Азот донор, а ион
- 10. Образование ИС NaCl Na )2 )8 )1 Электронная формула Cl)2 )8 )7 Na2O O)2 )6 Na
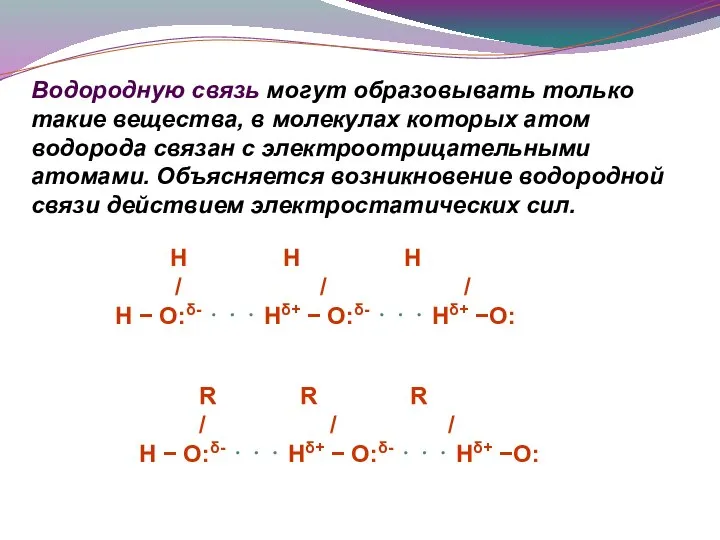
- 11. Водородную связь могут образовывать только такие вещества, в молекулах которых атом водорода связан с электроотрицательными атомами.
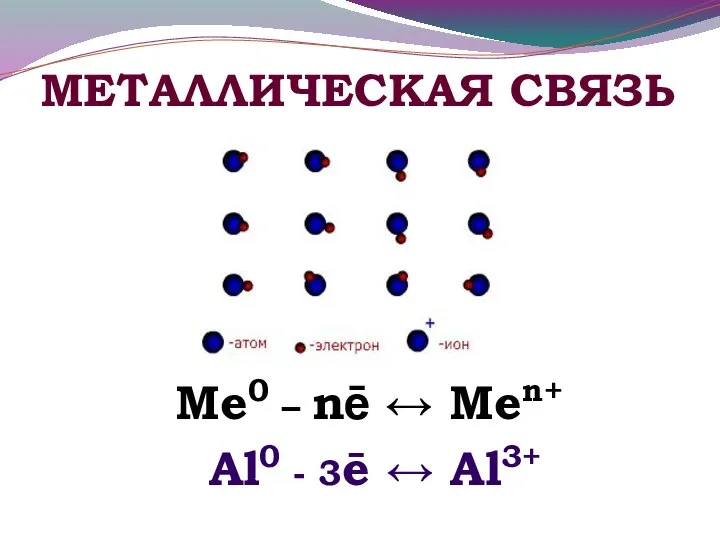
- 12. МЕТАЛЛИЧЕСКАЯ СВЯЗЬ Ме0 – nē ↔ Меn+ Al0 - 3ē ↔ Al3+
- 13. ХАРАКТЕРИСТИКИ ХИМИЧЕСКОЙ СВЯЗИ.
- 14. Важной характеристикой химической связи является ее энергия. Это мера прочности связи. Ее величина определяется выделенной или
- 15. Также важна длина связи - расстояние между центрами ядер атома в молекуле или кристалле. Например: Длина
- 16. Число ковалентных связей, которое способен образовывать некоторый атом в каждом конкретном случае ограничено числом тех валентных
- 17. НАПРАВЛЕННОСТЬ ХИМИЧЕСКИХ СВЯЗЕЙ
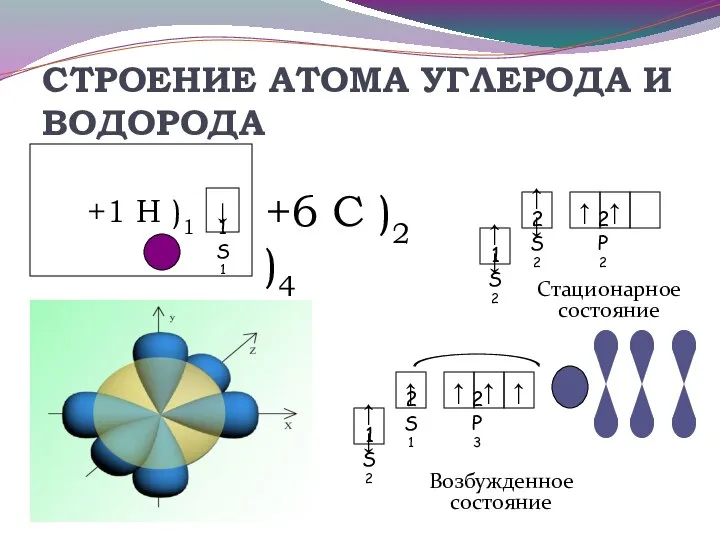
- 18. СТРОЕНИЕ АТОМА УГЛЕРОДА И ВОДОРОДА Возбужденное состояние +6 С )2 )4 Стационарное состояние
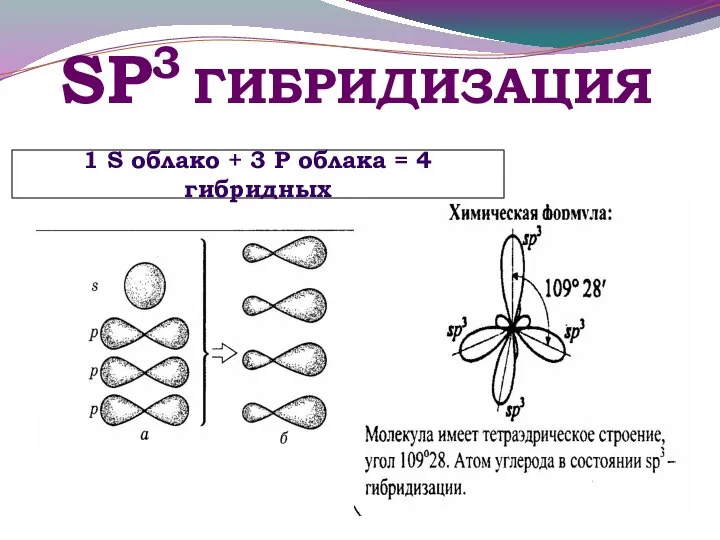
- 19. SР3 ГИБРИДИЗАЦИЯ 1 S облако + 3 Р облака = 4 гибридных
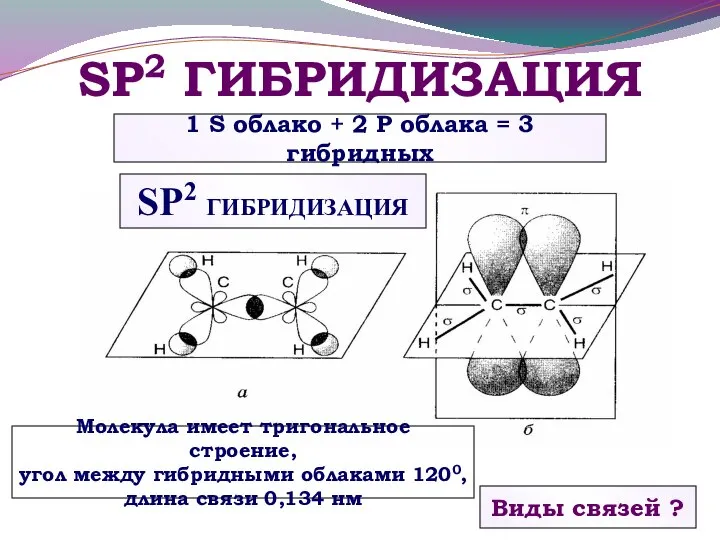
- 20. SP2 ГИБРИДИЗАЦИЯ Виды связей ? Молекула имеет тригональное строение, угол между гибридными облаками 1200, длина связи
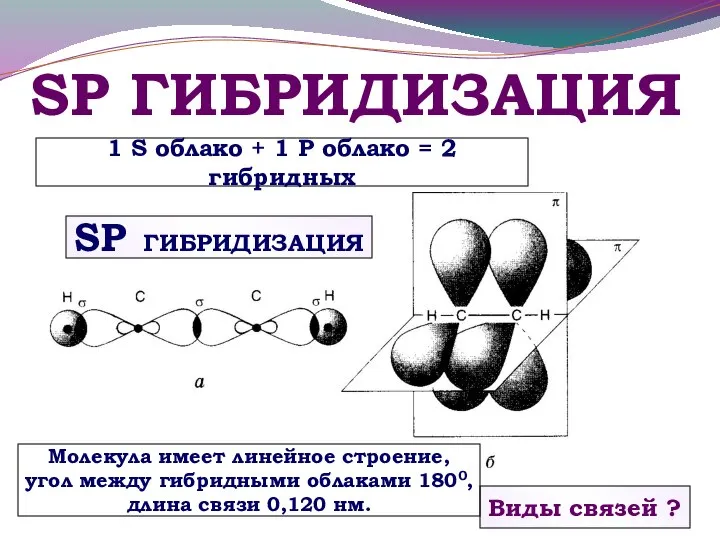
- 21. SP ГИБРИДИЗАЦИЯ Виды связей ? Молекула имеет линейное строение, угол между гибридными облаками 1800, длина связи
- 23. Скачать презентацию









 Эмульсия. Основные типы эмульсий
Эмульсия. Основные типы эмульсий Квантовая химия
Квантовая химия Алкены Бутен
Алкены Бутен Металлы
Металлы Химический диктант по органической химии. 9 класс
Химический диктант по органической химии. 9 класс Химические реакции. Классификация
Химические реакции. Классификация Знакомство с химией
Знакомство с химией Применение каучука
Применение каучука Неорганический мозговой штурм
Неорганический мозговой штурм Практическая работа: Очистка загрязнённой поваренной соли
Практическая работа: Очистка загрязнённой поваренной соли Буферные системы
Буферные системы Cеминар 6 -Алканы-2
Cеминар 6 -Алканы-2 Химические реакции
Химические реакции Электроосмос. Практическое применение электроосмоса
Электроосмос. Практическое применение электроосмоса Магматические горные породы
Магматические горные породы 1_
1_ Физические и химические свойства металлов
Физические и химические свойства металлов Строение электронных оболочек атома
Строение электронных оболочек атома Железо
Железо Производные салициловой, пара-аминобензойной кислот, применяемые в медицине
Производные салициловой, пара-аминобензойной кислот, применяемые в медицине коррозия металлов
коррозия металлов Индикаторная бумага
Индикаторная бумага Тренажер - Валентность. 8 класс
Тренажер - Валентность. 8 класс Потенциометрический анализ, титрование
Потенциометрический анализ, титрование Алкины
Алкины Лучший тест для подготовки к ЕГЭ по химии
Лучший тест для подготовки к ЕГЭ по химии Тривиальные названия веществ, наиболее часто встречаемых в ЕГЭ
Тривиальные названия веществ, наиболее часто встречаемых в ЕГЭ Блок колонн на установке замедленного коксования производительностью 730000 тонн/год гудрона (поз.к-1, кх-1)
Блок колонн на установке замедленного коксования производительностью 730000 тонн/год гудрона (поз.к-1, кх-1)