Содержание
- 2. Известные методы синтеза 5-аминосалициловой кислоты Основным способом получения 5-АСК в настоящее время является восстановление 5-фенилазосалициловой кислоты.
- 3. Квантово-химическое исследование реакции карбоксилирования Квантово-химические расчёты были произведены с использованием програмного комплекса ORCA методом функционала плотности
- 5. Скачать презентацию
Слайд 2Известные методы синтеза 5-аминосалициловой кислоты
Основным способом получения 5-АСК в настоящее время является
Известные методы синтеза 5-аминосалициловой кислоты
Основным способом получения 5-АСК в настоящее время является
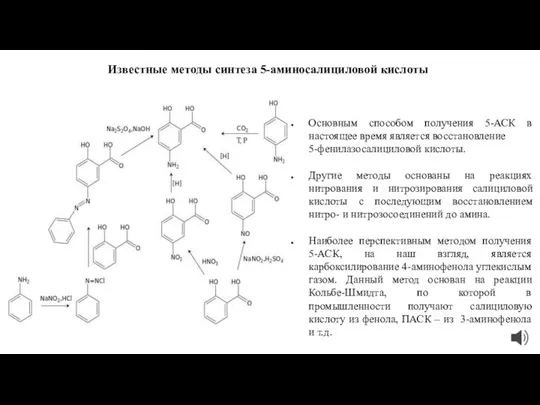
восстановление 5-фенилазосалициловой кислоты.
Другие методы основаны на реакциях нитрования и нитрозирования салициловой кислоты с последующим восстановлением нитро- и нитрозосоединений до амина.
Наиболее перспективным методом получения 5-АСК, на наш взгляд, является карбоксилирование 4-аминофенола углекислым газом. Данный метод основан на реакции Кольбе-Шмидта, по которой в промышленности получают салициловую кислоту из фенола, ПАСК – из 3-аминофенола и т.д.
Другие методы основаны на реакциях нитрования и нитрозирования салициловой кислоты с последующим восстановлением нитро- и нитрозосоединений до амина.
Наиболее перспективным методом получения 5-АСК, на наш взгляд, является карбоксилирование 4-аминофенола углекислым газом. Данный метод основан на реакции Кольбе-Шмидта, по которой в промышленности получают салициловую кислоту из фенола, ПАСК – из 3-аминофенола и т.д.
Слайд 3Квантово-химическое исследование реакции карбоксилирования
Квантово-химические расчёты были произведены с использованием програмного комплекса ORCA
Квантово-химическое исследование реакции карбоксилирования
Квантово-химические расчёты были произведены с использованием програмного комплекса ORCA
методом функционала плотности с гибридным функционалом DFT B3LYP/6-311G**.
Изменения полной электронной энергии в реакции карбоксилирования натриевой соли 4-аминофенола составила -33,84 кДж/моль, а изменение свободной энергии Гиббса -36,04 кДж/моль, в то время как при использовании 4-аминофенола в качестве исходного соединения — 106,6 и 102,6 кДж/моль. Данные значения показывают возможность протекания реакции лишь с солями 4-аминофенола.
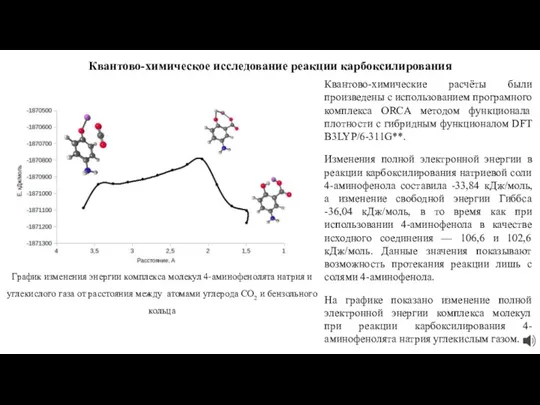
На графике показано изменение полной электронной энергии комплекса молекул при реакции карбоксилирования 4-аминофенолята натрия углекислым газом.
Изменения полной электронной энергии в реакции карбоксилирования натриевой соли 4-аминофенола составила -33,84 кДж/моль, а изменение свободной энергии Гиббса -36,04 кДж/моль, в то время как при использовании 4-аминофенола в качестве исходного соединения — 106,6 и 102,6 кДж/моль. Данные значения показывают возможность протекания реакции лишь с солями 4-аминофенола.
На графике показано изменение полной электронной энергии комплекса молекул при реакции карбоксилирования 4-аминофенолята натрия углекислым газом.
График изменения энергии комплекса молекул 4-аминофенолята натрия и углекислого газа от расстояния между атомами углерода CO2 и бензольного кольца
Следующая -
Паразитарные болезни нервной системы Типы кристаллических решеток
Типы кристаллических решеток Судын оксидтермен реакциясы
Судын оксидтермен реакциясы Ионная химическая связь
Ионная химическая связь Классы неорганических соединений
Классы неорганических соединений Истина - дочь времени, а не авторитета
Истина - дочь времени, а не авторитета Презентация на тему Виды кристаллических решеток
Презентация на тему Виды кристаллических решеток 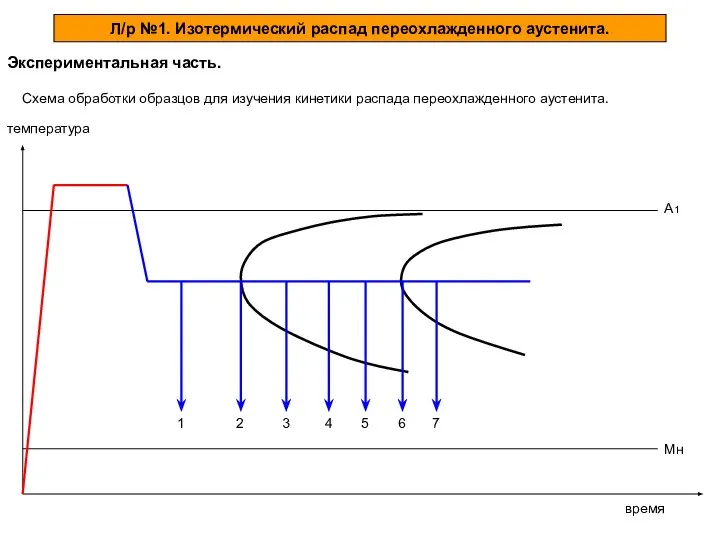 Изотермический распад переохлажденного аустенита. Экспериментальная часть
Изотермический распад переохлажденного аустенита. Экспериментальная часть Содержание варианта ЕГЭ
Содержание варианта ЕГЭ 11_.21
11_.21 Использование комплексно-ориентированных заданий на уроках
Использование комплексно-ориентированных заданий на уроках Окислительно-восстановительные реакции (ОВР)
Окислительно-восстановительные реакции (ОВР) Реакции окисления-восстановления в химическом анализе. (Лекция 7.2)
Реакции окисления-восстановления в химическом анализе. (Лекция 7.2) Алканы
Алканы Химия и автомобиль
Химия и автомобиль Общая характеристика элементов подгруппы углерода. Углерод – его строение и свойства
Общая характеристика элементов подгруппы углерода. Углерод – его строение и свойства Природный каучук
Природный каучук Классификация оксидов
Классификация оксидов Химические реакции
Химические реакции Образование и получение веществ. 6 класс
Образование и получение веществ. 6 класс Металлы
Металлы Закон сохранения массы веществ. Уравнения химических реакций.
Закон сохранения массы веществ. Уравнения химических реакций. Сравнительная характеристика стиральных порошков
Сравнительная характеристика стиральных порошков Валентность. Определение валентности по формулам
Валентность. Определение валентности по формулам Кроссворд. Плотность
Кроссворд. Плотность Алкены
Алкены Коррозия металлов
Коррозия металлов Вещества с атомной кристаллической решеткой
Вещества с атомной кристаллической решеткой Cкорость химических реакций
Cкорость химических реакций