Содержание
- 3. 7. Используя только неорганические вещества и полученные из них органические прекурсоры, предложите способ получения аспирина. Любая
- 4. 8. Определите, какие два вещества вступили в химическую реакцию, если в ее результате получены следующие продукты
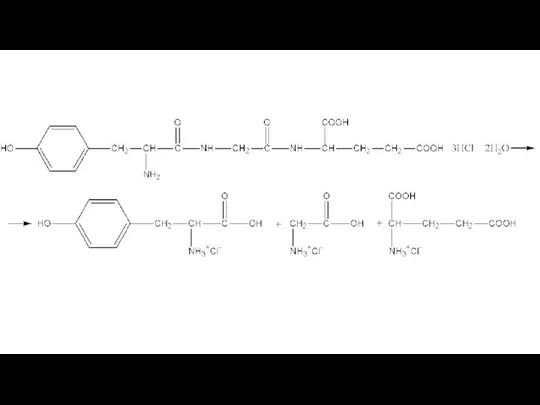
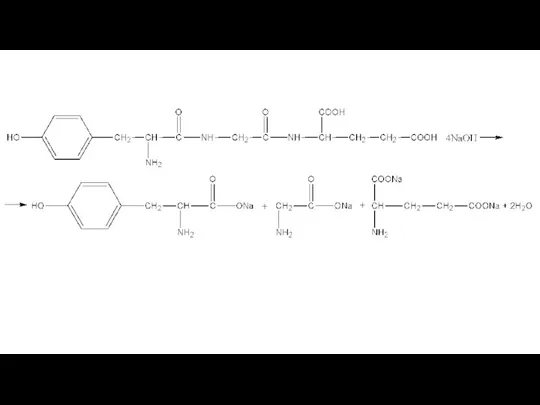
- 5. 9. Неизвестный трипептид подвергли гидролизу, в результате которого получилась смесь двух дипептидов и двух аминокислот. Массовая
- 6. Предположение о наличии трипептидов Glu-Tyr-Tyr Glu-Glu-Tyr Glu-Tyr-Glu Tyr-Glu-Tyr Дипептиды, образующиеся при гидролизе трипептидов Glu-Tyr, Tyr-Tyr, Glu-Glu
- 9. 10. Для установления состава природного алкалоида пиридинового ряда сожгли 1,251 г исследуемого вещества. Продукты реакции охладили.
- 10. Запишем молярное соотношение и определим молекулярную формулу алкалоида: ν(С):ν(Н):ν(N):ν(Cl) = 0,066:0,078:0,012:0,006, разделим на наименьшее число (0,006)
- 13. Скачать презентацию
Слайд 37. Используя только неорганические вещества и полученные из них органические прекурсоры, предложите
7. Используя только неорганические вещества и полученные из них органические прекурсоры, предложите

1) CaO + 3C = CaC2 + CO (в электропечи при 20000С);
2) СaC2 + 2H2O = Ca(OH)2 + HC≡CH;
3) 3HC≡CH = C6H6 (6000С, катализатор – активированный уголь);
4)
5)
6)
;
7)
8) HC=CH + H2O = CH3-CHO (кислая среда, в присутствии Hg2+);
9) CH3-CHO + 2[Ag(NH3)2OH] = CH3-COONH4 + 2Ag + 3NH3 + H2O (при нагревании);
10) CH3-COONH4 + HCl = CH3-COOH + NH4Cl;
11)
12)
Слайд 48. Определите, какие два вещества вступили в химическую реакцию, если в ее
8. Определите, какие два вещества вступили в химическую реакцию, если в ее

a) ? + ? → С6Н6 + К2CO3;
б) ? + ? → СН3COONa+ C2H5OH.
в) ? + ? → CH2=C=CH2 + KBr + H2O;
г) ? + ? → Br-CH2-CН2-СH2-Br;
д) ? + ? → CH3-C(O)-CH2-CH3.
а) С6Н5-СООК + KОН = C6H6 + K2CO3 (реагируют твердые бензоат калия и гидроксид калия при нагревании);
б) СН3-С(О)-О-С2Н5 + NaOH = CH3-COONa + C2H5OH (реагируют этилацетат и водный раствор гидроксида
натрия при нагревании);
в) СН2=СН-СН2-Br + KOH = CH2=C=CH2 + KBr + H2O (реагируют 3-бромпропен со спиртовым раствором гидроксида
калия при нагревании (возможна изомеризация в пропин при кипячении);
г) Br2 + = Br-CH2-CH2-CH2-Br (реагируют бром и циклопропан при ультрафиолетовом облучении);
д) НС≡С-СН2-СН3 + Н2О = СН3-С(О)-СН2-СН3 (реагируют бутин-1 и вода в присутствии Нg2+, H+).
Слайд 59. Неизвестный трипептид подвергли гидролизу, в результате которого получилась смесь двух дипептидов
9. Неизвестный трипептид подвергли гидролизу, в результате которого получилась смесь двух дипептидов

Определим аминокислоты, образовавшиеся при гидролизе трипептида. Отношение масс кислорода и азота в простейшей аминокислоте глицине, составляет 32/14 = 2,2857. В неизвестной аминокислоте 1 это отношение составляет 4,5714 (в два раза больше). Это значит, что в аминокислоте присутствует 2 карбоксильные группы. Условию задачи (ω(С+Н)=0,46938) соответствует глутаминовая кислота (Glu): HOOC-CH(NH2)-CH2-CH2-COOH.
В неизвестной аминокислоте 2 отношение составляет 3,4286, что соответствует наличию одной карбоксильной, одной аминогруппы и очевидно гидроксильной группы. Условию задачи (ω(С+Н)=0,65746) соответствует тирозин (Tyr):
.
Слайд 6Предположение о наличии трипептидов
Glu-Tyr-Tyr Glu-Glu-Tyr Glu-Tyr-Glu Tyr-Glu-Tyr
Дипептиды, образующиеся при гидролизе
Предположение о наличии трипептидов
Glu-Tyr-Tyr Glu-Glu-Tyr Glu-Tyr-Glu Tyr-Glu-Tyr
Дипептиды, образующиеся при гидролизе

Glu-Tyr, Tyr-Tyr, Glu-Glu
Образующиеся дипептиды не удовлетворяют соотношению молярных масс, равному 6:7.
Поскольку молярные массы дипептидов отличаются не значительно, предположим, что в состав трипептида входит простейшая аминокислота – глицин (Gly).
Тогда строение трипептида: Tyr-Gly-Glu, при гидролизе образуются дипептиды: Tyr-Gly и Gly-Glu. M(Tyr-Gly) = 238, а M(Gly-Glu) = 204, что соответствует условию задачи 6/7 = 0,8571 = 204/238.
Слайд 910. Для установления состава природного алкалоида пиридинового ряда сожгли 1,251 г исследуемого
10. Для установления состава природного алкалоида пиридинового ряда сожгли 1,251 г исследуемого

реакции охладили. Полученный при этом конденсат представлял собой раствор HCl, массой 0,867 г с массовой долей
вещества 25,26 %. Оставшуюся газовую смесь объемом 1,6128 л (н.у.) пропустили через избыток раствора щелочи. При
этом объем газовой смеси уменьшился до 134,4 мл (н.у.). Осаждение током сухого хлороводорода эфирного раствора
такой же навески исследуемого образца привело к образованию осадка массой 1,689 г.
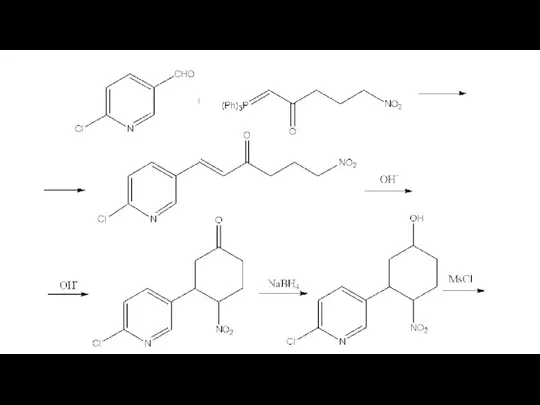
В качестве исходного соединения при разработке метода синтеза этого алкалоида был взят 3-замещенный 6-хлорпиридин,
и при помощи классических реакций увеличения углеродной цепи и нуклефильного присоединения был получен
3,4-дизамещенный циклогексанон состава C11H11N2O3Cl. Циклогексанон был превращен в целевой продукт
трехстадийным синтезом, включающим восстановление и нуклеофильное замещение, которые привели к образованию
фрагмента гетероцикла, структурно родственного норборнану. Алкалоид имеет один ассиметрический центр.
Определите строение этого алкалоида. Какую биологическую активность проявляет это соединение? Известны ли Вам
другие методы получения этого алкалоида?
Определим молекулярную формулу алкалоида:
m(HCl) = 0,867∙0,2526 = 0,219 г, что соответствует 0,219/36,5 = 0,006 моль;
m(H2O) = 0,867-0,219 = 0,648 г, что соответствует 0,6458/18 = 0,036 моль;
газ – поглотившийся избытком щелочи – углекислый газ, его объем – 1,4784 л, что соответствует 1,4784/22,4 = 0,066 моль;
газ – не поглотившийся избытком щелочи – азот, его объем 0,1344 л, что соответствует 0,1344/22,4 = 0,006 моль.
Слайд 10Запишем молярное соотношение и определим молекулярную формулу алкалоида: ν(С):ν(Н):ν(N):ν(Cl) = 0,066:0,078:0,012:0,006, разделим
Запишем молярное соотношение и определим молекулярную формулу алкалоида: ν(С):ν(Н):ν(N):ν(Cl) = 0,066:0,078:0,012:0,006, разделим
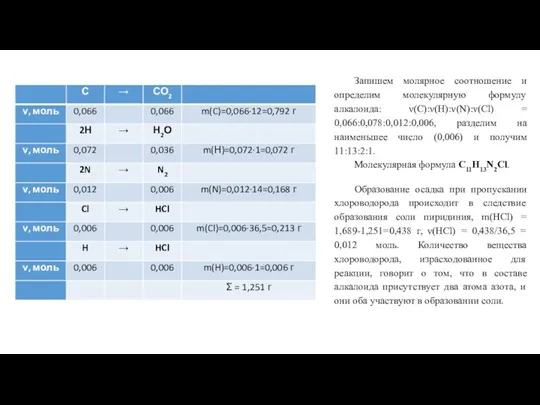
Молекулярная формула C11H13N2Cl.
Образование осадка при пропускании хлороводорода происходит в следствие образования соли пиридиния, m(HCl) = 1,689-1,251=0,438 г, ν(НСl) = 0,438/36,5 = 0,012 моль. Количество вещества хлороводорода, израсходованное для реакции, говорит о том, что в составе алкалоида присутствует два атома азота, и они оба участвуют в образовании соли.
 Основания. Схема образования гидроксида натрия
Основания. Схема образования гидроксида натрия Алкан бутан (C4H10)
Алкан бутан (C4H10) Состав атома
Состав атома Классификация коррозионных процессов металлов
Классификация коррозионных процессов металлов Лекция1Тов
Лекция1Тов Адсорбция. Механизмы адсорбции. Термодинамика адсорбции. Лекция 5
Адсорбция. Механизмы адсорбции. Термодинамика адсорбции. Лекция 5 Валентность, классы и номенклатура неорганических веществ
Валентность, классы и номенклатура неорганических веществ Водные биоресурсы и аквакультура. Расчеты в объемном анализе
Водные биоресурсы и аквакультура. Расчеты в объемном анализе Основания
Основания тб в кабинете биологии [Автосохраненный]
тб в кабинете биологии [Автосохраненный] Основные понятия термодинамики.Первое начало термодинамики и его применимость к биосистемам. (Лекция 04)
Основные понятия термодинамики.Первое начало термодинамики и его применимость к биосистемам. (Лекция 04) Практическая работа №5. Качественные реакции на анионы 1-3 групп
Практическая работа №5. Качественные реакции на анионы 1-3 групп Марганец. Химия элементов. Кислородосодержащие соединения
Марганец. Химия элементов. Кислородосодержащие соединения Химия в нашей жизни
Химия в нашей жизни Избыток, недостаток. Решение задач
Избыток, недостаток. Решение задач Процессы минералообразования
Процессы минералообразования Закономерности изменения окислительно-востановительных свойств соединений в периодах и группах
Закономерности изменения окислительно-востановительных свойств соединений в периодах и группах Получение и применение аренов
Получение и применение аренов Оксиды. Классификация оксидов
Оксиды. Классификация оксидов Лекция 6 Смазочные масла
Лекция 6 Смазочные масла Спирты. Тест
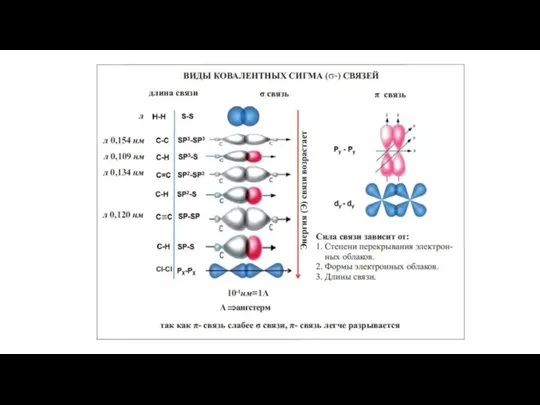
Спирты. Тест ОСОБЕННОСТИ СТРОЕНИЯ, РЕАКЦИОННОЙ СПОСОБНОСТИ И МЕТОДЫ СИНТЕЗА АЛКИНОВ
ОСОБЕННОСТИ СТРОЕНИЯ, РЕАКЦИОННОЙ СПОСОБНОСТИ И МЕТОДЫ СИНТЕЗА АЛКИНОВ Презентация на тему Химическая связь
Презентация на тему Химическая связь  Закалка и отпуск стали. Ознакомление со структурами серого и белого чугуна. Распознавание руд железа
Закалка и отпуск стали. Ознакомление со структурами серого и белого чугуна. Распознавание руд железа Сераорганические соединения
Сераорганические соединения Химическае препараты
Химическае препараты Срспальфа-олефинсульфанаттар
Срспальфа-олефинсульфанаттар Презентация по Химии "Строение и физические свойства металлов"
Презентация по Химии "Строение и физические свойства металлов"