Содержание
- 2. 1 признак химической реакции: Число и состав исходных и полученных веществ. 1) Реакция соединения – это
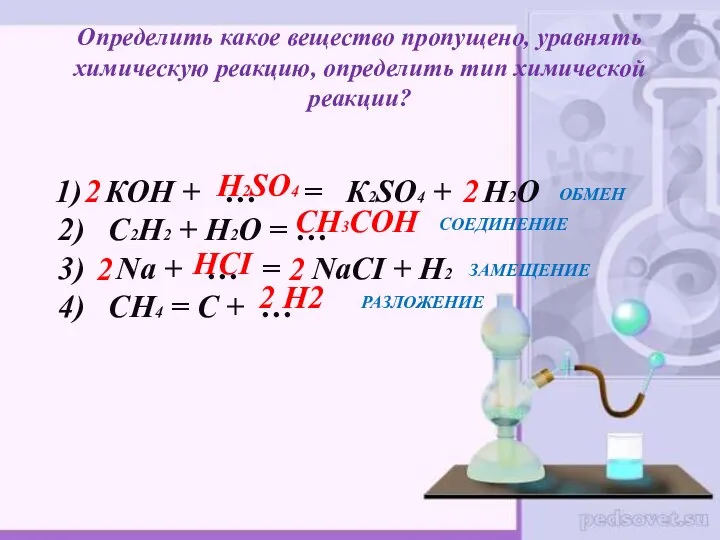
- 3. Определить какое вещество пропущено, уравнять химическую реакцию, определить тип химической реакции? 1) КОН + … =
- 4. 2 признак химической реакции: Изменение степени окисления. 1) Степени окисления – величина, которая показывает количество электронов
- 5. 3 признак химической реакции: Тепловой эффект. 1) Тепловой эффект реакции – энергия реакции, которая поглощается или
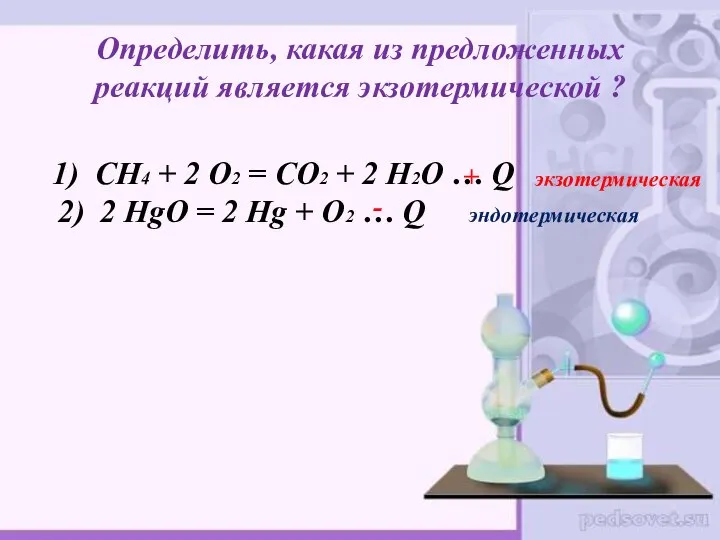
- 6. Определить, какая из предложенных реакций является экзотермической ? 1) СН4 + 2 О2 = СО2 +
- 7. 4 признак химической реакции: Агрегатное состояние веществ 1) Гомогенная реакция – это процесс, в котором все
- 8. Определить тип химической реакции по агрегатному состоянию веществ. 1) 3 C2H2(Г) = C6H6(Ж) 2) Zn(тв.) +
- 9. 5 признак химической реакции: Введение других веществ. 1) Катализатор – вещество, ускоряющее химическую реакцию, но само
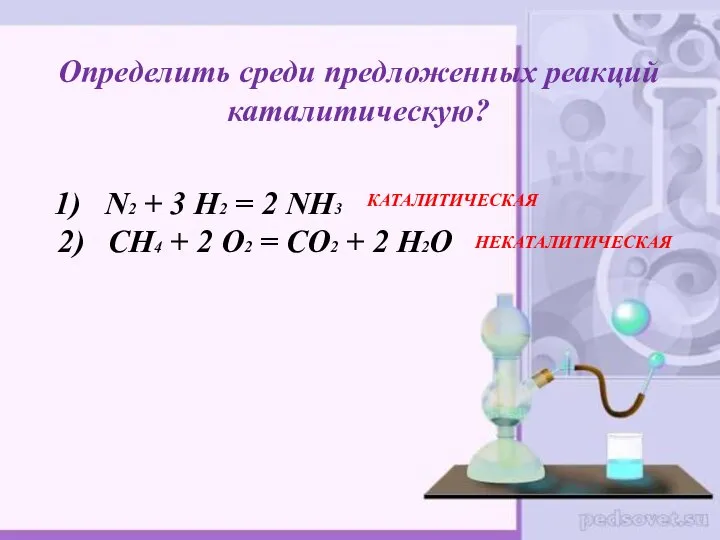
- 10. Определить среди предложенных реакций каталитическую? 1) N2 + 3 H2 = 2 NH3 2) СН4 +
- 11. 6 признак химической реакции: Обратимость 1) Необратимая реакция – это процесс, идущий в одном направлении (до
- 13. Скачать презентацию







 Полимеры с включением атомов бора и карборановой группировки - полиборорганосилоксаны и поликарборанорганосилосксаны
Полимеры с включением атомов бора и карборановой группировки - полиборорганосилоксаны и поликарборанорганосилосксаны Окисно-відновні реакції. Процеси окиснення та відновлення, окисники та відновники. 9 клас
Окисно-відновні реакції. Процеси окиснення та відновлення, окисники та відновники. 9 клас Масс-спектрометрия – аналитический метод определения молекулярной массы свободных ионов в высоком вакууме
Масс-спектрометрия – аналитический метод определения молекулярной массы свободных ионов в высоком вакууме Презентация на тему Химическая связь (8 класс)
Презентация на тему Химическая связь (8 класс)  Вымораживание воды
Вымораживание воды Ароматические углеводороды на примере бензола
Ароматические углеводороды на примере бензола Проектная работа Кристаллизация
Проектная работа Кристаллизация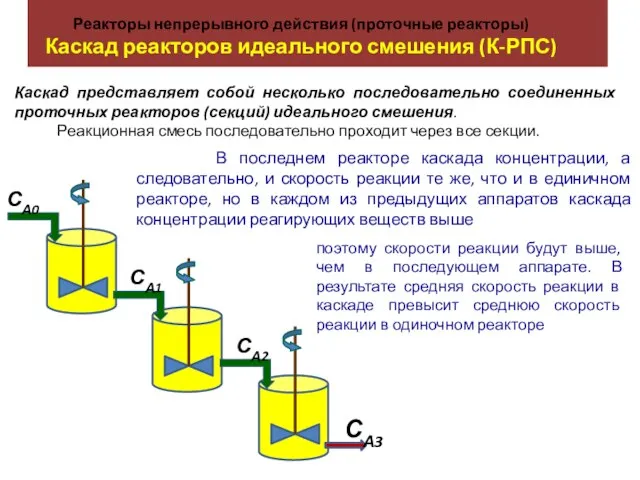 Реакторы непрерывного действия (проточные реакторы). Каскад реакторов идеального смешения (К-РПС)
Реакторы непрерывного действия (проточные реакторы). Каскад реакторов идеального смешения (К-РПС) Презентация на тему Оксиды
Презентация на тему Оксиды  10-4 (2)
10-4 (2) Аммиак. Свойства (9 класс)
Аммиак. Свойства (9 класс) Химическая связь. Строение вещества
Химическая связь. Строение вещества Кислород
Кислород Идеальный газ
Идеальный газ Презентация на тему Типы реакций
Презентация на тему Типы реакций  Технология растворов на неводных растворителях
Технология растворов на неводных растворителях Предмет органическая химия. Теория строения органических веществ
Предмет органическая химия. Теория строения органических веществ Основные классы неорганических соединений
Основные классы неорганических соединений Презентация на тему Обобщение по типам химических реакций
Презентация на тему Обобщение по типам химических реакций  Путешествие в мир кислот
Путешествие в мир кислот Презентация на тему: Изомерия
Презентация на тему: Изомерия Кроссворд по теме Металлы
Кроссворд по теме Металлы Органическая химия
Органическая химия Технология одноступенчатого гидрокрекинга. Аппаратное оформление и основные технологические решения
Технология одноступенчатого гидрокрекинга. Аппаратное оформление и основные технологические решения Многоэлектронные атомы
Многоэлектронные атомы Понятие об ароматических спиртах и фенолах. Особенности строения фенола
Понятие об ароматических спиртах и фенолах. Особенности строения фенола Получение галогенов. Биологическое значение и применение галогенов и их соединений
Получение галогенов. Биологическое значение и применение галогенов и их соединений V группа. Побочная подгруппа
V группа. Побочная подгруппа