Содержание
- 2. Цель урока: Продолжить формирование понятия об атоме как сложной нейтральной частице, состоящей из протонов, нейтронов и
- 3. Задачи урока; Образовательные: Познакомить учащихся с моделями атома Томсона и Резерфорда Изучить планетарную модель атома, состав
- 4. Эпиграф к уроку «Отыщи всему начало и ты многое поймешь»
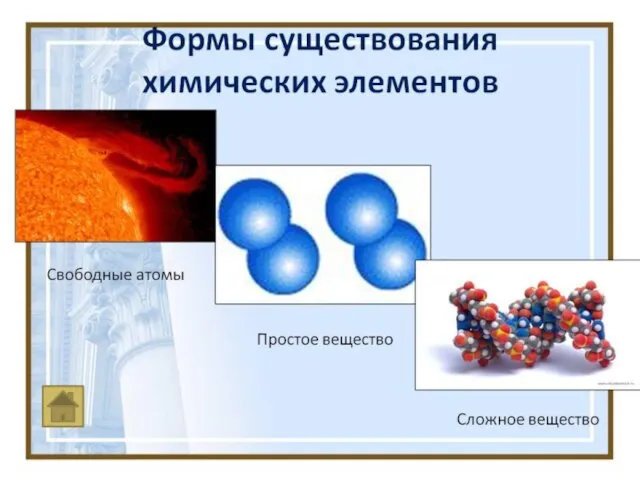
- 5. УРОК ХИМИИ В 8 КЛАССЕ ОСНОВНЫЕ СВЕДЕНИЯ О СТРОЕНИИ АТОМОВ
- 7. Демокрит В основе философии Демокрита лежит учение об атомах и пустоте как двух принципах, порождающих многообразие
- 8. Ирландский физик Стони на основании опытов пришел к выводу, что электричество переносится мельчайшими частицами, существующими в
- 9. Модель Томсона В 1904 году Томсон представил свою новую модель атома. Она представляла собой также равномерно
- 10. Расщепление радиоактивного излучения в электрическом поле
- 11. Опыт Резерфорда Резерфорд исследовал особенности прохождения альфа-частиц через тонкие металлические пластинки. На основании этих опытов ученый
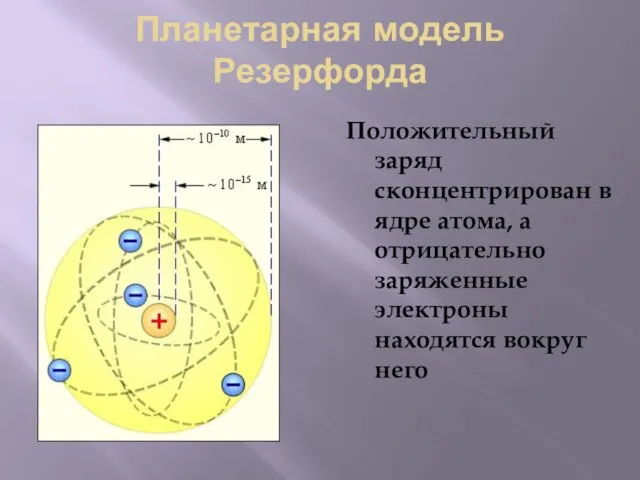
- 12. Планетарная модель Резерфорда Положительный заряд сконцентрирован в ядре атома, а отрицательно заряженные электроны находятся вокруг него
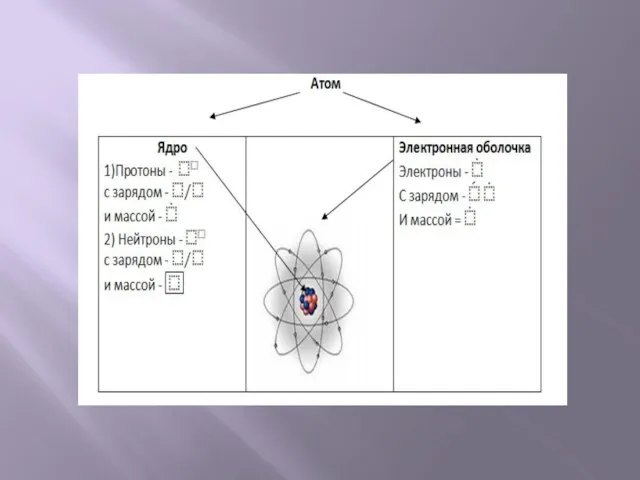
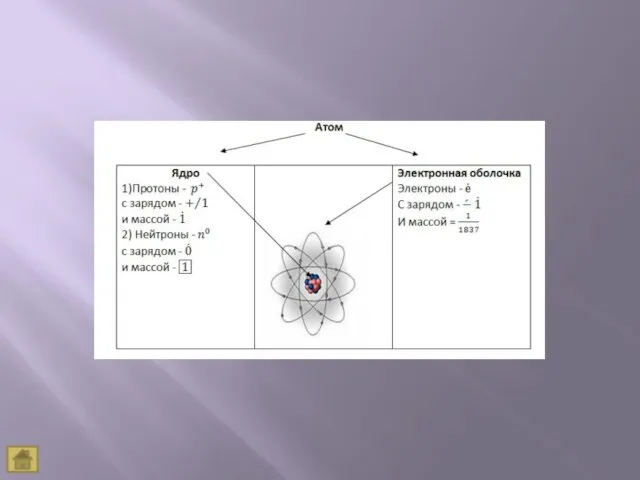
- 13. В атоме электроны вращаются вокруг атомного ядра, которое заряжено положительно и притягивает отрицательно заряженные электроны В
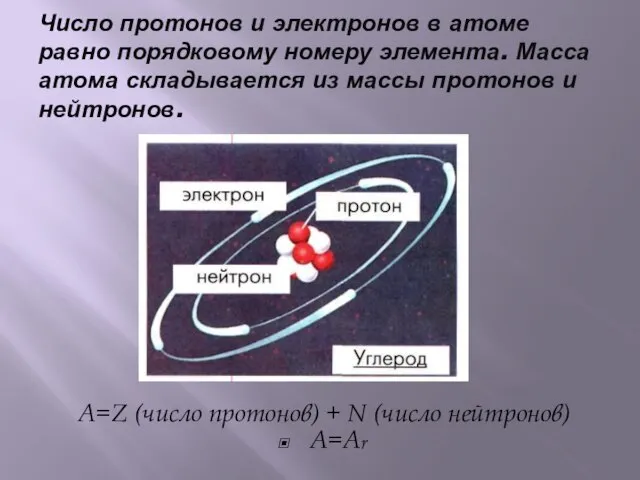
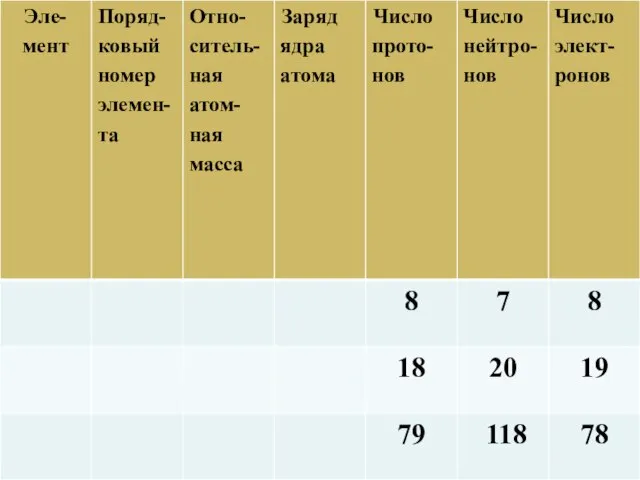
- 14. Число протонов и электронов в атоме равно порядковому номеру элемента. Масса атома складывается из массы протонов
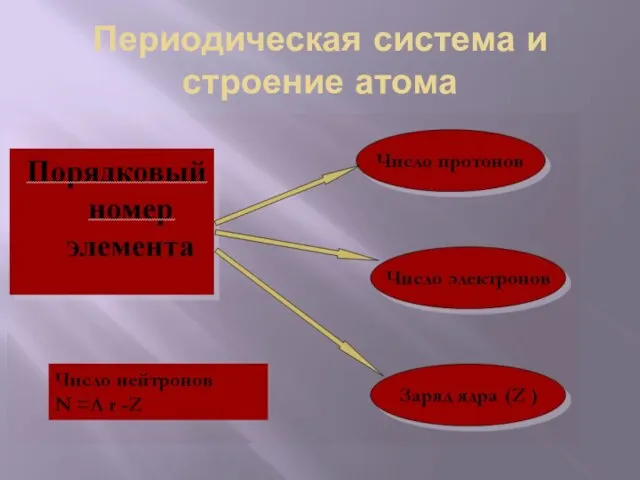
- 16. Периодическая система и строение атома
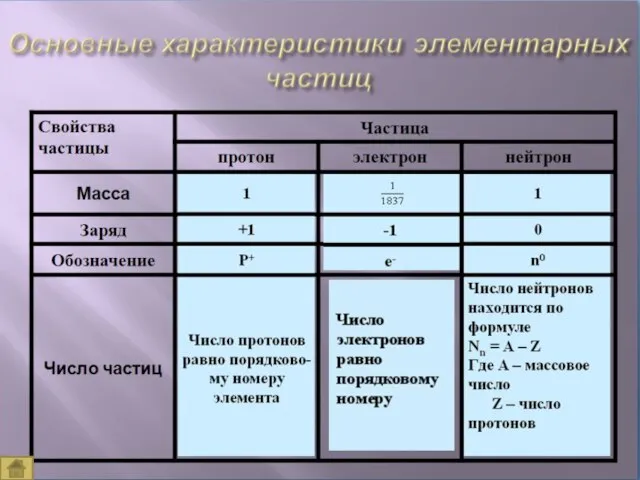
- 17. Z – порядковый номер химического элемента, указывает на заряд ядра, а следовательно на число протонов, а
- 18. Порядковый Заряд Число номер = ядра = электронов элемента атома в атоме
- 19. Порядковый Заряд Число Число номер = ядра = электронов = протонов элемента атома в атоме в
- 20. N=А- Z;
- 21. НАПРИМЕР СТРОЕНИЕ АТОМА УГЛЕРОДА 6 протонов 6 электронов 6 нейтронов
- 22. Основные выводы Атом является мельчайшей частицей вещества Вся масса атома сосредоточена в его ядре, объем которого
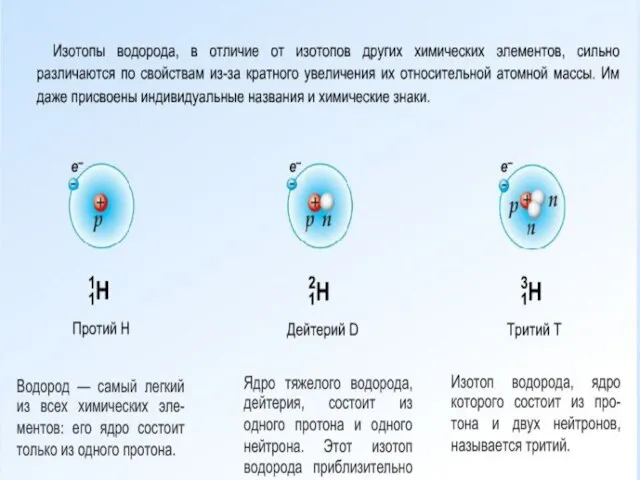
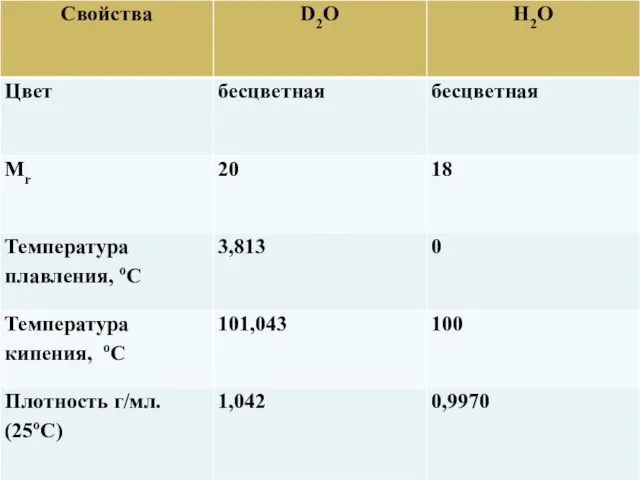
- 24. Изотопы – это разновидности атомов одного химического элемента, имеющие одинаковое число протонов и электронов, но разное
- 25. Изотопы
- 26. + Масса изотопа-1 * распростра-ненность Масса изотопа-2 * распростра-ненность Аr =
- 27. Химический элемент – это совокупность атомов с одинаковым зарядом ядра.
- 34. Выберите верные утверждения Ядро атома содержит протоны и нейтроны, суммарная масса которых равна массовому числу атома.
- 35. Выберите верные утверждения Ядро атома содержит протоны и нейтроны, суммарная масса которых равна массовому числу атома.
- 38. Домашнее задание; § 6 – повторить; § 7 § 8 – учить; письменно выполнить 2 стр.
- 39. Тест по теме «Строение атома» 1. Положительно заряженная частица называется А) электронБ) протонВ) нейтрон 2. Отрицательно
- 40. Вставьте пропущенные слова 2. Вся масса атома сосредоточена в . Число нейтронов = -
- 41. Оценка своего эмоционального состояния учащимися
- 43. Скачать презентацию













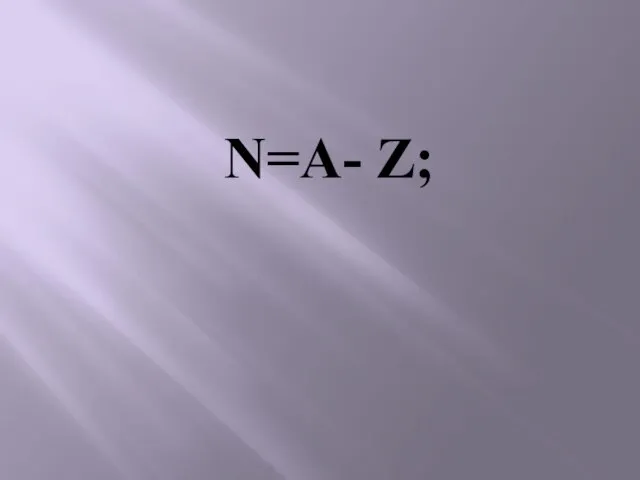














 Криптон. Самостоятельная работа
Криптон. Самостоятельная работа 20170625_otkrytyy_integrirovannyy_urok_himiya-geografiya
20170625_otkrytyy_integrirovannyy_urok_himiya-geografiya Устойчивость коллоидных лиофобных дисперсных систем. Теория ДЛФО. Лекция 14
Устойчивость коллоидных лиофобных дисперсных систем. Теория ДЛФО. Лекция 14 Строение атома
Строение атома Обобщающий урок по теме: Изменения происходящие с веществами
Обобщающий урок по теме: Изменения происходящие с веществами Метод МО Хюккеля (МОХ)
Метод МО Хюккеля (МОХ) Сравнительный анализ Фармакопейных статей для субстанций, представленных в мировых Фармакопеях
Сравнительный анализ Фармакопейных статей для субстанций, представленных в мировых Фармакопеях Гибридизация АО. Пространственное строение молекул (геометрия молекул)
Гибридизация АО. Пространственное строение молекул (геометрия молекул) Презентация по Химии "Химический БРЕЙН-РИНГ"
Презентация по Химии "Химический БРЕЙН-РИНГ"  Сера и ее соединения
Сера и ее соединения Prezentatsia1_1 (1)
Prezentatsia1_1 (1) Интеллектуальная игра по теме: «Периодический закон и система химических элементов Д.И. Менделеева». «Химический дом и его обитат
Интеллектуальная игра по теме: «Периодический закон и система химических элементов Д.И. Менделеева». «Химический дом и его обитат Төртінші негізгі топша элементтері
Төртінші негізгі топша элементтері Презентация на тему Показатели воды - её жесткость и кислотность
Презентация на тему Показатели воды - её жесткость и кислотность  Химия һәм сәламәт яшәү рәвеше
Химия һәм сәламәт яшәү рәвеше Вуглеводи
Вуглеводи Синтез и свойства кукурбитурилов
Синтез и свойства кукурбитурилов Сложные эфиры
Сложные эфиры Азот
Азот Закон сохранения массы веществ. Уравнения химических реакций.
Закон сохранения массы веществ. Уравнения химических реакций. Подготовка к контрольной работе. 8 класс
Подготовка к контрольной работе. 8 класс Аттестационная работа. Многогранники: от молекулы до кристалла
Аттестационная работа. Многогранники: от молекулы до кристалла Химические волокна. Урок 1-2
Химические волокна. Урок 1-2 Простые вещества - металлы. 8 класс
Простые вещества - металлы. 8 класс Полимеры
Полимеры Генетическая связь между классами неорганических соединений
Генетическая связь между классами неорганических соединений Магний - активный, но под защитой
Магний - активный, но под защитой Водород
Водород