Содержание
- 2. Расскажу сегодня, что ли, О зловредной роли моли. Моль съедает шерсть и мех – Просто паника
- 3. Моль Моль – это такое количество вещества, в котором содержится 6*10 23 молекул (или других структурных
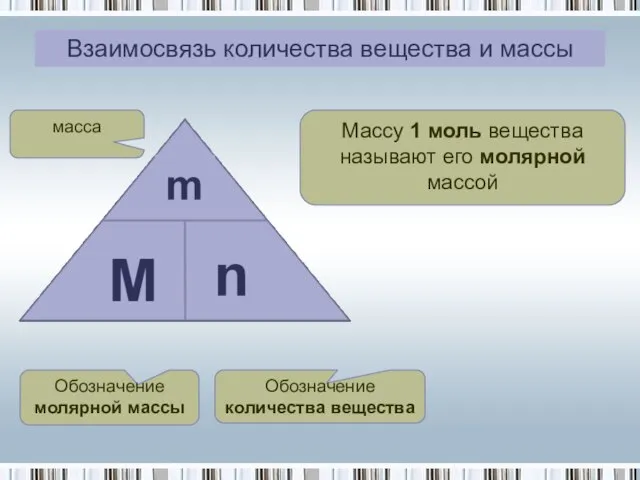
- 4. Взаимосвязь количества вещества и массы Массу 1 моль вещества называют его молярной массой Обозначение молярной массы
- 5. Единицы измерения [ М] – г/моль, [ m] – г, кг/кмоль, кг, мг/ммоль. мг. [ n]
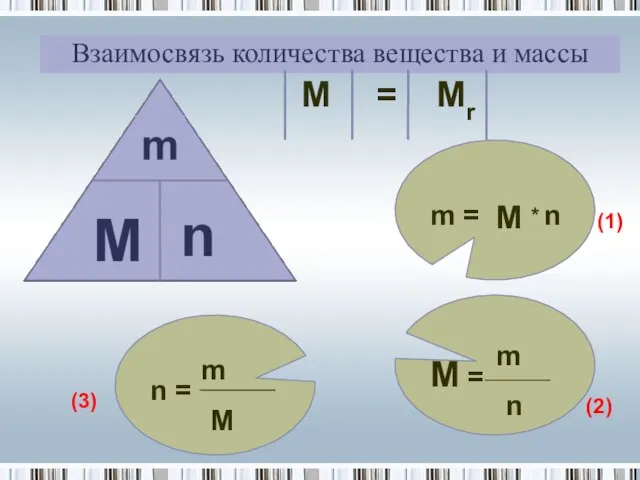
- 6. Взаимосвязь количества вещества и массы m = M n (1) M = m n (2) n
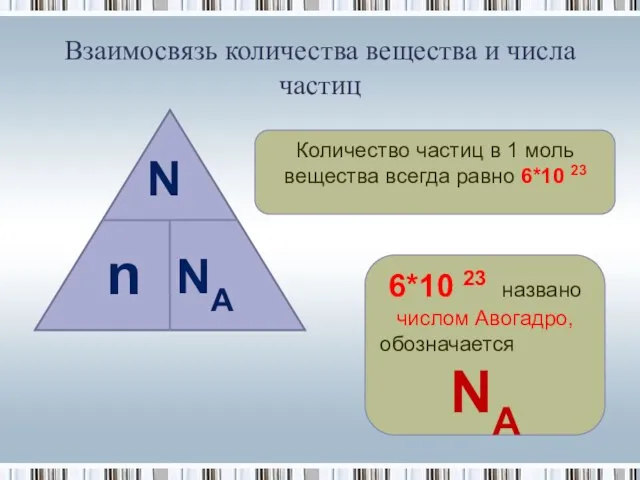
- 7. Взаимосвязь количества вещества и числа частиц Количество частиц в 1 моль вещества всегда равно 6*10 23
- 8. Куча песка, засыпавшая большой завод, содержит песчинок в 22400 раз меньше, чем число частиц в 1
- 9. Ниагарский водопад (США)
- 10. Число Авогадро - NA Некоторое представление о величине числа Авогадро даёт следующий пример. Количество воды, которое
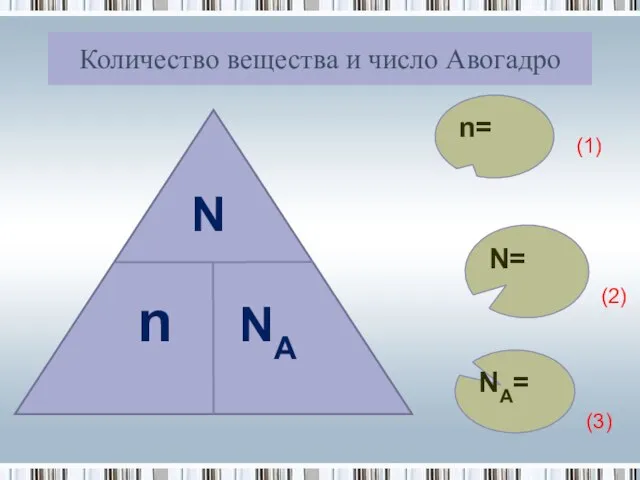
- 11. Количество вещества и число Авогадро n= N= NA= (1) (2) (3)
- 12. тема урока Относительная атомная и молекулярная массы
- 13. Химический диктант Начертите таблицу по образцу, аккуратно перепишите в неё формулы
- 14. Задания
- 15. Относительная атомная масса Атомы элементов характеризуются определённой (только им присущей) массой. Например, масса атома Н равна
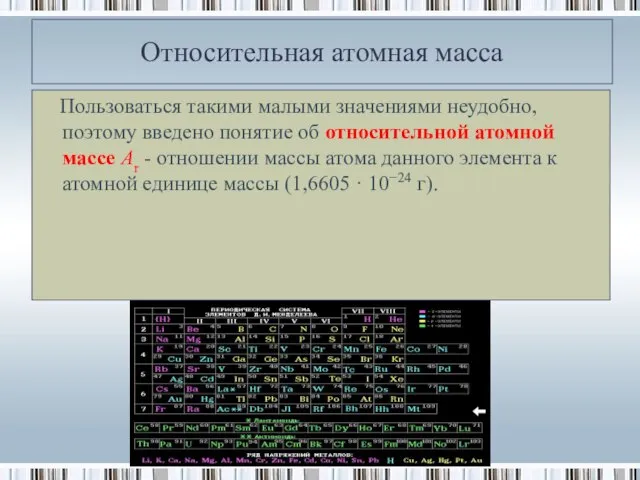
- 16. Относительная атомная масса Пользоваться такими малыми значениями неудобно, поэтому введено понятие об относительной атомной массе Аr
- 17. Относительная молекулярная масса - Мr Значения относительной молекулярной массы рассчитываются из значений относительной атомной массы с
- 18. Относительная молекулярная масса - Мr Установлено, что 12 г углерода (в виде графита или алмаза) содержат
- 19. Массовая доля элемента в сложном веществе По известной химической формуле сложного вещества определяют массовые доли элементов,
- 20. Массовая доля элемента в сложном веществе Массовая доля элемента - это доля от единицы или доля
- 21. Домашнее задание § 16, № 2,3
- 23. Скачать презентацию


![Единицы измерения [ М] – г/моль, [ m] – г, кг/кмоль, кг,](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/849541/slide-4.jpg)











 Аморфные и кристаллические вещества
Аморфные и кристаллические вещества Структуры железоуглеродистых сплавов в равновесном состоянии
Структуры железоуглеродистых сплавов в равновесном состоянии Основания. Равновесия в растворах
Основания. Равновесия в растворах Генетическая связь между классами неорганических веществ
Генетическая связь между классами неорганических веществ Соли, их классификация и свойства
Соли, их классификация и свойства Образовательные технологии, используемые на уроках химии для повышения мотивации обучения
Образовательные технологии, используемые на уроках химии для повышения мотивации обучения Названия комплексов с мостиковыми лигандами
Названия комплексов с мостиковыми лигандами Химические структуры
Химические структуры Сравнение относительной эффективности предполагаемых ингибиторов коррозии методом гальванопары
Сравнение относительной эффективности предполагаемых ингибиторов коррозии методом гальванопары Гибридизация АО. Пространственное строение молекул (геометрия молекул)
Гибридизация АО. Пространственное строение молекул (геометрия молекул) Нитробактерии. Нитратное дыхание
Нитробактерии. Нитратное дыхание Виды изомерии. Углеводороды
Виды изомерии. Углеводороды Презентация на тему Викторина "Узнай химический элемент"
Презентация на тему Викторина "Узнай химический элемент"  Загрязнение почв пестицидами
Загрязнение почв пестицидами АКТИВІЗАЦІЯ ТВОРЧОЇ ДІЯЛЬНОСТІ УЧНІВ У ПРОЦЕСІ СТВОРЕННЯ І ВИКОРИСТАННЯ ПРОЕКТІВ У POWER POINT НА УРОКАХ ХІМІЇ
АКТИВІЗАЦІЯ ТВОРЧОЇ ДІЯЛЬНОСТІ УЧНІВ У ПРОЦЕСІ СТВОРЕННЯ І ВИКОРИСТАННЯ ПРОЕКТІВ У POWER POINT НА УРОКАХ ХІМІЇ Галогениды. Лекция 11
Галогениды. Лекция 11 Общие свойства растворов
Общие свойства растворов Сильные и слабые электролиты
Сильные и слабые электролиты Арены. Бензол
Арены. Бензол Железо и его соединения
Железо и его соединения Нитраты в продуктах
Нитраты в продуктах Предмет органической химии. Урок №1
Предмет органической химии. Урок №1 Надмолекулярные структуры
Надмолекулярные структуры Презентация на тему Валентность и степень окисления (8 класс)
Презентация на тему Валентность и степень окисления (8 класс)  Презентация на тему Химический алфавит
Презентация на тему Химический алфавит  Соли. Составление формул и номенклатура
Соли. Составление формул и номенклатура Дисперсные системы. Гели
Дисперсные системы. Гели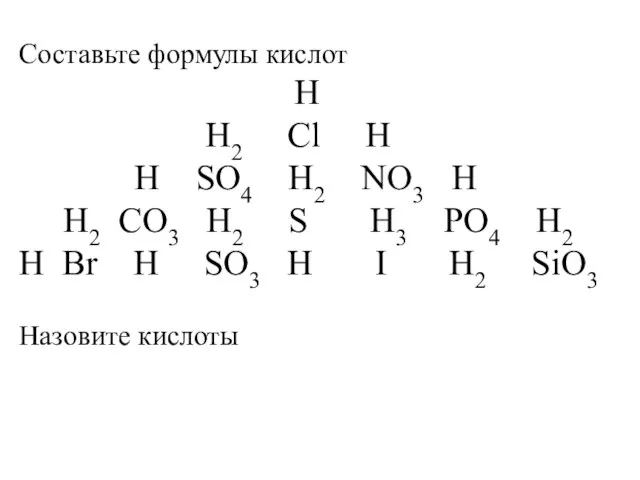 Составьте формулы кислот
Составьте формулы кислот