Содержание
- 2. VLASTNOSTI Už v minulosti ľudia zistili, že niektoré látky majú kyslú chuť a nazvali ich kyseliny.
- 3. VLASTNOSTI Indikátory sú napr.: lakmus metyloranž metylčerveň fenolftaleín
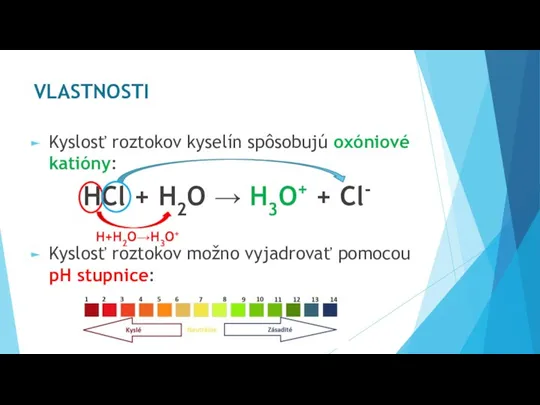
- 4. VLASTNOSTI Kyslosť roztokov kyselín spôsobujú oxóniové katióny: HCl + H2O → H3O+ + Cl- Kyslosť roztokov
- 6. KYSELINY V DOMÁCNOSTI Sú to napr.: kyselina citrónová (citrusové ovocie) kyselina octová (ocot) kyselina askorbová (=vitamín
- 7. ROZDELENIE KYSELÍN 1. BEZKYSLÍKATÉ KYSELINY sú dvojprvkové zlúčeniny vodíka a nekovového prvku, v ktorých je to
- 8. ROZDELENIE KYSELÍN 2. KYSLÍKATÉ KYSELINY sú trojprvkové zlúčeniny vodíka a nekovového prvku a kyslíka, napr: HNO3
- 9. NÁZOV je dvojslovný: podstatné meno + prídavné meno Podstatné meno = kyselina Prídavné meno = názov
- 10. má tri časti, ktoré sú uložené v poradí: napr. kyselina dusičná HI NV O-II I+V=6:2=3 HNO3
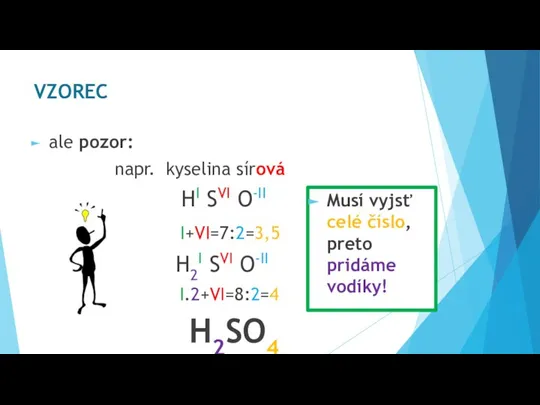
- 11. ale pozor: napr. kyselina sírová HI SVI O-II I+VI=7:2=3,5 H2I SVI O-II I.2+VI=8:2=4 H2SO4 VZOREC Musí
- 12. HaI XbI-VIII Oc-II I.a+(I-VIII).b=číslo:2=c VŠEOBECNÝ VZOREC Prečo a a b? Lebo kyselina môže obsahovať viac vodíkov
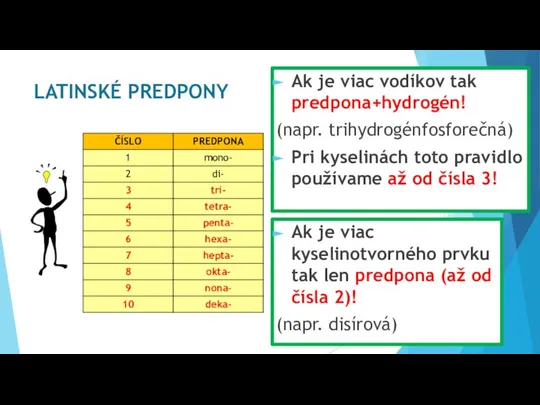
- 13. LATINSKÉ PREDPONY Ak je viac vodíkov tak predpona+hydrogén! (napr. trihydrogénfosforečná) Pri kyselinách toto pravidlo používame až
- 14. napr. kyselina trihydrogénfosforečná H3I PV O-II I.3+V=8:2=4 H3PO4 VZOREC
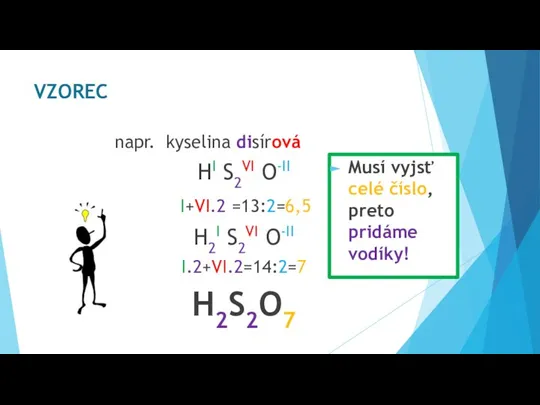
- 15. napr. kyselina disírová HI S2VI O-II I+VI.2 =13:2=6,5 H2I S2VI O-II I.2+VI.2=14:2=7 H2S2O7 VZOREC Musí vyjsť
- 16. VÝZNAMNÉ KYSELINY Kyseliny sú žieraviny, preto sa pri práci s nimi musia dodržiavať bezpečnostné opatrenia.
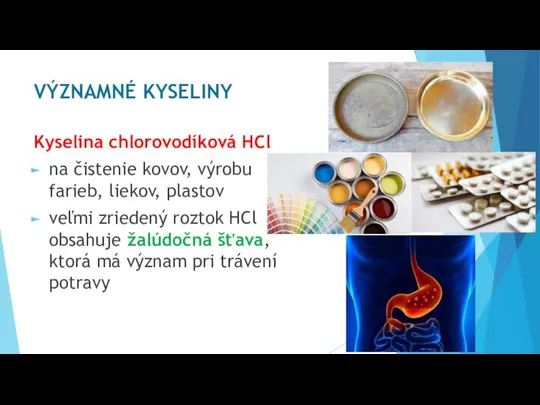
- 17. VÝZNAMNÉ KYSELINY Kyselina chlorovodíková HCl na čistenie kovov, výrobu farieb, liekov, plastov veľmi zriedený roztok HCl
- 18. VÝZNAMNÉ KYSELINY Kyselina dusičná HNO3 VÝROBA: výbušnín liekov farieb hnojív
- 20. Скачать презентацию












 Химическое равновесие
Химическое равновесие Химия и география. Блиц-опрос. 7 класс
Химия и география. Блиц-опрос. 7 класс Амилаза. Строение амилазы
Амилаза. Строение амилазы Моющие и чистящие средства
Моющие и чистящие средства Основные химические законы
Основные химические законы Соли: получение
Соли: получение Синтетическое моторное масло. Маркировка моторных масел
Синтетическое моторное масло. Маркировка моторных масел Khim_8
Khim_8 Химические реакции
Химические реакции Систематизация знаний по периодической системе химических элементов
Систематизация знаний по периодической системе химических элементов химия
химия Nevarne snovi
Nevarne snovi Основания. Классификация
Основания. Классификация Стелс-материалы
Стелс-материалы Тип кристаллической решетки у белого фосфора…. Тест
Тип кристаллической решетки у белого фосфора…. Тест Классификация и свойства кислот
Классификация и свойства кислот Сeквенирование нуклеиновых кислот
Сeквенирование нуклеиновых кислот Набор для выращивания монокристалла. Защита проекта
Набор для выращивания монокристалла. Защита проекта Алканы. Строение, номенклатура, изомерия, физические свойства
Алканы. Строение, номенклатура, изомерия, физические свойства Реакции разложения и соединения
Реакции разложения и соединения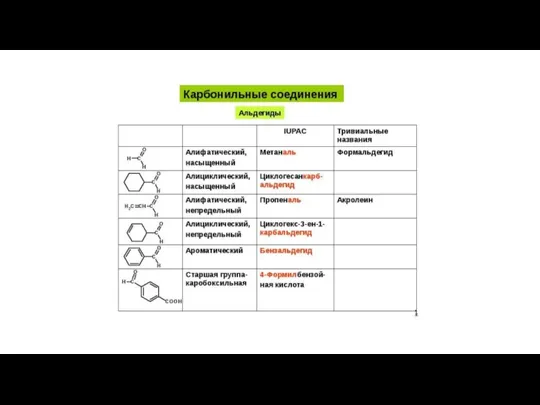 Карбонильные соединения (альдегиды)
Карбонильные соединения (альдегиды) карбоновые кислоты
карбоновые кислоты Вуглеводи. Групи
Вуглеводи. Групи Вычисление температур стеклования полимера при различных степенях отверждения смолы
Вычисление температур стеклования полимера при различных степенях отверждения смолы Сера
Сера Валенттілік. Атом-молекулалы ілім
Валенттілік. Атом-молекулалы ілім Классификация органических соединений
Классификация органических соединений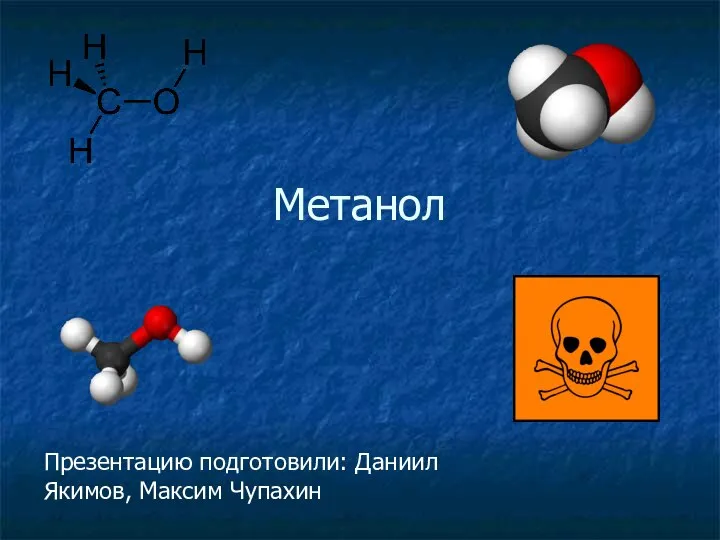 Метанол. Краткая характеристика
Метанол. Краткая характеристика