Содержание
- 2. А + В = С + D Условная реакция Чем быстрее происходит процесс изменения концентраций веществ,
- 3. Δn Для того чтобы определить скорость химической реакции нужно знать изменение химического количества ∆n одного из
- 4. Скорость химической реакции — это величина, которая равна отношению изменения молярной концентрации вещества к интервалу времени,
- 5. Гомогенные реакции — это реакции, протекающие в однородной среде, т.е. там, где нет поверхности раздела реагирующих
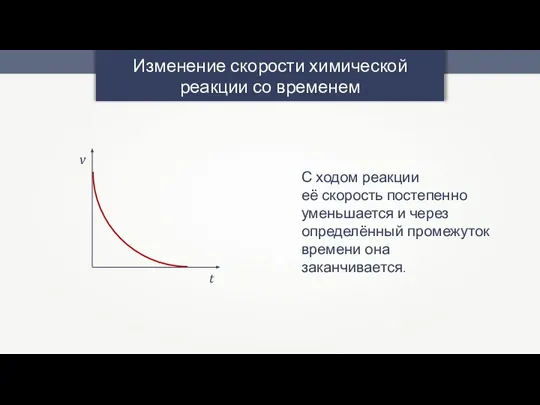
- 6. Изменение скорости химической реакции со временем v t С ходом реакции её скорость постепенно уменьшается и
- 7. Химическая кинетика — раздел химии, который изучает скорость химических реакций.
- 8. Факторы, которые оказывают влияние на скорость химических реакций: – природа реагирующих веществ; – их концентрация; –
- 9. 1. Природа реагирующих веществ HCl Цинк (Zn) Железо (Fe) Медь (Cu)
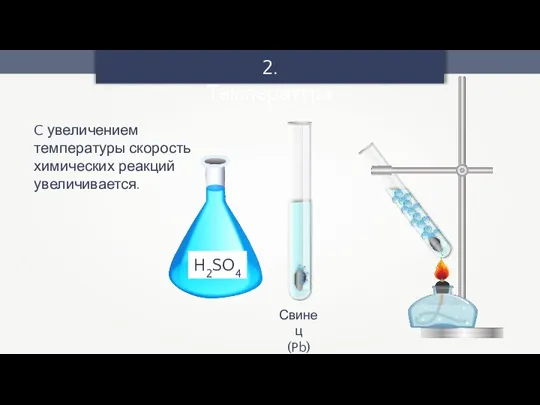
- 10. 2. Температура Свинец (Pb) C увеличением температуры скорость химических реакций увеличивается.
- 11. Якоб Хендрик Вант-Гофф 1852–1911 гг. Голландский учёный. Установил количественную зависимость скорости реакций от температуры в 1884
- 12. Правило Вант-Гоффа: при изменении температуры (повышении либо понижении) на каждые 10°С скорость реакции соответственно изменяется (увеличивается
- 13. γ — температурный коэффициент, который показывает во сколько раз увеличится скорость реакции с повышением температуры на
- 14. 3. Концентрация исходных веществ Чем выше молярные концентрации исходных веществ, тем больше скорость химической реакции.
- 15. К. Гульдберг и П. Вааге Зависимость скорости химической реакции от концентрации реагирующих веществ описана основным законом
- 16. Закон действующих масс: скорость химической реакции прямо пропорциональна произведению концентраций реагирующих веществ, взятых в степенях, равных
- 17. Закон действующих масс справедлив только для наиболее простых по своему механизму взаимодействий.
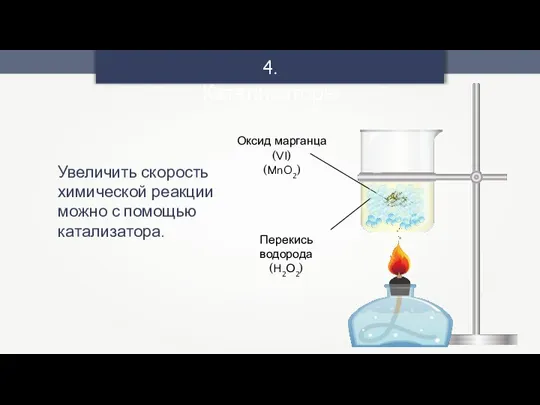
- 18. 4. Катализаторы Увеличить скорость химической реакции можно с помощью катализатора.
- 19. Катализатор — вещество, которое увеличивает скорость химической реакции, но само при этом не расходуется и в
- 20. Катализ — процесс изменения скорости химической реакции добавлением катализатора. Каталитические реакции — реакции с участием катализаторов.
- 21. Ферменты — биологические катализаторы белковой природы.
- 22. Ферменты действуют только в определённом интервале температур и определённой среде, что связано с их белковым происхождением.
- 23. Ингибиторы — вещества, которые служат для уменьшения скорости реакции.
- 25. Скачать презентацию

















 Амины, азо- и диазосоединения (продолжение)
Амины, азо- и диазосоединения (продолжение) Консерванты, их виды и применение
Консерванты, их виды и применение Электронные оболочки атомов
Электронные оболочки атомов Химическая связь
Химическая связь Физические свойства водорода
Физические свойства водорода Биосинтез фенольных соединений в растениях
Биосинтез фенольных соединений в растениях Вязкость жидкости
Вязкость жидкости Алюминий и его органические производные
Алюминий и его органические производные Plexiglas. Органическое стекло
Plexiglas. Органическое стекло Алмаз, бриллиант
Алмаз, бриллиант Презентация на тему Лабораторное оборудование. Посуда и средства защиты
Презентация на тему Лабораторное оборудование. Посуда и средства защиты  Основания и их свойства
Основания и их свойства Материаловедение. Стали. Свойства сталей. Классификация сталей
Материаловедение. Стали. Свойства сталей. Классификация сталей Мило. Вищі карбонові кислоти
Мило. Вищі карбонові кислоти Относительная молекулярная массa. Химический диктант
Относительная молекулярная массa. Химический диктант Типы химических реакций. 8 класс
Типы химических реакций. 8 класс Строение и функции отдельных коферментов
Строение и функции отдельных коферментов Известная и неизвестная вода
Известная и неизвестная вода Алюминий и его соединения
Алюминий и его соединения Соли. Состав и классификация
Соли. Состав и классификация Химические средства защиты растений
Химические средства защиты растений Периодическая система Д.И.Менделеева
Периодическая система Д.И.Менделеева Алкадиены. Каучук
Алкадиены. Каучук Молекулы. Свойства молекул
Молекулы. Свойства молекул Эксперимент с духами
Эксперимент с духами Закон сохранения массы. 11 класс
Закон сохранения массы. 11 класс Кристаллические решетки
Кристаллические решетки Кинетика физико-химических процессов
Кинетика физико-химических процессов