Содержание
- 2. ЗАДАНИЕ 1 (выполнить в тетрадях) Дайте названия следующим углеводородам по международной номенклатуре. СН3 СН3 – СН2
- 3. Строение молекулы CnH2n Химические свойства Изомерия Физические свойства Проверка знаний Получение Номенклатура Применение Алкены
- 4. Это интересно Всем известный полиэтилен был получен был получен в 1933 году Э. Фосеттом и Р.
- 5. Алкены – это углеводороды, в молекуле которых кроме одинарных связей содержится одна двойная связь между атомами
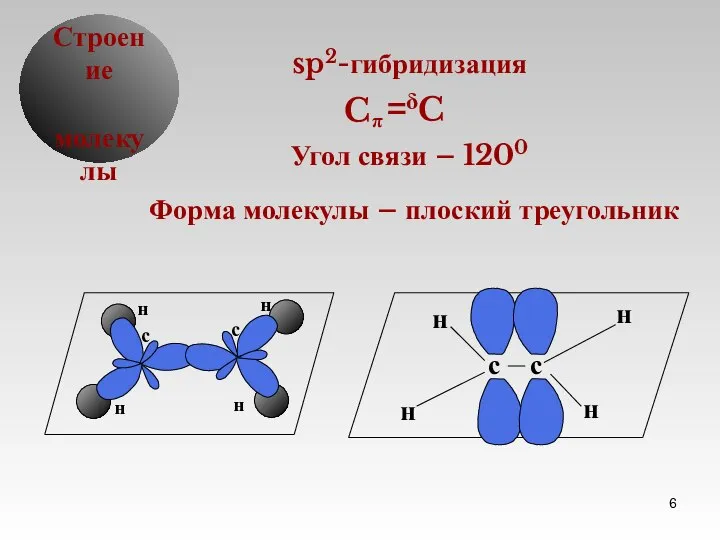
- 6. δ Строение молекулы sp2-гибридизация Угол связи – 1200 Форма молекулы – плоский треугольник C π C
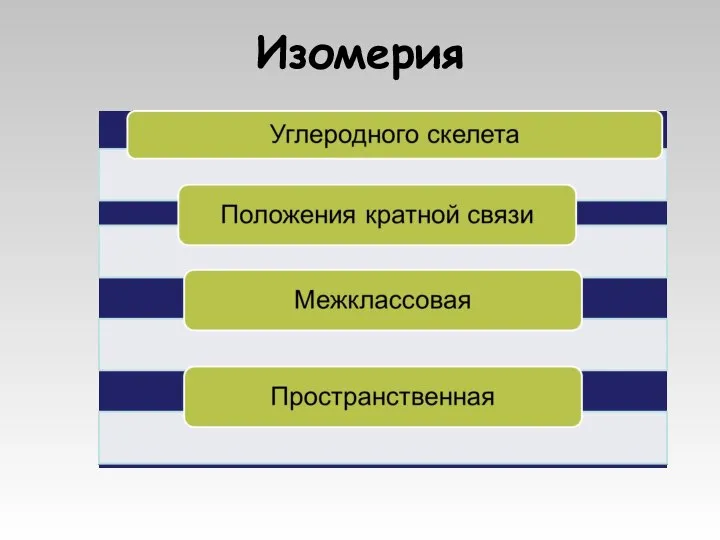
- 7. Изомерия
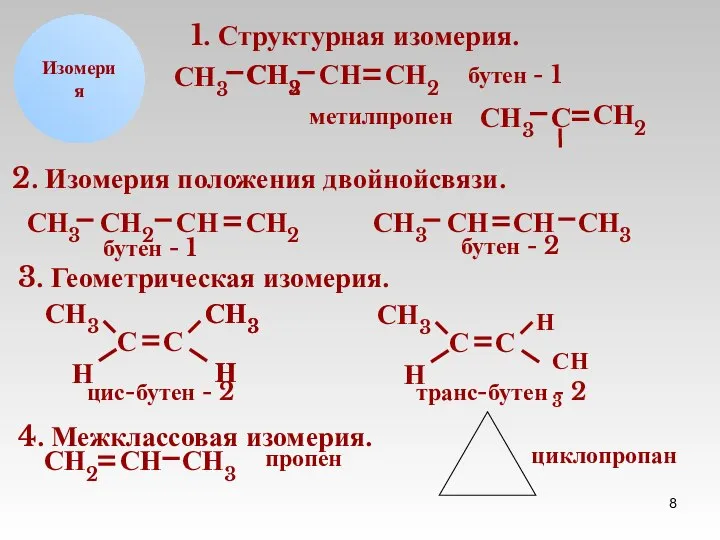
- 8. СН2 СН СН3 Н Изомерия 1. Структурная изомерия. СН2 СН3 С СН2 СН3 С СН2 бутен
- 9. Физические свойства Агрегатное состояние: С2Н4 – С4Н8 газообразные вещества; С5Н10 – С18Н36 жидкости; с С19Н38 твердые
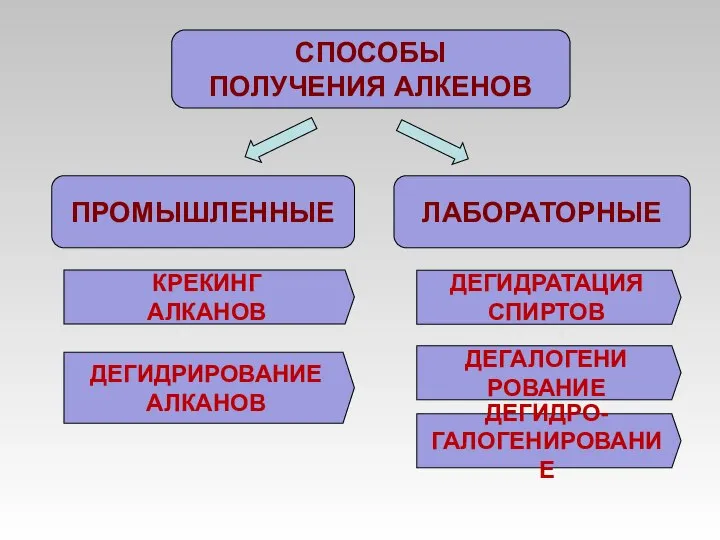
- 10. ПРОМЫШЛЕННЫЕ СПОСОБЫ ПОЛУЧЕНИЯ АЛКЕНОВ ЛАБОРАТОРНЫЕ КРЕКИНГ АЛКАНОВ ДЕГИДРИРОВАНИЕ АЛКАНОВ ДЕГИДРАТАЦИЯ СПИРТОВ ДЕГАЛОГЕНИ РОВАНИЕ ДЕГИДРО- ГАЛОГЕНИРОВАНИЕ
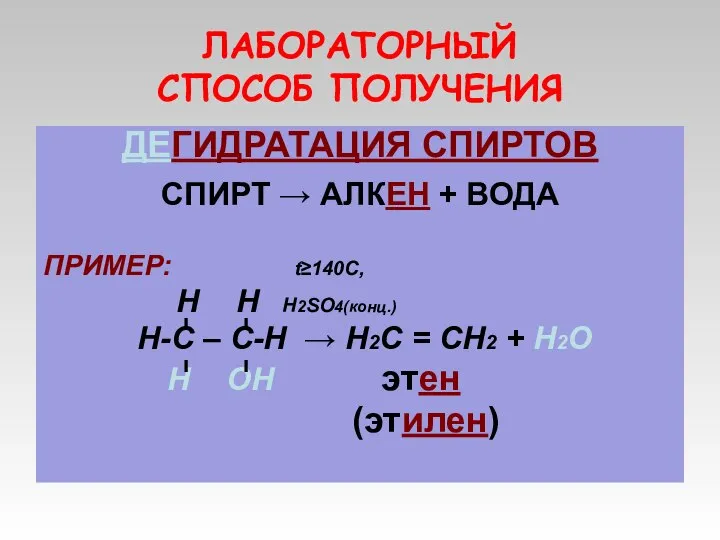
- 11. ЛАБОРАТОРНЫЙ СПОСОБ ПОЛУЧЕНИЯ ДЕГИДРАТАЦИЯ СПИРТОВ СПИРТ → АЛКЕН + ВОДА ПРИМЕР: t≥140C, Н Н Н2SO4(конц.) Н-С
- 12. Получение алкенов КРЕКИНГ АЛКАНОВ АЛКАН → АЛКАН + АЛКЕН С БОЛЕЕ ДЛИННОЙ С МЕНЕЕ ДЛИННОЙ УГЛЕРОДНОЙ
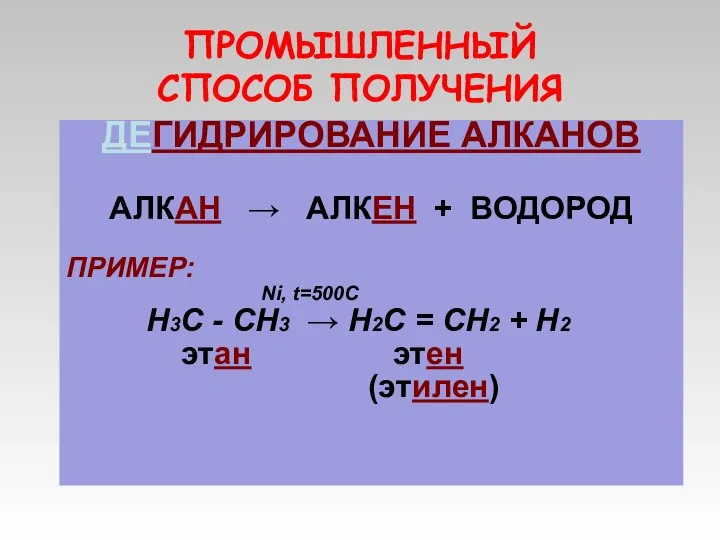
- 13. ПРОМЫШЛЕННЫЙ СПОСОБ ПОЛУЧЕНИЯ ДЕГИДРИРОВАНИЕ АЛКАНОВ АЛКАН → АЛКЕН + ВОДОРОД ПРИМЕР: Ni, t=500C Н3С - СН3
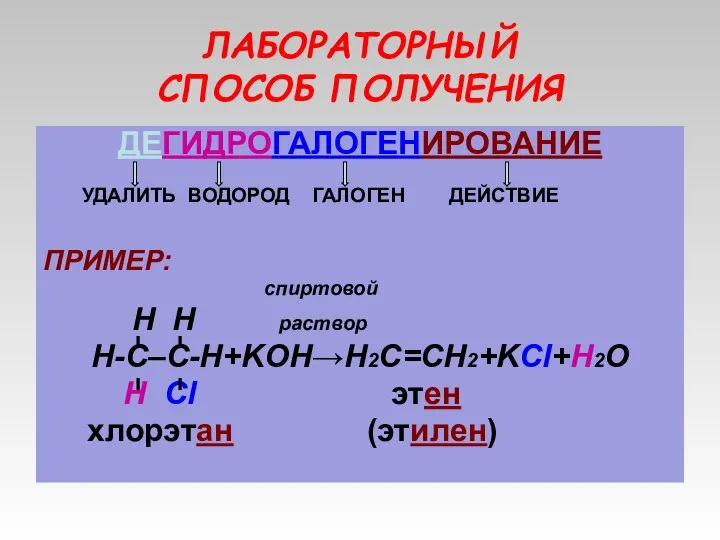
- 14. ЛАБОРАТОРНЫЙ СПОСОБ ПОЛУЧЕНИЯ ДЕГИДРОГАЛОГЕНИРОВАНИЕ УДАЛИТЬ ВОДОРОД ГАЛОГЕН ДЕЙСТВИЕ ПРИМЕР: спиртовой H H раствор Н-С–С-Н+KOH→Н2С=СН2+KCl+H2O Н Cl
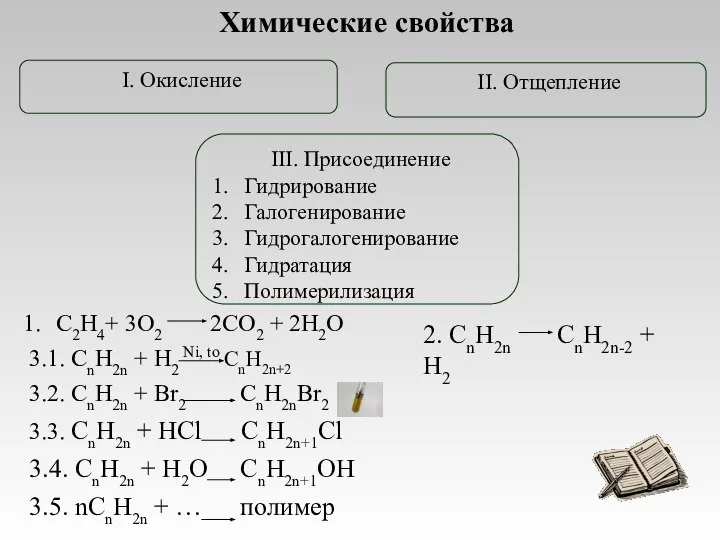
- 15. Химические свойства III. Присоединение Гидрирование Галогенирование Гидрогалогенирование Гидратация Полимерилизация
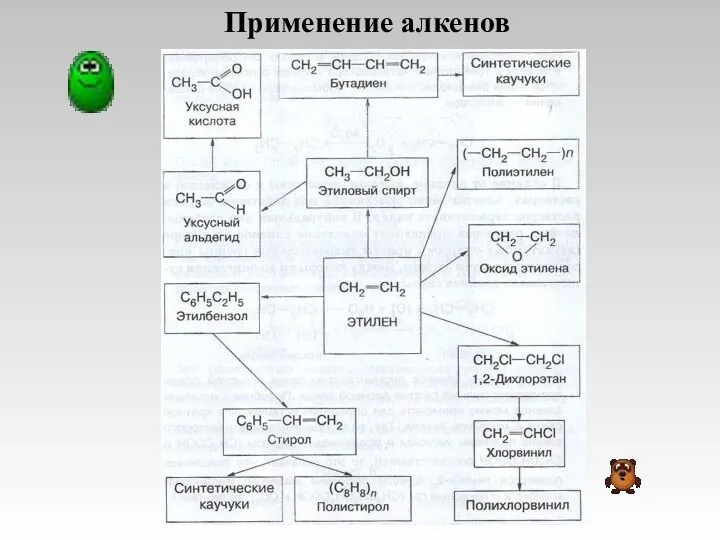
- 16. Применение алкенов
- 17. ЗАДАНИЕ 2. Тест (выполнить в тетрадях) 1. Алкены можно также назвать: а) этиленовыми углеводородами, б) олефиновыми
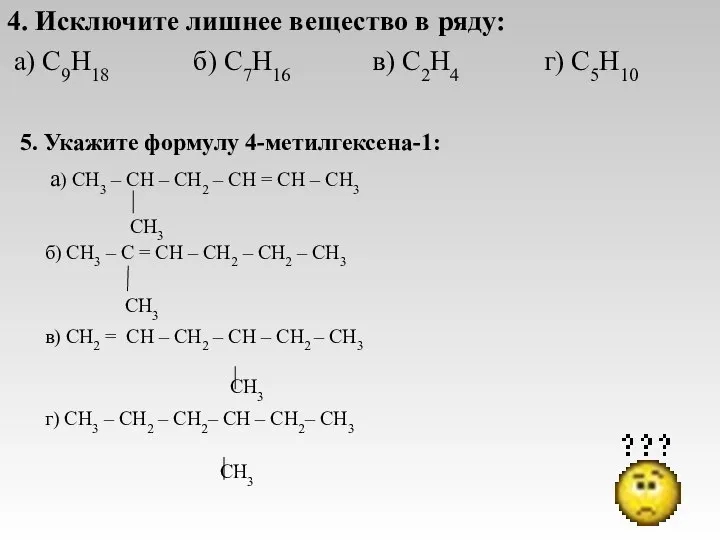
- 18. 4. Исключите лишнее вещество в ряду: а) C9H18 б) С7H16 в) C2H4 г) C5H10 5. Укажите
- 20. Скачать презентацию






 Характеристика кислорода как химического элемента и простого вещества
Характеристика кислорода как химического элемента и простого вещества Интеллектуальный турнир для старшеклассников Умножая таланты 2020
Интеллектуальный турнир для старшеклассников Умножая таланты 2020 Кислоты. Классификация кислот
Кислоты. Классификация кислот Кальций и его соединения
Кальций и его соединения Алифатические соединения. Тема № 6
Алифатические соединения. Тема № 6 Химический футбол на тему: Химия вокруг нас
Химический футбол на тему: Химия вокруг нас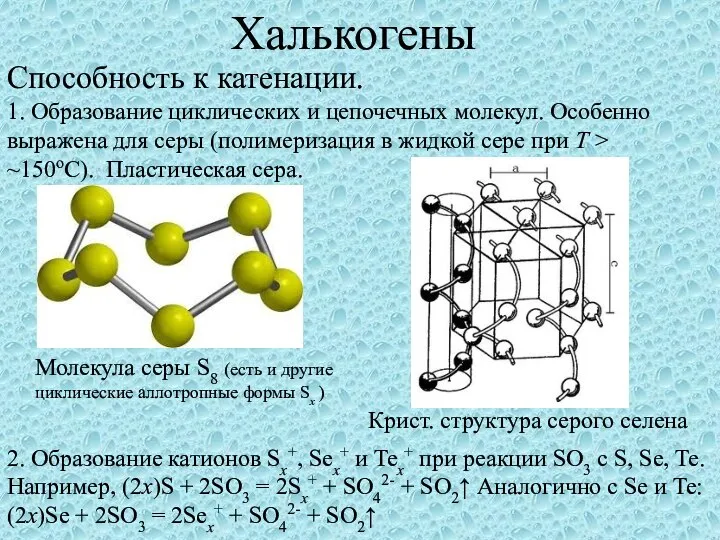 Халькогены. Способность к катенации
Халькогены. Способность к катенации Электролитическая диссоциация
Электролитическая диссоциация Презентация на тему Решение задач на смеси, сплавы, растворы
Презентация на тему Решение задач на смеси, сплавы, растворы  Кислород. Оксиды. Валентность
Кислород. Оксиды. Валентность Современные области применения изотопной продукции
Современные области применения изотопной продукции 10-4 (2)
10-4 (2) Коллоидная химия
Коллоидная химия Схема монооксигеназной цепи микросом
Схема монооксигеназной цепи микросом Классы неорганических веществ
Классы неорганических веществ Кристаллизация и десублимация
Кристаллизация и десублимация Формирование и контроль остаточных напряжений, возникающих под действием различных технологических операций
Формирование и контроль остаточных напряжений, возникающих под действием различных технологических операций Problem-solving. Test: real-time polymerase chain reaction
Problem-solving. Test: real-time polymerase chain reaction Относительная молекулярная масса вещества
Относительная молекулярная масса вещества Структура неорганических ионных соединений. Лекция 12
Структура неорганических ионных соединений. Лекция 12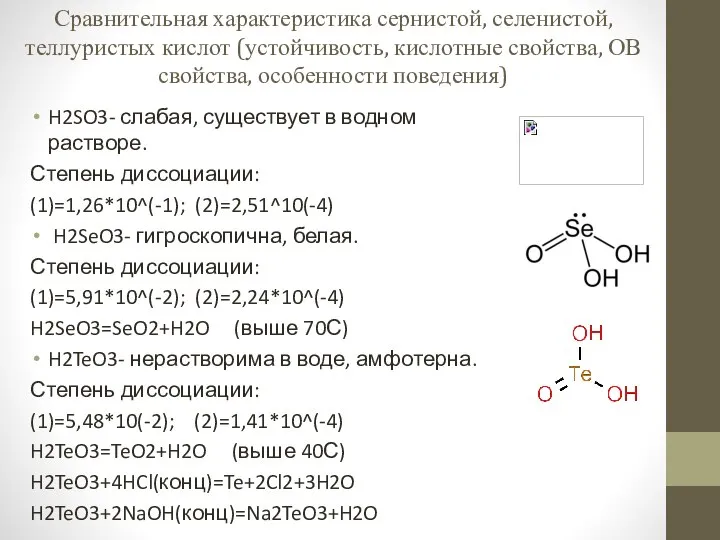 Сравнительная характеристика сернистой, селенистой, теллуристых кислот
Сравнительная характеристика сернистой, селенистой, теллуристых кислот Блеск и сила волос с точки зрения химии
Блеск и сила волос с точки зрения химии Методы отбора проб воды. Оформление и подготовка к анализу, протокол исследования воды, определение рН
Методы отбора проб воды. Оформление и подготовка к анализу, протокол исследования воды, определение рН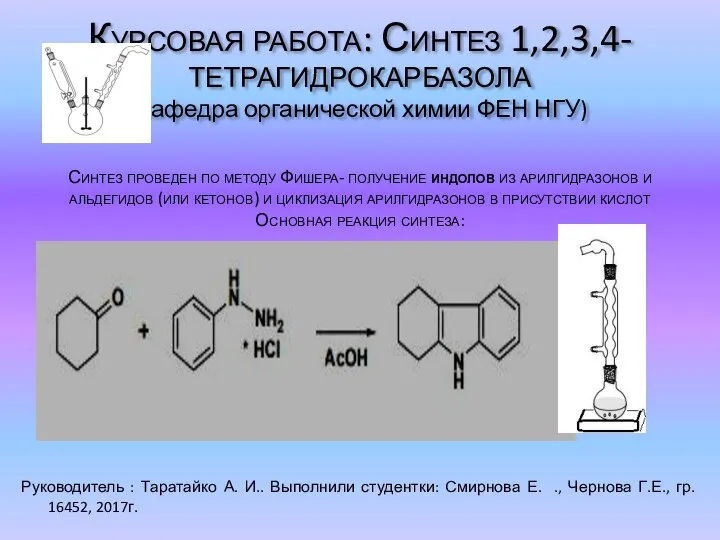 Синтез 1,2,3,4-тетрагидрокарбазола
Синтез 1,2,3,4-тетрагидрокарбазола Валентность. Определение валентности по формулам
Валентность. Определение валентности по формулам Соляная кислота
Соляная кислота Презентация на тему Генетическая связь между классами неорганических вещ-в
Презентация на тему Генетическая связь между классами неорганических вещ-в  Теория строения химических соединений
Теория строения химических соединений