Слайд 2Что такое магний?
Магний — элемент 2 группы (по старой классификации — главной группы и подгруппы второй

группы), третьего периода периодической системы химических элементов Д. И. Менделеева, с атомным номером 12. Обозначается символом Mg (лат. Magnesium). Простое вещество магний — лёгкий, ковкий металл серебристо-белого цвета.
Слайд 3Физические свойства магния
Физические свойства
Магний Mg — это щелочной металл. Серебристо-белый, относительно мягкий, пластичный, ковкий

металл. На воздухе покрыт оксидной пленкой. Сильный восстановитель.
Относительная молекулярная масса Mr = 24,305; относительная плотность для твердого и жидкого состояния d = 1,737; tпл = 648º C; tкип = 1095º C.
Слайд 4Химические свойства магния
1. Магний — сильный восстановитель. Поэтому он реагирует почти со всеми неметаллами:
1.1. Магний взаимодействует с

азотом при 780 — 800º С образуя нитрид магния: 3Mg + N2 = Mg3N2
1.2. Магний сгорает в кислороде (воздухе) при 600 — 650º С с образованием оксида магния: 2Mg + O2 = 2MgO
2. Магний активно взаимодействует со сложными веществами:
2.1. Магний реагирует с горячей водой. Взаимодействие магния с водой приводит к образованию гидроксида магния и газа водорода: Mg + 2H2O = Mg(OH)2↓ + H2↑
2.2. Магний взаимодействует с кислотами:
2.2.1. Магний реагирует с разбавленной соляной кислотой, при этом образуются хлорид магния и водород: Mg + 2HCl = MgCl2 + H2 ↑
Слайд 5Способ получения магния
1. В результате электролиза расплава хлорида магния образуются магний и хлор : MgCl2 = Mg↓ + Cl2↑
2. Нитрид магния разлагается при 700

— 1500º С образуя магний и азот: Mg3N2 = 3Mg + N2
3. Оксид магния легко восстанавливается углеродом при температуре выше 2000º С, образуя магний и угарный газ: MgO + C = Mg + CO
4. Оксид магния также легко восстанавливается кальцием при 1300º С с образованием магния и оксида кальция: MgO + Ca = CaO + Mg
Слайд 6Сплавы магния
Сплавы магния – это продукция металлургического производства, в которой основным элементом

является магний, а дополнительными элементами – легирующие добавки металлов и неметаллов, влияющие на свойства основного элемента. Главная отличительная особенность, обеспечивающая им широкое применение в промышленности – лёгкость материала (его высокая прочность при низкой плотности)
Слайд 7Маркировка сплавов магния
Отечественная промышленность маркирует магниевые сплавы на основе двухбуквенной маркировки с

дополнительными цифрами:
Литейные — МЛ1 – МЛ20
Деформируемые — МА1 – МА19
Жаропрочные магниевые сплавы ВМЛ1 – ВМЛ2
Слайд 8Интересные факты про магний
В 1808 году английский ученый Гемфри Дэви, анализируя белую

магнезию, расплавил ее, потом подверг электролизу и получил новый элемент, который был назван магнием. Точнее, Дэви получил амальгаму магния, а чистый металл впервые выделил Фарадей в 1833 году.
Магний является щелочноземельным металлом. Хотя он отсутствует в свободной чистой форме, его соединения встречаются в больших отложениях в виде магнезита, доломита и других минералов.
Магний является 8-м наиболее распространенным элементом в земной коре, а после железа, кислорода и кремния это 4-й наиболее распространенный элемент на Земле в целом составляет 13% массы нашей планеты.







 Щелочноземельные металлы
Щелочноземельные металлы Адамсит. Дигидрофенарсазинхлорид HN(C6H4)2AsCl
Адамсит. Дигидрофенарсазинхлорид HN(C6H4)2AsCl Основы материаловедения. Раздел 1
Основы материаловедения. Раздел 1 Природные смолы: канифоль, янтарь, сандарак (2)
Природные смолы: канифоль, янтарь, сандарак (2) Алгоритм названия органического соединения
Алгоритм названия органического соединения Сталь 12Х18Н10Т
Сталь 12Х18Н10Т Презентация на тему Подгруппа углерода и азота
Презентация на тему Подгруппа углерода и азота  3 Серная кислота
3 Серная кислота Калий. Общая информация
Калий. Общая информация Метиловый спирт
Метиловый спирт Дисперсные системы
Дисперсные системы Свойства металлов. Лекция №8
Свойства металлов. Лекция №8 Использование ИКТ в преподавании химии
Использование ИКТ в преподавании химии Методы повышения надежности. Резервирование сложных ХТС
Методы повышения надежности. Резервирование сложных ХТС Disinfection without Chlorine and Chemistry
Disinfection without Chlorine and Chemistry Презентация на тему Медь
Презентация на тему Медь  Применение солей
Применение солей Презентация на тему Растворение. Растворы (8 класс)
Презентация на тему Растворение. Растворы (8 класс)  Презентация на тему Производство аммиака
Презентация на тему Производство аммиака  Положение металлов в периодической системе Д.И. Менделеева. Физические свойства металлов
Положение металлов в периодической системе Д.И. Менделеева. Физические свойства металлов Химические свойства амфотерных оксидов и гидроксидов
Химические свойства амфотерных оксидов и гидроксидов Презентация на тему Кислород (9 класс)
Презентация на тему Кислород (9 класс)  gidroliz_soley (1)
gidroliz_soley (1) Гидролиз. Виды гидролиза
Гидролиз. Виды гидролиза Изучаем химию с Агатой Кристи
Изучаем химию с Агатой Кристи Презентация на тему Альдегиды и их свойства
Презентация на тему Альдегиды и их свойства 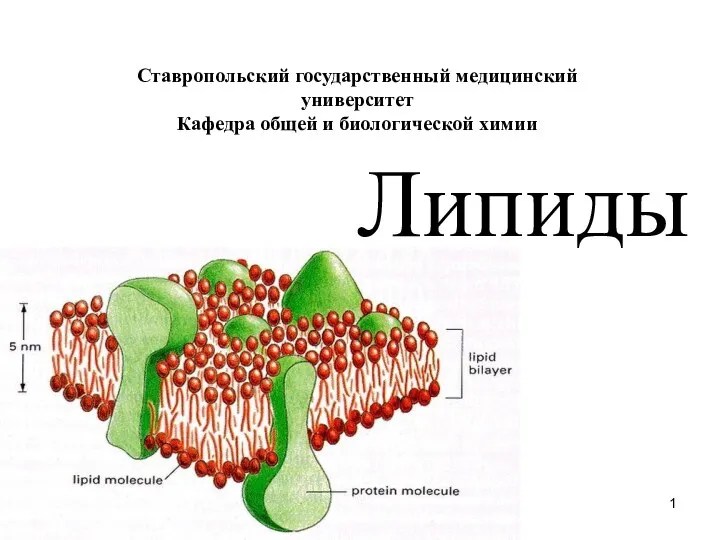 Липиды
Липиды Алюминий
Алюминий