Слайд 2План урока:
1.Анализ контрольной работы.
Работа над ошибками.
2.Металлы-простые вещества ,их свойства.
3.Неметаллы-простые вещества,

их свойства.
4.Применение простых веществ-металлов и неметаллов.
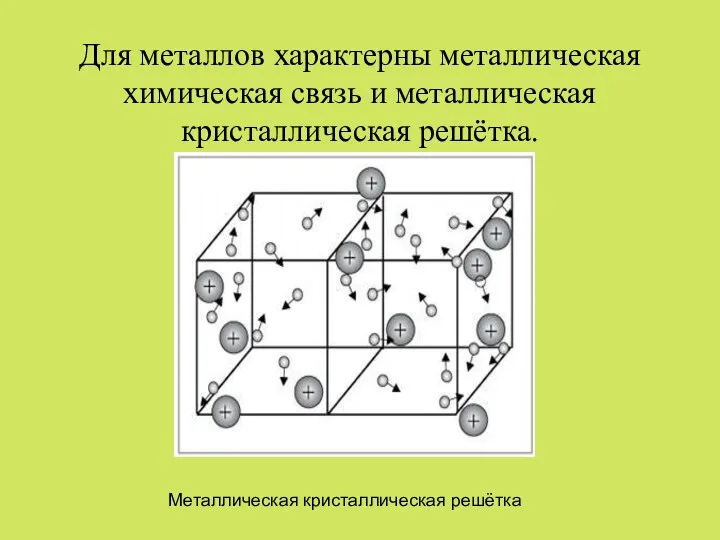
Слайд 4Для металлов характерны металлическая химическая связь и металлическая кристаллическая решётка.
Металлическая кристаллическая решётка
Слайд 5Большинство встречающихся в природе простых веществ - металлы. Некоторые из них мы

часто встречаем в повседневной жизни, так что знаем, как они выглядят и для чего их можно использовать.
Большое количество предметов, найденных при археологических раскопках, свидетельствуют о том, что наши далекие предки использовали металлы для создания простых орудий труда и украшений.
Слайд 6При комнатной температуре металлы - твердые вещества, за исключением ртути (она жидкая).
Большинство

металлов серебристо-серого цвета с разными оттенками, за исключением золота и меди.
Все металлы имеют характерный блеск, называемый металлическим блеском.
Металлы хорошо проводят тепло и электричество.
Металлы различаются по твердости.
Металлы сильно различаются по температуре плавления.
Металлы гибкие и ковкие.
Металлы значительно различаются по плотности, например: плотность натрия 0,97 г/см3, а плотность платины 21,45 г/см3.
В металлургии металлы делят на черные (железо, марганец, хром) и цветные (все остальные металлы).
Слайд 7Физические свойства металлов
металлический блеск
прочность, пластичность, упругость
электропроводность
теплопроводность.
ковкость ,пластичность

Слайд 8 1. Какие металлы использовались в древние и средние века?
2.

Какие металлы называют черными, какие цветными?
3. Самый легкий металл?
4.Самый твердый металл.
5.Какой металл придает нашей крови красный цвет?
6. Самый тяжелый металл
7.Металл- жидкость.
8.Самый используемый металл в мире.
Слайд 91. (Fe, Cu, Sn, Pb, Hg, Au, Ag)
2. (Черные - железо и

его сплавы, цветные – Al, Cu, Pb, Zn, Sn, Ag)
3. (Литий)
4. (Хром)
5. (Железо)
6. (Осмий)
7 (Ртуть)
8. (Железо)
Слайд 11Металлический блеск наиболее выражен у серебра . Его используют в создании зеркал.

Слайд 12Свойство электропроводности ярко выражено у меди

Слайд 13А теплопроводность меди используется при изготовлении посуды

Слайд 14Алюминий –лёгкий металл. Его используют для создания «крылатых» сплавов.

Слайд 15Свинец – очень тяжелый металл, его используют как балласт при погружении в

воду.
Слайд 16Температура плавления разных металлов довольно сильно различается. Так, ртуть плавится при -39

°С, а платина - не ниже +1735 °С.
Слайд 17Свойство пластичности наиболее ярко выражено у золота.

Слайд 19Медь – металл с красноватым блеском.

Слайд 21Многие предметы, которыми мы ежедневно пользуемся, сделаны из металлов.

Слайд 22Без металлов невозможен технический прогресс

Слайд 24 Все простые вещества делятся на металлы и неметаллы.
Примеры неметаллов:
водород,
кислород,
азот,
сера,
фосфор,
углерод,
иод,
бром,
хлор.
Неметаллы -

это химические элементы, которые образуют простые вещества, не обладающие свойствами, характерными для металлов.
(Графит (одна из форм углерода) - единственный неметалл, проводящий электрический ток.)
Слайд 25Кислород, водород – пример газообразных бесцветных неметаллов

Слайд 26Хлор (как и фтор) – окрашенные газообразные неметаллы.

Слайд 27При растворении хлора в воде получается хлорная вода

Слайд 28Бром – жидкость красно-бурого цвета

Слайд 29При растворении брома в воде получается бромная вода

Слайд 30Большинство неметаллов имеют твёрдое агрегатное состояние
Сера – кристаллическое вещество жёлтого цвета

Слайд 33Большинство неметаллов нерастворимы или малорастворимы в воде
Уголь

Слайд 36Для неметаллов характерно явление аллотропии
Способность атомов одного химического элемента образовывать несколько

простах веществ называют аллотропией , а эти простые вещества –аллотропными видоизменениями или модификациями.
Сравните свойства простых веществ – кислорода и озона, алмаза и графита.
Слайд 37Существует небольшая группа встречающихся в природе элементов, называемых металлоидами.
Металлоиды:
бор - В,
кремний -

Si,
германий - Ge,
мышьяк - As,
теллур - Те,
сурьма – Sb.
Они обладают промежуточными между металлами и неметаллами свойствами.
В одних условиях они проявляют свойства, характерные для металлов, в других - для неметаллов.



































 Аминокислоты. Химические и физические свойства
Аминокислоты. Химические и физические свойства Композиционные материалы. Структура и свойства
Композиционные материалы. Структура и свойства Белки́ (протеины, полипепти́ды)
Белки́ (протеины, полипепти́ды) Обобщение. Неметаллы
Обобщение. Неметаллы Презентация на тему Производство аммиака
Презентация на тему Производство аммиака  Теория строения вещества. Межмолекулярные взаимодействия. Водородная связь. Специфические взаимодействия
Теория строения вещества. Межмолекулярные взаимодействия. Водородная связь. Специфические взаимодействия Дисперсные системы
Дисперсные системы Основные химические законы
Основные химические законы Белки
Белки Химия һәм сәламәт яшәү рәвеше
Химия һәм сәламәт яшәү рәвеше Натуральный каучук
Натуральный каучук Алканы в торфянисто-подзолисто-глееватых почвах Габов Д.Н., Безносиков В.А., Кондратенок Б.М., Груздев И.В.
Алканы в торфянисто-подзолисто-глееватых почвах Габов Д.Н., Безносиков В.А., Кондратенок Б.М., Груздев И.В. Заманауи косметика биотехнологиясы
Заманауи косметика биотехнологиясы Опыт разработки учебно-методического комплекса Химия
Опыт разработки учебно-методического комплекса Химия Концентрированная серная кислота
Концентрированная серная кислота Презентация по Химии "Химические элементы металлы и здоровье человека"
Презентация по Химии "Химические элементы металлы и здоровье человека"  Презентация на тему Альдегиды
Презентация на тему Альдегиды  Отчёт по ПП 03.01. Лаборант химического анализа. Подготовка химической посуды, приборов и лабораторного оборудования
Отчёт по ПП 03.01. Лаборант химического анализа. Подготовка химической посуды, приборов и лабораторного оборудования Эвапориты. Химические осадки из ионных растворов
Эвапориты. Химические осадки из ионных растворов Азотосодержащие соединения: Амины. Аминокислоты. Белки
Азотосодержащие соединения: Амины. Аминокислоты. Белки Химическая связь
Химическая связь Генетическая связь между классами неорганических веществ
Генетическая связь между классами неорганических веществ Скорость химической реакции
Скорость химической реакции Презентация на тему Основные классы неорганических соединений
Презентация на тему Основные классы неорганических соединений  Вермикулит. Технические характеристики
Вермикулит. Технические характеристики Кислород (Лекция 7)
Кислород (Лекция 7) Разложение отходов. 11 класс
Разложение отходов. 11 класс Строение атома. Экзаменационные вопросы
Строение атома. Экзаменационные вопросы