Слайд 2Введение
Цель: исследование физико-химических свойств щавелевой кислоты.
Задачи:
1. Подбор и освоение литературы по теме

курсовой работы
2. Изучение физико-химических свойств щавелевой кислоты
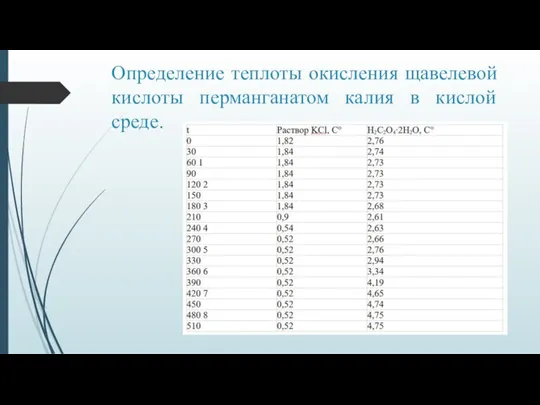
Слайд 3Определение теплоты окисления щавелевой кислоты перманганатом калия в кислой среде.
Слайд 4
Температурная кривая процесса растворения KCl
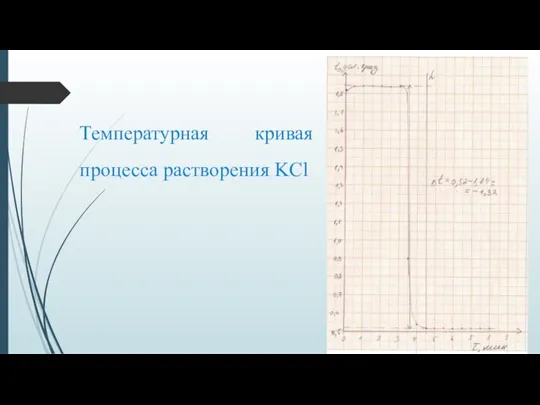
Слайд 5Температурная кривая процесса растворения H2C2O4∙2H2O

Слайд 6На основе графика для процесса растворения KCl нашли:
Изменение температуры:
∆t = 0,52 —

1,84 = - 1,32 усл.град. (∆t < 0)
Теплоемкость калориметрической системы Скс:
Скс= ∆solHKCl / ∆t
∆solHKCl = 0,7067 + 3,01*10-3*(18,4-25) = 0,69 кДж
Cкс = -0,69/ - 1,32 = 0,52 кДж
На основе графика для процесса растворения H2C2O4∙2H2O нашли:
∆t1 = 4,65 — 2,79 = 1,86 усл.град
∆H = (M/m)*Ckc* ∆t1
M — молярная масса щавелевой кислоты (г/моль), m — масса окисленной щавелевой кислоты (г)
∆H = (90/0,18)*0,52*1,86 = 483,6 кДж
Слайд 7Определение степени электролитической диссоциации криоскопическим методом
Степень диссоциации: 0,55

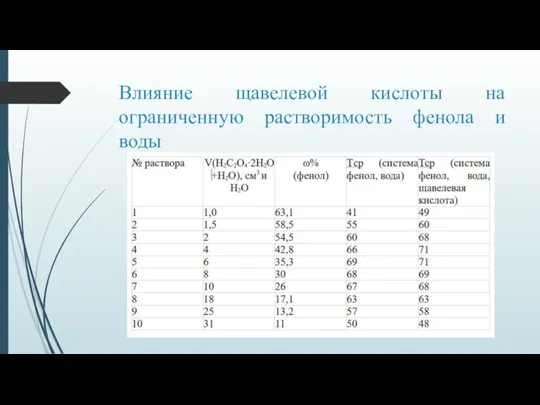
Слайд 8Влияние щавелевой кислоты на ограниченную растворимость фенола и воды
Слайд 9Диаграмма растворимости системы фенол-вода+H2C2O4∙2H2О и диаграмма растворимости системы фенол-вода
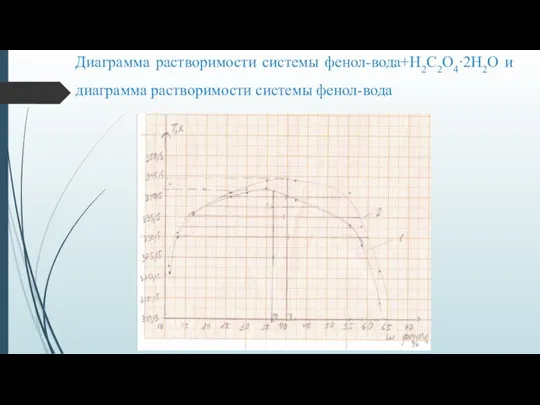
Слайд 10Определяем графически критическую температуру расслоения Tкр системы фенол – вода+ H2C2O4∙2H2О по

правилу Алексеева.
Tкр=344,15 К
Определяем состав системы, отвечающий Ткр
ωкр=40 %
Абсолютная ошибка: ∆Ткр = 4,75, ∆ωкр(Н2О) = 5,4
Относительная ошибка: 1,4% и 15,6% соответственно
Слайд 11Выводы
1) Исследовали физико-химические свойства щавелевой кислоты.
2) При определении теплоты окисления при комнатной

температуре получилась со знаком плюс, так как процесс является эндотермическим.
3) Криоскопический метод можно использовать для определения степени диссоциации электролита, так как ошибка измерений составила 20%. ?
4) В ходе исследования влияния щавелевой кислоты на ограниченную растворимость фенола и воды выяснили, что щавелевая кислота увеличивает площадь гетерогенной области, так как Ткр для системы фенол — раствор H2C2O4∙2H2О равна 344,15, а Ткр для фенол — вода — 341,15, и критический состав смещается в сторону содержания воды.










 Презентация на тему Окислительно-восстановительные реакции
Презентация на тему Окислительно-восстановительные реакции  Презентация на тему Сложные эфиры. Жиры
Презентация на тему Сложные эфиры. Жиры  Пентоза - відновлювальна сировина для синтезу фуранових сполук
Пентоза - відновлювальна сировина для синтезу фуранових сполук Дождь из облака
Дождь из облака По страницам истории российской химической науки
По страницам истории российской химической науки Явление хемилюменисценции
Явление хемилюменисценции Сложные вещества кислоты
Сложные вещества кислоты Что изучает химия?
Что изучает химия? Окислительно-восстановительные реакции. Классификация ОВР
Окислительно-восстановительные реакции. Классификация ОВР Термодинамика. Основные понятия и законы. Особенности термодинамики живых систем
Термодинамика. Основные понятия и законы. Особенности термодинамики живых систем Аналитический обзор по теме Процесс разложения аммиака
Аналитический обзор по теме Процесс разложения аммиака Презентация на тему Игра «Путешествие в страну Атомолия»
Презентация на тему Игра «Путешествие в страну Атомолия»  Белки
Белки Углеводороды. Общие знания
Углеводороды. Общие знания Ca КАЛЬЦИЙ
Ca КАЛЬЦИЙ Органическая химия. Йенс Якоб Берцелиус (1779 - 1848)
Органическая химия. Йенс Якоб Берцелиус (1779 - 1848) Презентация на тему Альдегиды (10 класс)
Презентация на тему Альдегиды (10 класс)  Щелочные металлы
Щелочные металлы Жесткость воды и способы ее устранения
Жесткость воды и способы ее устранения Презентация на тему Валентность и степень окисления (8 класс)
Презентация на тему Валентность и степень окисления (8 класс)  Основной государственный экзамен. Химия 2022. Задание 2
Основной государственный экзамен. Химия 2022. Задание 2 Своя игра. Атомы
Своя игра. Атомы ИКТ как средство реализации проблемного обучения на уроках химии
ИКТ как средство реализации проблемного обучения на уроках химии Алюминий. Применение
Алюминий. Применение Хлороводород и соляная кислота
Хлороводород и соляная кислота Химические свойства оксидов
Химические свойства оксидов Химическая связь. Строение вещества
Химическая связь. Строение вещества Презентация на тему Основания и их классификация
Презентация на тему Основания и их классификация