Содержание
- 2. Количество металлов среди всех химических элементов
- 3. Расположение элементов – металлов в ПСХЭ: 1 группа главная подгруппа – щелочные металлы 2 группа главная
- 4. Большая часть металлов существует в природе в виде минеральных образований - руд Некоторые неактивные металлы существуют
- 5. Металлы – это химические элементы, атомы которых отдают электроны внешнего ( предвнешнего) электронного слоя, превращаясь в
- 6. Главные особенности элементов металлов. Число валентных электронов (1-3 ). Сравнительно большие радиусы атомов. Небольшие значения электроотрицательности
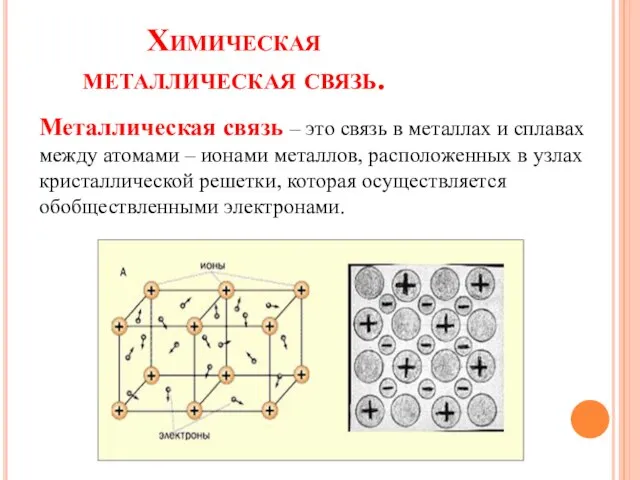
- 7. Химическая металлическая связь. Металлическая связь – это связь в металлах и сплавах между атомами – ионами
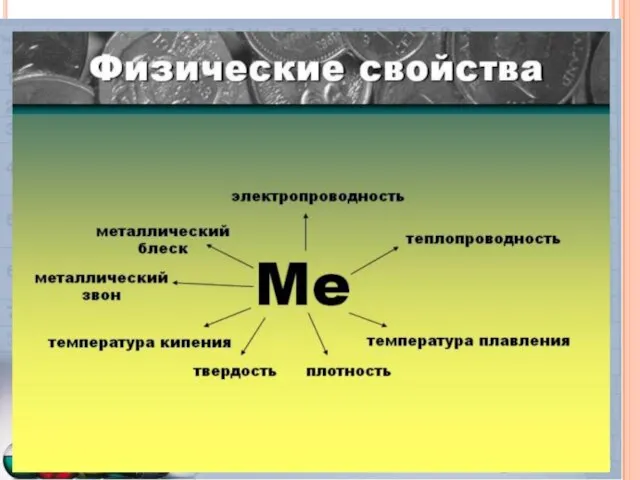
- 8. Металлы – простые вещества. Все металлы обладают общими физическими свойствами: Пластичность – смещение слоев ионов под
- 10. Взаимодействие металлов с галогенами o +2 -1 2Са + Н 2О → 2Сa(ОН) o +3 -1
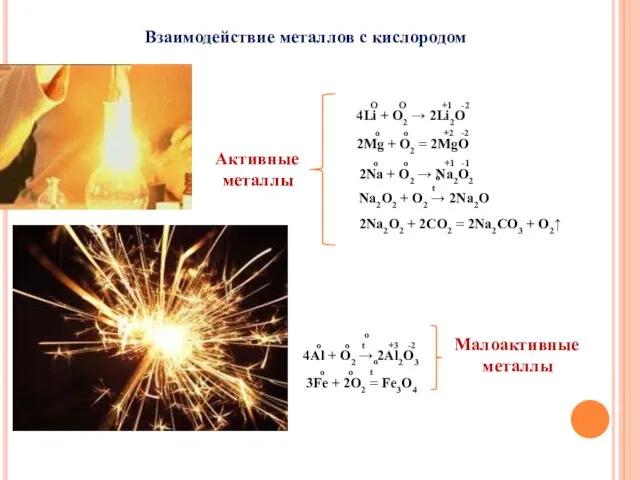
- 11. Взаимодействие металлов с кислородом Активные металлы O O +1 -2 4Li + O2 → 2Li2O o
- 12. o +1 -1 +2 -1 o Zn + 2HCl → ZnCl2 + H2 Взаимодействие металлов с
- 13. Химические свойства металлов 1. Все металлы проявляют только восстановительные свойства 2. Атомы металлов легко отдают электроны
- 14. Применение металлов
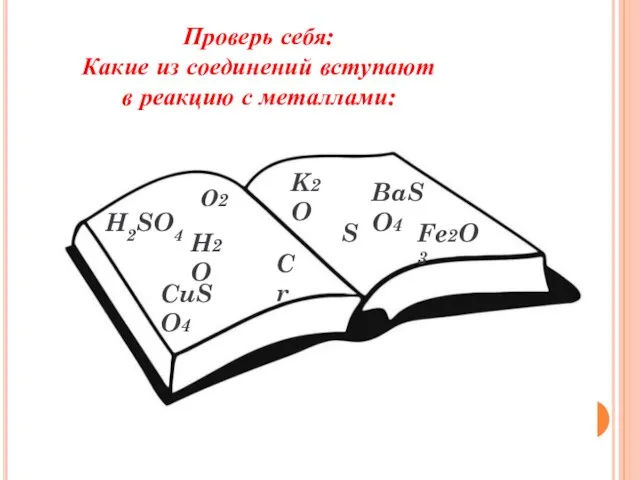
- 15. Проверь себя: Какие из соединений вступают в реакцию с металлами: О2 K2O CuSO4 H2O S BaSO4
- 17. Скачать презентацию










 Презентация на тему Знаки химических элементов
Презентация на тему Знаки химических элементов  Предмет биоорганической химии. Лекция 1
Предмет биоорганической химии. Лекция 1 Периодическая система химических элементов Д.И. Менделеева. Знаки химических элементов
Периодическая система химических элементов Д.И. Менделеева. Знаки химических элементов Химические реакции
Химические реакции Химическая промышленность
Химическая промышленность Строение атома
Строение атома Химия в загадках
Химия в загадках Эфиры. 10 класс
Эфиры. 10 класс Твердые материалы для художественно-оформительских работ
Твердые материалы для художественно-оформительских работ Рівноваги у розчинах електролітів
Рівноваги у розчинах електролітів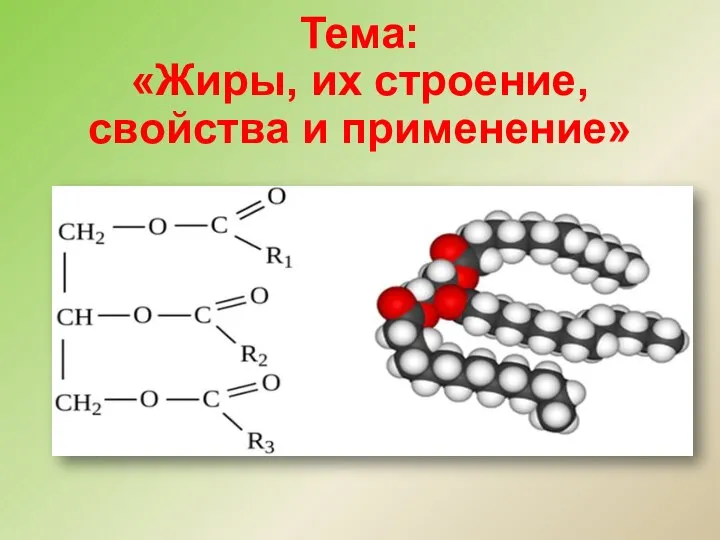 Жиры, их строение, свойства и применение
Жиры, их строение, свойства и применение Кислоты
Кислоты Природные источники углеводородов. Природный и попутный нефтяные газы. Нефть. Каменный уголь
Природные источники углеводородов. Природный и попутный нефтяные газы. Нефть. Каменный уголь Соли в природе. Реакции с участием солей. Модуль 2. Лекция 2.1
Соли в природе. Реакции с участием солей. Модуль 2. Лекция 2.1 Физика Доклад
Физика Доклад Металлургия
Металлургия Введение. Тренажер
Введение. Тренажер Моделирование состава биоплёночного материала
Моделирование состава биоплёночного материала Презентация на тему Эфиры и жиры
Презентация на тему Эфиры и жиры  Роль М.В. Ломоносова и Дж. Дальтона в создании атомно-молекулярного учения
Роль М.В. Ломоносова и Дж. Дальтона в создании атомно-молекулярного учения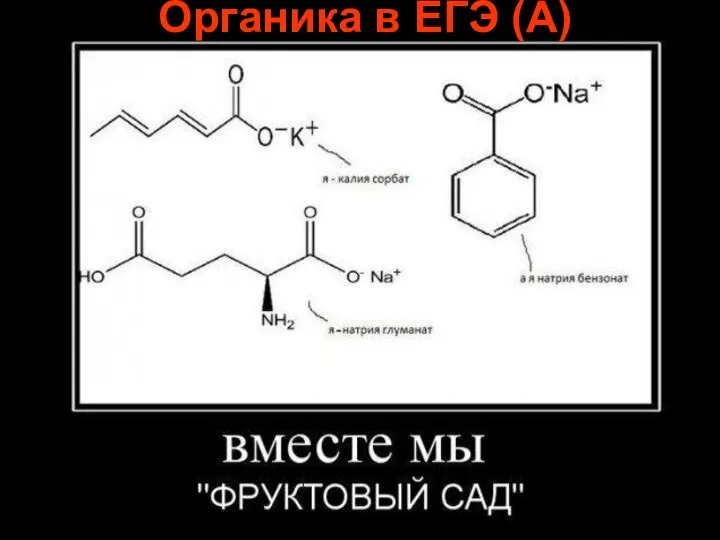 Органика в ЕГЭ (А)
Органика в ЕГЭ (А) Презентация на тему Теллур
Презентация на тему Теллур  Витамины. Классификация витаминов
Витамины. Классификация витаминов Галогены. Их значение в жизни человека
Галогены. Их значение в жизни человека Химиялық есептердің кеңістіктік шешімдері
Химиялық есептердің кеңістіктік шешімдері Презентация на тему Химические уравнения. Реакции обмена
Презентация на тему Химические уравнения. Реакции обмена  Модель химического образования на основе технологического подхода. Методическая система учителя химии
Модель химического образования на основе технологического подхода. Методическая система учителя химии Аммиак. Состав вещества
Аммиак. Состав вещества