Содержание
- 7. Разработка методики качественного определения катионов меди и никеля в растворах (в пробирках)
- 8. Получение гексацианоферрата(II) меди(II) из тетраамминмеди(II) 1 – исходный 10 % раствор сульфата меди(II); 2 – гидроксид
- 9. Образование гексацианоферратов и аммиакатов в смесях модельных растворов СuSO4 и NiSO4
- 10. Разработка методики качественного определения катионов меди и никеля в растворах (капельный метод анализа)
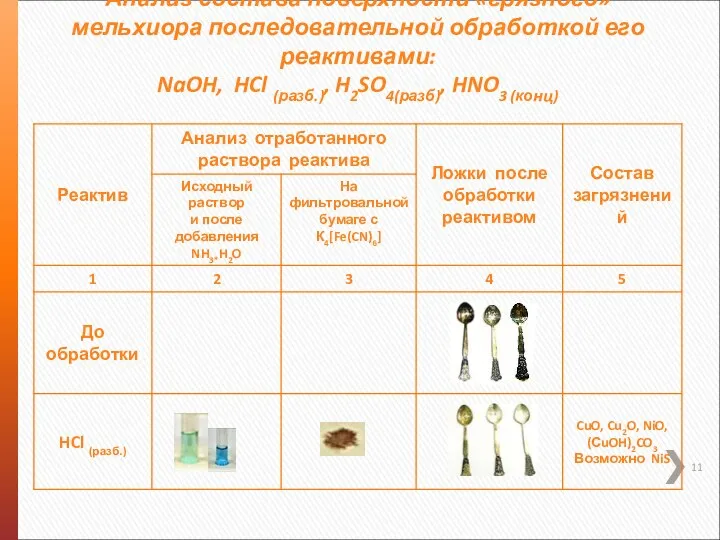
- 11. Анализ состава поверхности «грязного» мельхиора последовательной обработкой его реактивами: NaOH, HCl (разб.), H2SO4(разб), HNO3 (конц)
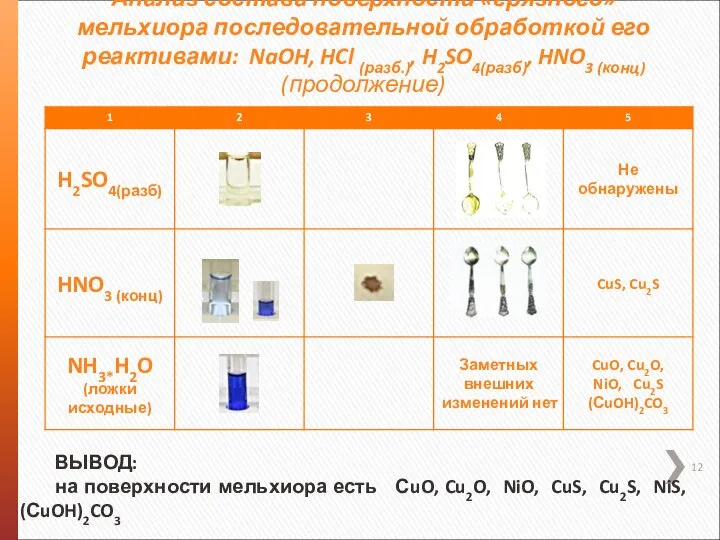
- 12. Анализ состава поверхности «грязного» мельхиора последовательной обработкой его реактивами: NaOH, HCl (разб.), H2SO4(разб), HNO3 (конц) (продолжение)
- 13. Способ очистки мельхиора: «прокипятить изделие 15-20 минут в алюминиевой посуде с раствором питьевой соды (вариант —
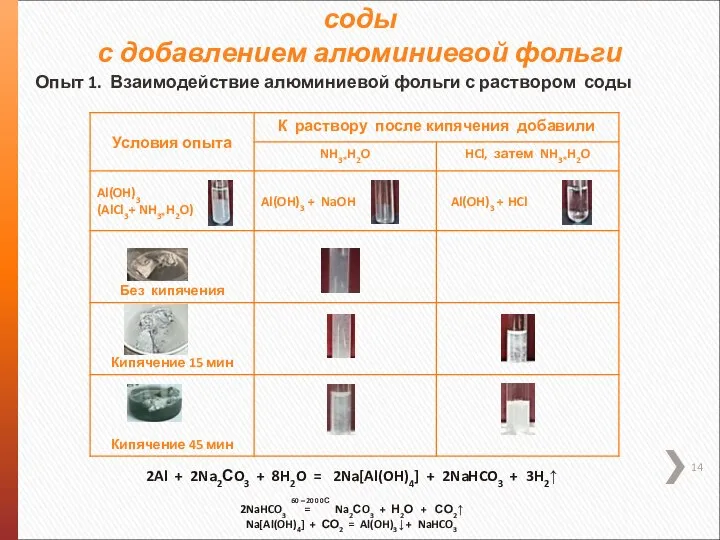
- 14. Очистка мельхиора кипячением в растворе соды с добавлением алюминиевой фольги Опыт 1. Взаимодействие алюминиевой фольги с
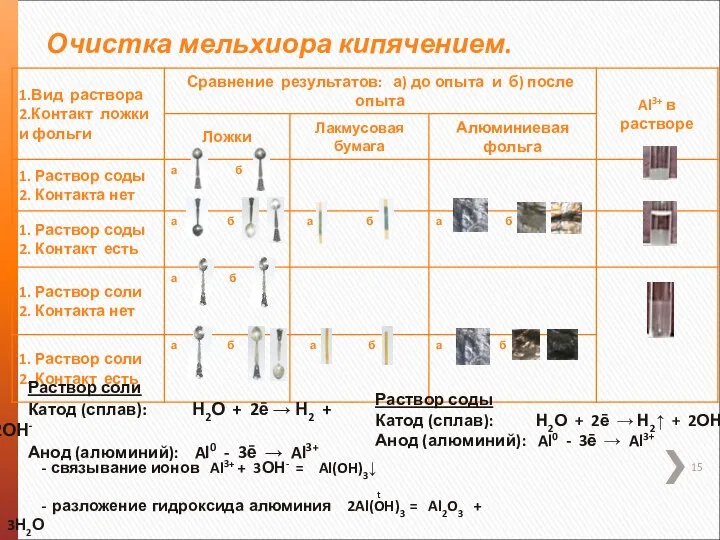
- 15. Очистка мельхиора кипячением. Раствор соли Катод (сплав): Н2О + 2ē → Н2 + 2ОН- Анод (алюминий):
- 16. Выводы: Медные сплавы обладают набором уникальных свойств, позволяющих широко использовать их в народном хозяйстве. Мельхиор при
- 18. Скачать презентацию






 Основные понятия химической термодинамики
Основные понятия химической термодинамики Генетическая связь между классами неорганических соединений
Генетическая связь между классами неорганических соединений Получение гидроген хлорида
Получение гидроген хлорида Самородные металлы
Самородные металлы Применение центрифугирования
Применение центрифугирования Растворы. Типы растворов. Способы выражения концентрации растворов
Растворы. Типы растворов. Способы выражения концентрации растворов Обратимость химических реакций. Химическое равновесие
Обратимость химических реакций. Химическое равновесие Викторина Что это?
Викторина Что это? Изменения, происходящие с веществами. Физические явления в химии
Изменения, происходящие с веществами. Физические явления в химии Общая характеристика нефти и газа
Общая характеристика нефти и газа Bool-doser team
Bool-doser team Растворение +СО2 + в +Н2О. Агрегатное состояние вещества
Растворение +СО2 + в +Н2О. Агрегатное состояние вещества Органические вещества. 9 класс
Органические вещества. 9 класс Свойства радиоактивных элементов
Свойства радиоактивных элементов Определение площади поверхности и пористости материалов методом сорбции газов
Определение площади поверхности и пористости материалов методом сорбции газов Основания. Структурная формула
Основания. Структурная формула Белки
Белки Алканы
Алканы Синтез оксида меди и йодида меди для формирования буферных слоев для ГОНП
Синтез оксида меди и йодида меди для формирования буферных слоев для ГОНП Азот
Азот Презентация на тему Алкадиены: строение, номенклатура, гомологи, изомерия
Презентация на тему Алкадиены: строение, номенклатура, гомологи, изомерия  Logo кроссворд первоначальные понятия. 8 класс
Logo кроссворд первоначальные понятия. 8 класс Презентация на тему Полимеразная цепная реакция
Презентация на тему Полимеразная цепная реакция  Циклические эфиры (окиси)
Циклические эфиры (окиси) Презентация на тему Обратимость химических реакций. Химическое равновесие
Презентация на тему Обратимость химических реакций. Химическое равновесие  В1 витамині
В1 витамині смеси
смеси Идентификация органических соединений
Идентификация органических соединений