Слайд 2Что такое простое вещество?
Вещество , образованное химическими элементами
Вещество, образованное атомами химических элементов
Вещество,

образованное атомами одного химического элемента
Вещество, образованное атомами разных химических элементов.
Слайд 3В каком ряду расположены только вещества
поваренная соль, сахар, свеча
вода, железо, сера
медь, гвоздь,

кислород
кирпич, пищевая сода, керамический стакан.
Слайд 4Верны ли следующие суждения?
А) Вещество - это то, из чего состоит физическое

тело.
В) Химический элемент - это определенный вид атомов.
Верно только А
Верно только В
Верны оба суждения
Оба суждения неверны.
Слайд 5Тело:
Графит
Полиэтилен
Свинец
Пробирка

Слайд 6Вещество:
Медная проволока
Медная монета
Медная пластина
Медь

Слайд 7Простое вещество:
Водород
Углекислый газ
Сахар
Поваренная соль

Слайд 8Сложное вещество
Фосфор
Крахмал
Сера
Медь

Слайд 9Говорят о водороде, как о простом веществе:
Водород – самый легкий газ
Порядковый номер

водорода в Периодической таблице-1
Водород входит в состав воды
Водород входит в состав кислоты
Слайд 10Говорят о меди как о химическом элементе
Медь не реагирует с соляной кислотой
Медь

окисляется при нагревании
Медная проволока
Медь входит в состав медного купороса
Слайд 11Структура ОГЭ по химии
Экзаменационная работа по химии состоит из 2 частей, включающих в

себя 24 задания:
Часть 1 содержит 19 заданий с кратким ответом. Максимальное количество баллов — 24.
Часть 2 содержит 3 задания с развернутым ответом. Это задание на расстановку коэффициентов методом электронного баланса в заданном уравнении, цепочка превращений из трех неорганических реакций и расчетная задача. Максимальный балл — 10.
В Части 2 присутствуют 2 экспериментальных задания. Сначала необходимо выполнить задание 23: записать уравнения реакций и описать предполагаемые качественные признаки превращений. Затем следует изучить инструкцию и сообщить организатору в аудитории о своей готовности приступить к выполнению самого эксперимента (задание 24). Максимальный балл — 6.
На выполнение всей экзаменационной работы по химии отводится 3 часа (180 минут).
Слайд 12Разбалловка такая:
5 выставляется при получении 31-40 баллов.
4 выставляется при получении 21-30 баллов.
3

выставляется при получении 10-20 баллов.
Если у вас меньше 10 баллов, вы не сдали экзамен.
Слайд 13Строение атома. Строение электронных оболочек первых 20 элементов Периодической системы Д.И. Менделеева.
Тема

1.
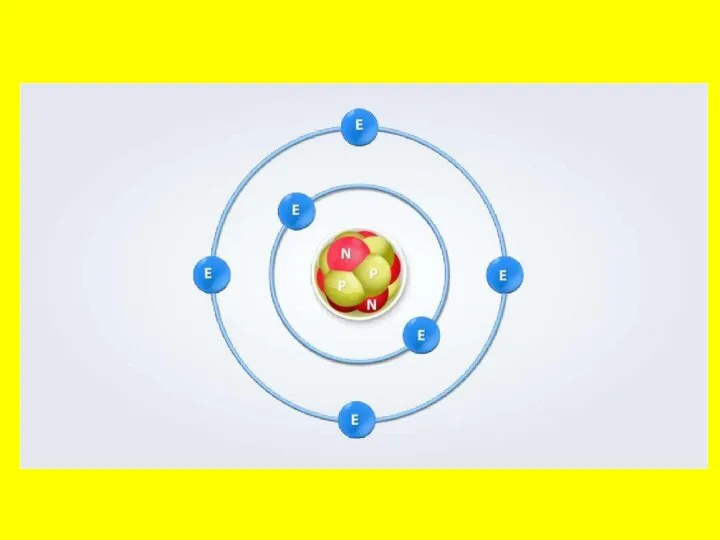
Слайд 15Атом — это мельчайшая, электронейтральная, химически неделимая частица вещества, состоящая из положительно заряженного

ядра и отрицательно заряженной электронной оболочки.
Слайд 16При этом электроны двигаются довольно хаотично. Совокупность электронов, которые двигаются вокруг ядра,

называется электронной оболочкой.
Атомное ядро — массивное и положительно заряженное, расположено в центральной части атома. Структура ядра довольно сложна, и изучается в ядерной физике. Основные частицы, из которых оно состоит — протоны и нейтроны. Они связаны ядерными силами (сильное взаимодействие).
Слайд 17Рассмотрим основные характеристики протонов, нейтронов и электронов:

Слайд 18И — самое главное. Периодическая система химических элементов, структурированная Дмитрием Ивановичем Менделеевым,

подчиняется простой и понятной логике: номер атома — это число протонов в ядре этого атома.
Следовательно, заряд ядра Z равен числу протонов, т.е. номеру атома в Периодической системе химических элементов.
Слайд 19Атом — это электронейтральная частица, следовательно, число протонов равно числу электронов: Ne = Np =

Z.
Масса атома (массовое число A) примерно равна суммарной массе крупных частиц, которые входят в состав атома — протонов и нейтронов. Поскольку масса протона и нейтрона примерно равна 1 атомной единице массы, можно использовать формулу:
M = Np + Nn
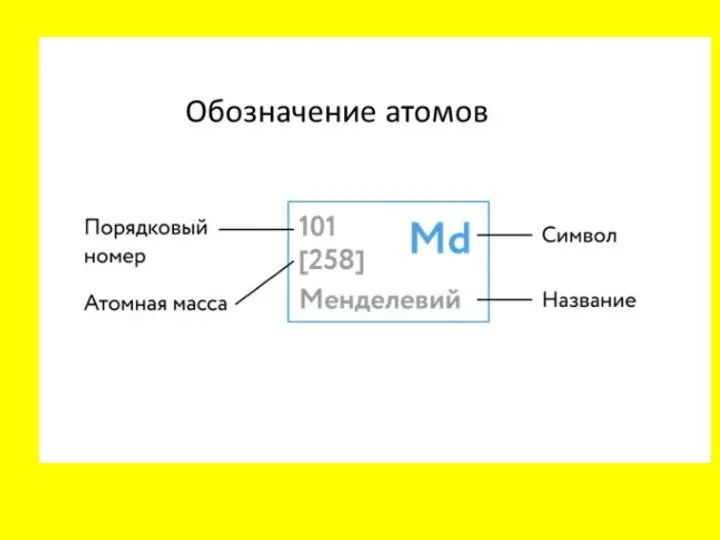
Слайд 20Массовое число указано в Периодической системе химических элементов в ячейке каждого элемента.

Слайд 21Важно
При решении задач ЕГЭ массовое число всех атомов, кроме хлора, округляется до

целого по правилам математики. Массовое число атома хлора в ЕГЭ принято считать равным 35,5.
Слайд 22Таким образом, рассчитать число нейтронов в атоме можно, вычтя из массового числа

номер атома: Nn = M – Z.
В Периодической системе собраны химические элементы — атомы с одинаковым зарядом ядра. Однако, может ли меняться у этих атомов число остальных частиц? Вполне. Например, атомы с разным числом нейтронов называют изотопами данного химического элемента. У одного и того же элемента может быть несколько изотопов.
Слайд 23У изотопов одного элемента массовое число одинаковое или разное?
У изотопов одного элемента

число протонов одинаковое или разное?
Слайд 24Разновидности атомов одного химического элемента, имеющие разные атомные массы, называют изотопами. Изотопы

— разновидности атомов с одинаковым числом протонов в ядре (зарядом ядра), но разным числом нейтронов. Значит, изотопы отличаются только числом нейтронов.
Слайд 25Химические свойства атомов определяются строением электронной оболочки и зарядом ядра. Таким образом, химические

свойства изотопов одного элемента практически не отличаются.
Поскольку атомы одного элемента могут существовать в форме разных изотопов, в названии часто указывается массовое число, например, хлор-35, и принята такая форма записи атомов:
Слайд 26Определите количество нейтронов, протонов и электронов в изотопе брома-81.
Определите число нейтронов в

изотопе хлора-37.
Слайд 27Двухатомные молекулы
Запомнить 7 двухатомных молекул.
H2 N2 O2 F2 Cl2 Br2 I2

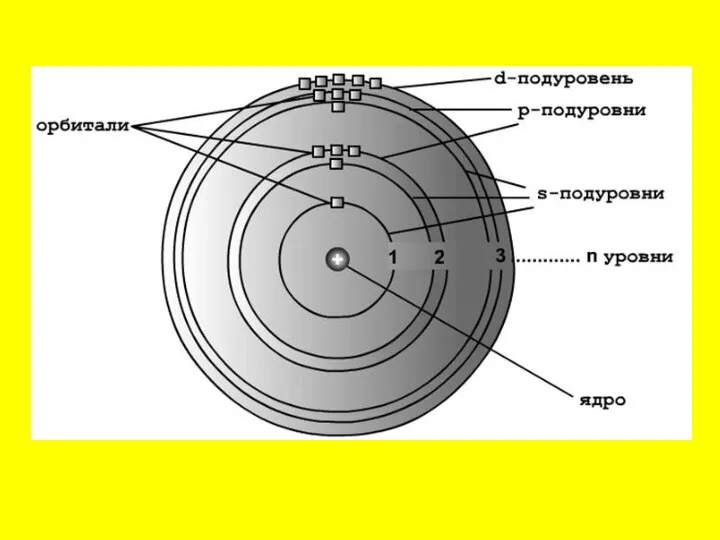
Слайд 28Строение электронной оболочки
Согласно квантовой модели строение атома Нильса Бора, электроны в атоме

могут двигаться только по определенным (стационарным) орбитам, удаленным от ядра на определенное расстояние и характеризующиеся определенной энергией. Другое название стационарны орбит — электронные слои или энергетические уровни.
Слайд 30Электронные уровни можно обозначать цифрами — 1, 2, 3, …, n. Номер

слоя увеличивается мере удаления его от ядра. Номер уровня соответствует главному квантовому числу n.
В одном слое электроны могут двигаться по разным траекториям. Траекторию орбиты характеризует электронный подуровень. Тип подуровня характеризует орбитальное квантовое число l = 0,1, 2, 3 …, либо соответствующие буквы — s, p, d, g и др.
Слайд 32В рамках одного подуровня (электронных орбиталей одного типа) возможны варианты расположения орбиталей

в пространстве. Чем сложнее геометрия орбиталей данного подуровня, тем больше вариантов их расположения в пространстве. Общее число орбиталей подуровня данного типа l можно определить по формуле: 2l+1. На каждой орбитали может находиться не более двух электронов.
Слайд 33Электронная оболочка атома — это все электроны атома. Электроны в электронной оболочке атома расположены слоями.

Электроны в разных слоях различаются энергией взаимодействия с ядром атома. Чем дальше от ядра находится электрон, тем меньше энергия его взаимодействия с ядром.
Слайд 34Вместимость электронных слоев различная. В слое № 1, или в первом слое, у

всех элементов, кроме водорода, находится 2 электрона. (В атоме водорода всего 1. электрон, и он — в первом слое.) Во втором слое может находиться не больше восьми электронов. В третьем слое максимально может расположиться 18 электронов. В четвертом слое максимально бывает 32 электрона.
Если N — максимальное число электронов на электронном слое с номером n, то для определения числа N можно воспользоваться формулой
N = 2n2 .
Слайд 35Завершенный электронный слой — это слой в атоме, содержащий максимально возможное для

него число электронов.
Электронные слои заполняются так: сначала первый, потом второй и последующие — по мере уменьшения энергии их взаимодействия с ядром. Расположение по слоям электронов в атомах водорода, кислорода и магния:
Слайд 37Химические свойства атомов определяются свойствами их электронов. Движение электронов в атоме описывают

с привлечением понятия орбитали. Каждый электрон в атоме находится на своей орбитали.
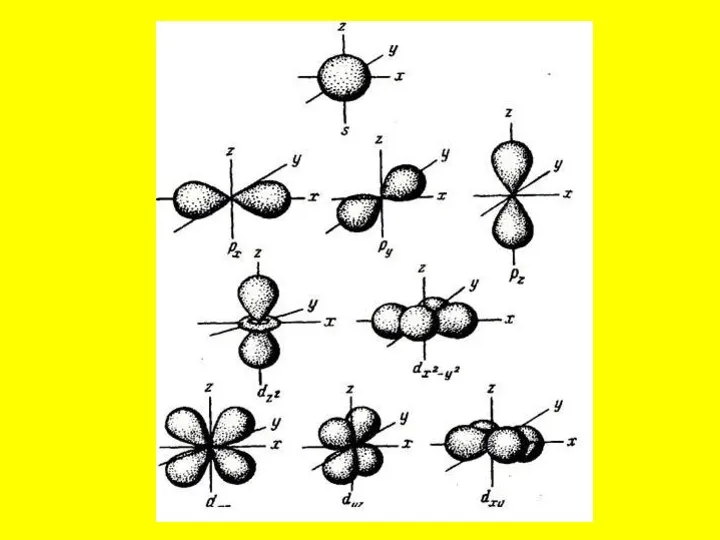
Слайд 39Орбиталь — это часть электронного облака, создаваемого электронами при движении в атоме. Орбиталь

— это пространство около ядра, где чаще всего находится электрон.
Слайд 40Заполнение электронами энергетических орбиталей происходит согласно некоторым основным правилам.
Принцип Паули (запрет Паули): на

одной атомной орбитали могут находиться не более двух электронов с противоположными спинами (спин — это квантовомеханическая характеристика движения электрона).
Правило Хунда. На атомных орбиталях с одинаковой энергией электроны располагаются по одному с параллельными спинами. Т.е. орбитали одного подуровня заполняются так: сначала на каждую орбиталь распределяется по одному электрону. Только когда во всех орбиталях данного подуровня распределено по одному электрону, занимаем орбитали вторыми электронами, с противоположными спинами.
Слайд 41Таким образом, сумма спиновых квантовых чисел таких электронов на одном энергетическом подуровне (оболочке)

будет максимальной.
Слайд 42Принцип минимума энергии. Электроны заполняют сначала орбитали с наименьшей энергией. Энергия атомной орбитали

эквивалентна сумме главного и орбитального квантовых чисел: n + l. Если сумма одинаковая, то заполняется первой та орбиталь, у которой меньше главное квантовое число n.
Слайд 44Таким образом, энергетический ряд орбиталей выглядит так:
1s < 2s < 2 p < 3s < 3p < 4s < 3d < 4p <

5s < 4d < 5p < 6s < 4f~5d < 6p < 7s <5f~6d …
Слайд 45Электронную структуру атома можно представлять в разных формах — энергетическая диаграмма, электронная формула и

др. Разберем основные.
Энергетическая диаграмма атома — это схематическое изображение орбиталей с учетом их энергии. Диаграмма показывает расположение электронов на энергетических уровнях и подуровнях. Заполнение орбиталей происходит согласно квантовым принципам.
Слайд 46Например, энергетическая диаграмма для атома углерода:
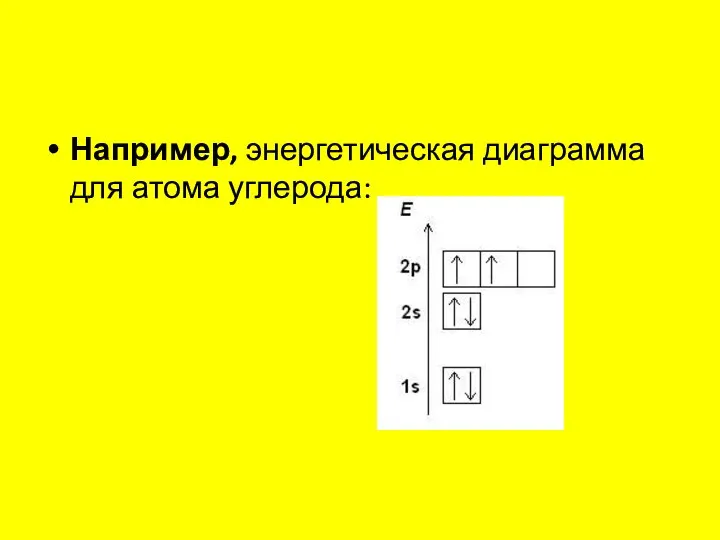
Слайд 47Электронная формула — это запись распределения электронов по орбиталям атома или иона. Сначала

указывается номер уровня, затем тип орбитали. Верхний индекс справа от буквы показывает число электронов на орбитали. Орбитали указываются в порядке заполнения. Запись 1s2 означает, что на 1 уровне s-подуровне расположено 2 электрона.
Например, электронная формула углерода выглядит так: 1s22s22p2.
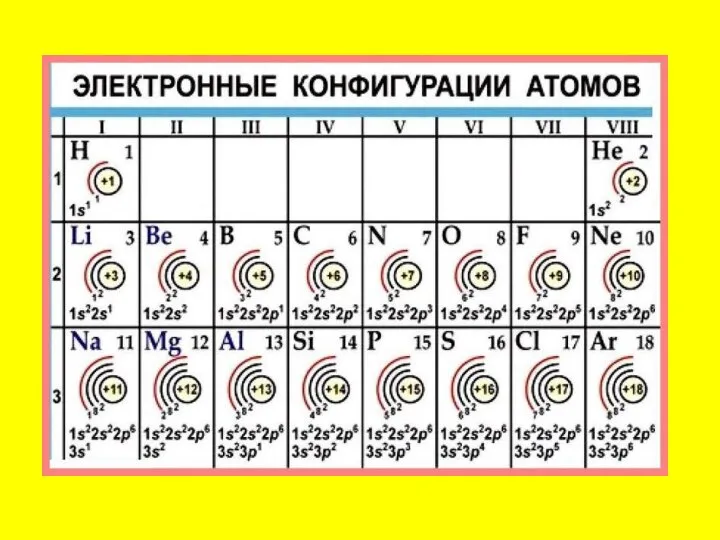
Слайд 48Электронные формулы элементов первых четырех периодов

Слайд 50Рассмотрим заполнение электронами оболочки элементов первых четырех периодов. У водорода заполняется самый первый энергетический

уровень, s-подуровень, на нем расположен 1 электрон:
Слайд 51У гелия 1s-орбиталь полностью заполнена:

Слайд 52У бериллия 2s-подуровень заполнен:

Слайд 53 У бора заполняется p-подуровень второго уровня:

Слайд 54У следующего элемента, углерода, очередной электрон, согласно правилу Хунда, заполняет вакантную орбиталь, а

не заполняет частично занятую:
Слайд 55Попробуйте составить электронную и электронно-графическую формулы для следующих элементов.
Азот
Кислород
Фтор

Слайд 57У неона завершено заполнение второго энергетического уровня:

Слайд 58У натрия начинается заполнение третьего энергетического уровня:

Слайд 59От натрия до аргона заполнение 3-го уровня происходит в том же порядке,

что и заполнение 2-го энергетического уровня.
А вот начиная с 19-го элемента, калия, иногда начинается путаница — заполняется не 3d-орбиталь, а 4s. Заполнение энергетических уровней и подуровней электронами происходит по энергетическому ряду орбиталей, а не по порядку. Рекомендую повторить его еще раз. Таким образом, формула калия:
Слайд 62Дальнейшее заполнение 3d-подуровня происходит согласно квантовым правилам, от титана до ванадия:

Слайд 63Однако, у следующего элемента порядок заполнения орбиталей нарушается. Электронная конфигурация хрома такая:

Слайд 64При «традиционном» порядке заполнения орбиталей (соответственно, неверном в данном случае — 3d44s2) ровно одна

ячейка в d-подуровне оставалась бы незаполненной. Оказалось, что такое заполнение энергетически менее выгодно. А более выгодно, когда d-орбиталь заполнена полностью, хотя бы единичными электронами. Этот лишний электрон переходит с 4s-подуровня. И небольшие затраты энергии на перескок электрона с 4s-подуровня с лихвой покрывает энергетический эффект от заполнения всех 3d-орбиталей. Этот эффект так и называется — «провал» или «проскок» электрона. И наблюдается он, когда d-орбиталь недозаполнена на 1 электрон (по одному электрону в ячейке или по два).
Слайд 65У меди мы снова наблюдаем провал (проскок) электрона — электрон опять проскакивает с 4s-подуровня на 3d-подуровень:
+29Cu [Ar]3d104s1

Слайд 66На цинке завершается заполнение 3d-подуровня:
+30Zn [Ar]3d104s2
![На цинке завершается заполнение 3d-подуровня: +30Zn [Ar]3d104s2](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/1002715/slide-65.jpg)
Слайд 67У следующих элементов, от галлия до криптона, происходит заполнение 4p-подуровня по квантовым правилам. Например, электронная

формула галлия:
+31Ga [Ar]3d104s24p1
Слайд 68Некоторые важные понятия:
Внешний энергетический уровень — это энергетический уровень в атоме с максимальным номером, на

котором есть электроны.
Например, у меди ([Ar]3d104s1) внешний энергетический уровень — четвёртый.
Слайд 69Валентные электроны — электроны в атоме, которые могут участвовать в образовании химической связи.

Например, у хрома (+24Cr [Ar]3d54s1) валентными являются не только электроны внешнего энергетического уровня (4s1), но и неспаренные электроны на 3d-подуровне, т.к. они могут образовывать химические связи.
Слайд 70Основное и возбужденное состояние атома

Слайд 71Электронные формулы, которые мы составляли до этого, соответствуют основному энергетическому состоянию атома.

Это наиболее выгодное энергетически состояние атома.
Однако, чтобы образовывать химические связи, атому в большинстве ситуаций необходимо наличие неспаренных (одиночных) электронов. А химические связи энергетически очень для атома выгодны. Следовательно, чем больше в атоме неспаренных электронов — тем больше связей он может образовать, и, как следствие, перейдёт в более выгодное энергетическое состояние.
Слайд 72Поэтому при наличии свободных энергетических орбиталей на данном уровне спаренные пары электронов могут распариваться, и один из

электронов спаренной пары может переходить на вакантную орбиталь. Таким образом число неспаренных электронов увеличивается, и атом может образовать больше химических связей, что очень выгодно с точки зрения энергии. Такое состояние атома называют возбуждённым и обозначают звёздочкой.
Слайд 73Например, в основном состоянии бор имеет следующую конфигурацию энергетического уровня:

Слайд 74На втором уровне (внешнем) одна спаренная электронная пара, один одиночный электрон и

пара свободных (вакантных) орбиталей. Следовательно, есть возможность для перехода электрона из пары на вакантную орбиталь, получаем возбуждённое состояние атома бора (обозначается звёздочкой):
Слайд 75Попробуйте самостоятельно составить электронную формулу, соответствующую возбуждённому состоянию атомов.
Углерод

Слайд 78Атомы могут отдавать и принимать электроны. Отдавая или принимая электроны, они превращаются

в ионы.
Ионы — это заряженные частицы. Избыточный заряд обозначается индексом в правом верхнем углу.
Слайд 79Если атом отдаёт электроны, то общий заряд образовавшейся частицы будет положительный (вспомним, что число протонов в

атоме равно числу электронов, а при отдаче электронов число протонов будет больше числа электронов). Положительно заряженные ионы — это катионы. Например: катион натрия образуется так:
+11Na 1s22s22p63s1 -1е = +11Na+ 1s22s22p63s0
Слайд 80Если атом принимает электроны, то приобретает отрицательный заряд. Отрицательно заряженные частицы — это анионы. Например, анион хлора образуется

так:
+17Cl 1s22s22p63s23p5 +1e = +17Cl— 1s22s22p63s23p6
Слайд 81Таким образом, электронные формулы ионов можно получить добавив или отняв электроны у атома. Обратите

внимание, при образовании катионов электроны уходят с внешнего энергетического уровня. При образовании анионов электроны приходят на внешний энергетический уровень.
Слайд 82Попробуйте составить самостоятельно электронный формулы ионов.
Ион Са2+

Слайд 83Электронная формула иона кальция Са2+:
+20Ca2+ 1s22s22p63s23p6




























































![На цинке завершается заполнение 3d-подуровня: +30Zn [Ar]3d104s2](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/1002715/slide-65.jpg)

















 Получение функциональных плёнок на основе TiO2
Получение функциональных плёнок на основе TiO2 Протолитические буферные системы. Буферные системы организма, их взаимодействие
Протолитические буферные системы. Буферные системы организма, их взаимодействие Ковалентная неполярная связь
Ковалентная неполярная связь Потенциометрические анализаторы Поверка рН - метра
Потенциометрические анализаторы Поверка рН - метра Амины. Аминокислоты. Белки. (Лекция 8)
Амины. Аминокислоты. Белки. (Лекция 8) Химический тренажер
Химический тренажер Электролитическая диссоциация. 9 класс
Электролитическая диссоциация. 9 класс Степень окисления
Степень окисления Всё о нефти. Часть 5
Всё о нефти. Часть 5 Презентация на тему Минеральные удобрения
Презентация на тему Минеральные удобрения  Проведение лабраторных общеклинических исследований
Проведение лабраторных общеклинических исследований Ацилирование. Лекция 4
Ацилирование. Лекция 4 Закономерности процессов тепло- и газообмена на пожаре
Закономерности процессов тепло- и газообмена на пожаре Презентация на тему Органическая химия. История развития
Презентация на тему Органическая химия. История развития  Способы получения металлов
Способы получения металлов Открытый урок по химии в 8 классе по теме: «Первоначальные химические понятия». Учитель химии ГБОУ СОШ № 650 Безверхова Олеся Влад
Открытый урок по химии в 8 классе по теме: «Первоначальные химические понятия». Учитель химии ГБОУ СОШ № 650 Безверхова Олеся Влад Исследование физико-химических свойств щавелевой кислоты
Исследование физико-химических свойств щавелевой кислоты Природные источники углеводородов
Природные источники углеводородов Ковалентная химическая связь
Ковалентная химическая связь Минералы
Минералы Составление ионных уравнений
Составление ионных уравнений Теоретические основы органической химии. Лекция 25
Теоретические основы органической химии. Лекция 25 Щелочноземельные металлы
Щелочноземельные металлы Железо и его сплавы
Железо и его сплавы Неметаллы. Особенности электронного строения атомов НМ
Неметаллы. Особенности электронного строения атомов НМ Стехиометрические законы химии
Стехиометрические законы химии Метаболизм азота
Метаболизм азота Общая химия. Основные понятия
Общая химия. Основные понятия