Содержание
- 2. Нахождение металлов в природе
- 3. восстановление металлов из руд при высоких температурах с помощью углерода, оксида углерода (II), водорода, алюминия и
- 4. Восстановление оксидом углерода (II) SnO2 + CO ? Восстановление алюминием или магнием Al + Fe2O3 ?
- 5. Восстановление металлов из солей в растворе. 2Na[Au(CN)2] + Zn ? Na2[Zn(CN)4] + 2Au (цианирование) СuSO4 +
- 6. Восстановление металлов при помощи электролиза. NaCl ? Al2O3 ? 3. Электрометаллургия
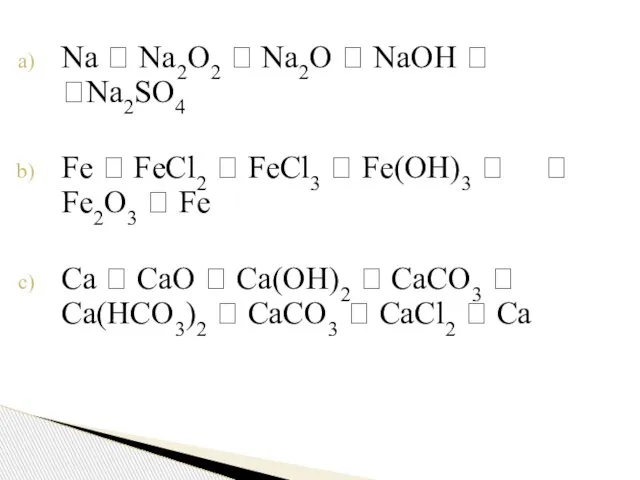
- 7. Na ? Na2O2 ? Na2O ? NaOH ? ?Na2SO4 Fe ? FeCl2 ? FeCl3 ? Fe(OH)3
- 9. Скачать презентацию



![Восстановление металлов из солей в растворе. 2Na[Au(CN)2] + Zn ? Na2[Zn(CN)4] +](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/865868/slide-4.jpg)

 Твердые электролиты
Твердые электролиты Презентация на тему Строение атома Химическая связь
Презентация на тему Строение атома Химическая связь  Коллоидные системы
Коллоидные системы Исследование молока
Исследование молока Реакцияға қабілетті олигомерлердің мономерлерге қарағанда артықшылығы
Реакцияға қабілетті олигомерлердің мономерлерге қарағанда артықшылығы Виготовлення водних розчинів з заданою масовою часткою розчиненої речовини
Виготовлення водних розчинів з заданою масовою часткою розчиненої речовини 98675992
98675992 Дизайн молекулярных магнетиков
Дизайн молекулярных магнетиков Щелочноземельные металлы
Щелочноземельные металлы Современное представление о строении атома, S- и P- орбитали
Современное представление о строении атома, S- и P- орбитали Пространственная изомерия органических соединений
Пространственная изомерия органических соединений Технологические процессы получения кислорода
Технологические процессы получения кислорода Получение меди
Получение меди Аналитические методы контроля в техносферной безопасности. Лекция 1
Аналитические методы контроля в техносферной безопасности. Лекция 1 Вещество. Простые и сложные вещества
Вещество. Простые и сложные вещества Факторы, влияющие на скорость химических реакций
Факторы, влияющие на скорость химических реакций Химический состав водотоков архипилага Новая земля и их воздействие на прибрежную зону
Химический состав водотоков архипилага Новая земля и их воздействие на прибрежную зону Угольная кислота и её соли
Угольная кислота и её соли Алкены. Непредельные углеводороды
Алкены. Непредельные углеводороды Природные источники углеводородов
Природные источники углеводородов Составление уравнений окислительно-восстановительных реакций
Составление уравнений окислительно-восстановительных реакций Оксид цинка ZnO
Оксид цинка ZnO 11 класс 15.09
11 класс 15.09 Термохимические эффекты реакций
Термохимические эффекты реакций Кислородсодержащие органические соединения
Кислородсодержащие органические соединения Оливины. Структура оливинов
Оливины. Структура оливинов Предельные углеводороды (алканы)
Предельные углеводороды (алканы) Интерактивная интеллектуальная игра Юный химик
Интерактивная интеллектуальная игра Юный химик