Слайд 2Классификация реакций
Все химические реакции можно разделить на 2 группы, в одних

реакциях степень окисления атомов остается неизменной (обменные реакции), а в других реакциях она меняется – это окислительно-восстановительные реакции.
Протекание их связано с переходом электронов от одних атомов (ионов) к другим.
Слайд 3Окислительно - восстановительные реакции (ОВР)
Реакции, протекающие с изменением степени окисления, называются окислительно

– восстановительными.
Степень окисления – условный заряд атома в соединении, вычисленный из предположения, что оно состоит только из ионов.
Слайд 4«─» степень окисления имеют атомы, которые приняли электроны от других атомов или

в их сторону смещены связующие электронные облака.
«+» степень окисления имеют атомы, которые отдали свои электроны другим атомам.
«0» степень окисления имеют атомы в молекулах простых веществ.
Слайд 5Правила определения степени окисления
самый электроотрицательный элемент, во всех соединениях -1.
за

исключением гидридов металлов
постоянная степень окисления –2, за исключением:
пероксида водорода
фторида кислорода
Слайд 6
Атомы элементов I-III групп ПС, отдающие свои электроны, имеют постоянную «+» степень

окисления, равную номеру группы.
Исключение: Cu (+1,+2),
Au (+1,+3),
Hg (+1,+2).
Слайд 7Атомы элементов главных подгрупп IV-VI групп могут проявлять несколько степеней окисления.
Высшую «+»,

равную номеру группы
Промежуточную, на 2 единицы меньше, чем высшая,
Низшую «─», равную разности между номером группы и число 8
Исключение: N (+1,+2,+3,+4,+5, -3)
Слайд 8Атомы металлов могут иметь только «+» степень окисления.
Атомы элементов VII группы, главной

подгруппы –галогены (кроме фтора) могут иметь в соединениях все нечетные степени окисления от ─1 до +7 (─1, +1, +3,+5,+7)
Алгебраическая сумма степеней окисления в соединение равна 0, а в сложном ионе – заряду иона.
Слайд 9Окислители и восстановители
Окислением называется процесс отдачи электронов, степень окисления атома при этом

повышается:
Al0 - 3ē → Al+3
S―2 - 8ē → S+6
Восстановлением называется процесс присоединения электронов, степень окисления при этом понижается:
S0 + 2ē → S―2
Al+3 + 3ē → Al0
Слайд 10Вещества, атомы которых присоединяют электроны, называются окислителями.
В процессе реакции окислители восстанавливаются.
Вещества,

атомы которых отдают электроны, называются восстановителями.
В реакции восстановители окисляются.
Слайд 12 Вещества, в состав которых входит элемент в промежуточной степени окисления, проявляют окислительно

– восстановительную двойственность: по отношению к окислителю они являются восстановителями, а по отношению к восстановителям – окислителями.
ОВР - это единство 2 противоположных процессов – окисления и восстановления. Число электронов, которое отдает восстановитель, равно числу электронов, которое присоединяет окислитель.
Слайд 13Составление уравнений ОВР методом электронного баланса
Пример 1. MnS +HNO3 → MnSO4 +

NO + H2O
1. Определяют степени окисления всех атомов и атомы, изменившие степень окисления:
Mn+2S―2 + H+N+5O3―2 →
Mn+2S+6O4―2 + N+2O―2 + H2+O―2
Слайд 142. Составляют схемы процессов окисления и восстановления.
3. Записывается число отданных и число

принятых электронов, для этих чисел находится наименьшее общее кратное, разделив которое на число отданных и ринятых электронов, получаем коэффициенты перед MnS и HNO3:
S―2 - 8ē → S+6 8 24 3 - окисление
N+5 + 3ē → N+2 3 8 – восстановление
MnS – восстановитель; HNO3 – окислитель.
Слайд 166. Для проверки - подсчитывают число атомов кислорода в левой и правой

частях уравнения.
В левой части уравнения 24 атома кислорода, в правой части – то же 24 атома кислорода.
Последовательность:
Основные коэффициенты;
Металлы;
Неметаллы;
Н;
Проверка по О.


















 Тренажёр: знаки химических элементов
Тренажёр: знаки химических элементов Алкены. Физические и химические свойства
Алкены. Физические и химические свойства Окислительно-восстановительные реакции
Окислительно-восстановительные реакции Химически опасные объекты Аварии, связанные с выбросом АХОВ
Химически опасные объекты Аварии, связанные с выбросом АХОВ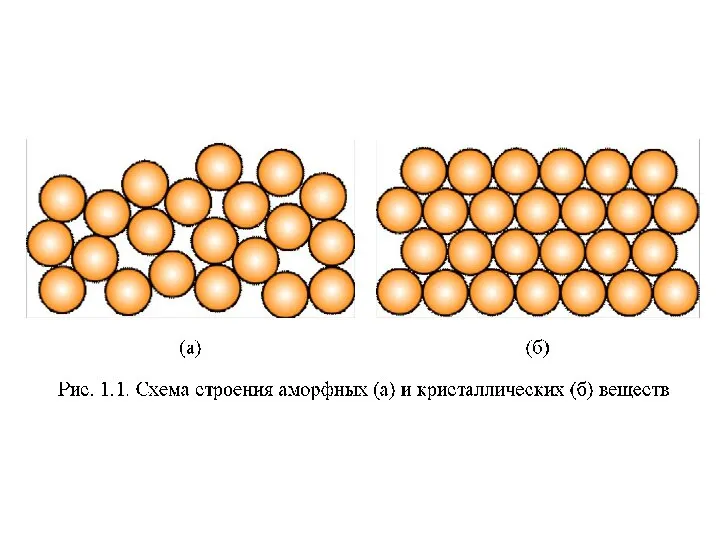 Материаловедение
Материаловедение Синтетические волокна
Синтетические волокна Презентация на тему Неметаллы, особенности строения
Презентация на тему Неметаллы, особенности строения  Электролиз (катод)
Электролиз (катод) Основные принципы работы химических сенсоров
Основные принципы работы химических сенсоров Химическая картина мира
Химическая картина мира Основания: определение, классификация, химические свойства
Основания: определение, классификация, химические свойства Металлы. Общая характеристика, химические свойства. Получение
Металлы. Общая характеристика, химические свойства. Получение Вебинар. Гидролиз солей
Вебинар. Гидролиз солей Свойства радиоактивных элементов
Свойства радиоактивных элементов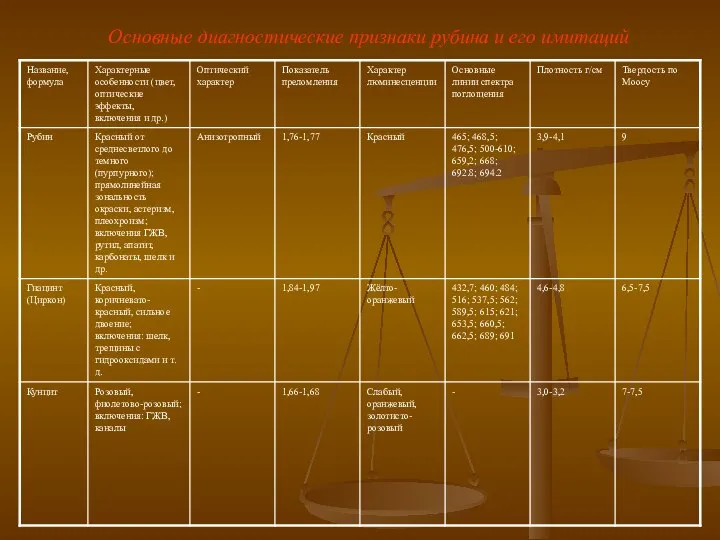 Основные диагностические признаки рубина и его имитаций
Основные диагностические признаки рубина и его имитаций Генетические ряды неорганических соединений
Генетические ряды неорганических соединений Двойные латуни. Диаграмма состояния. Примеси. Структура и свойства
Двойные латуни. Диаграмма состояния. Примеси. Структура и свойства Вуглеводи. Визначення вуглеводів
Вуглеводи. Визначення вуглеводів Галогены. Обобщение знаний
Галогены. Обобщение знаний Подготовка к ГИА по химии
Подготовка к ГИА по химии Предпосылки открытия Периодического закона Д. И. Менделеевым
Предпосылки открытия Периодического закона Д. И. Менделеевым ОВ. Структура и принцип работы параметры ОВ
ОВ. Структура и принцип работы параметры ОВ Абсолютное первенство по химии - 2012
Абсолютное первенство по химии - 2012 строение атома углерода. Валентные состояния атома углерода
строение атома углерода. Валентные состояния атома углерода Общая характеристика элементов IIА группы
Общая характеристика элементов IIА группы Вода… Химические названия
Вода… Химические названия Водород – первый элемент в периодической таблице
Водород – первый элемент в периодической таблице Кристаллы, выращенные учащимися
Кристаллы, выращенные учащимися