Содержание
- 2. Вещества Электролиты - вещества, растворы и расплавы которых не проводят электрический ток. Неэлектролиты - вещества, растворы
- 3. Неэлектролиты вещества, которые содержат ковалентные неполярные или малополярные связи. Эти связи не распадаются на ионы. газы,
- 4. Электролиты Вещества, которые содержат ионные и ковалентные полярные связи. Эти связи легко распадаются на ионы. Неорганические
- 5. Электролитическая диссоциация – процесс распада электролита на ионы при растворении его в воде или расплавлении
- 6. Вещества с ионной связью Кристаллическая решетка NaCl Кристалл NaCl
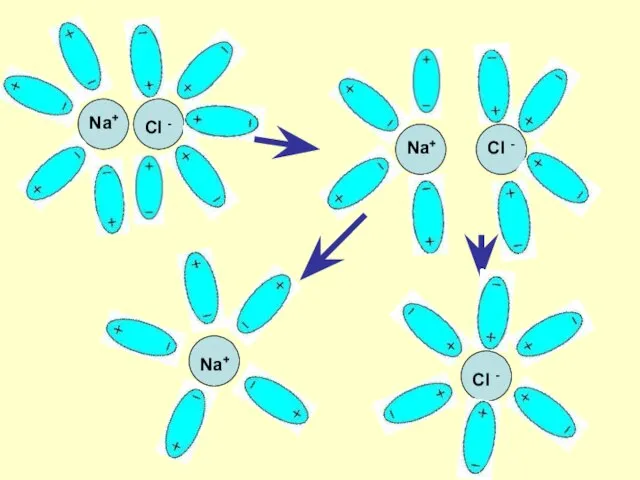
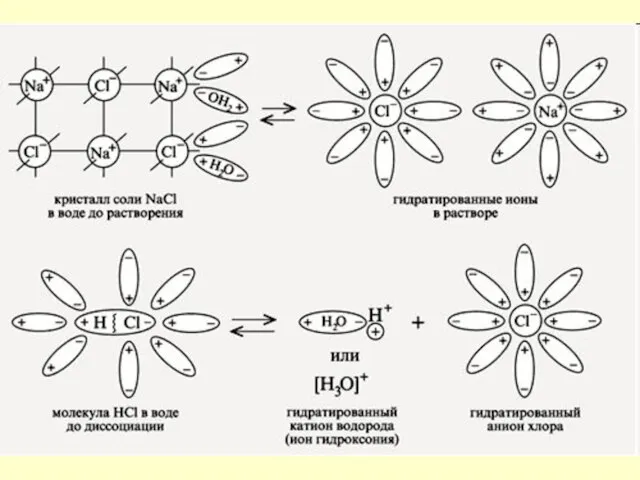
- 7. Механизм ЭД ионных веществ Ориентация диполей воды вокруг кристаллов соли. Образование между молекулами воды и ионами
- 8. Na+ Cl - Na+ Cl - Na+ Cl -
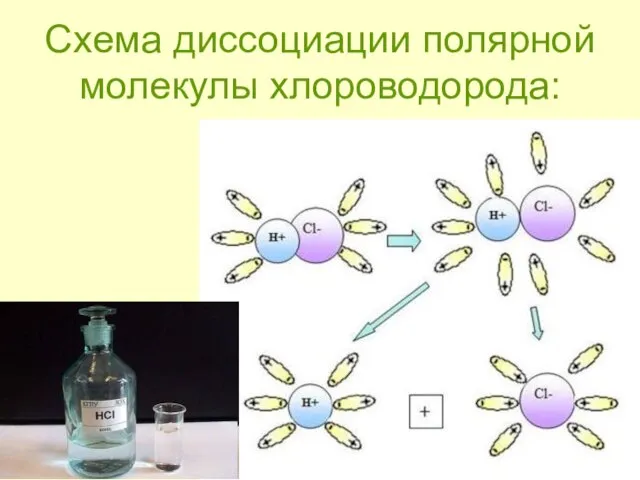
- 9. Механизм ЭД полярных веществ ориентация диполей воды вокруг полярной молекулы. еще большая поляризация полярной молекулы и
- 10. Схема диссоциации полярной молекулы хлороводорода:
- 11. Электролиты Сильные - при растворении в воде практически полностью распадаются на ионы. Слабые частично распадаются на
- 12. Сильные электролиты вещества с ионными или сильно полярными связями. все хорошо растворимые соли, сильные кислоты (HCl,
- 13. Слабые электролиты вещества с неполярными и малополярными связями: 1) почти все органические кислоты (CH3COOH, C2H5COOH и
- 14. Степень диссоциации Степень диссоциации (α) - отношение числа распавшихся на ионы молекул (n) к общему числу
- 15. Электролитическая диссоциация веществ, идущая с образованием свободных ионов объясняет электрическую проводимость растворов. CaCl2 = Ca2+ +
- 16. Диссоциация кислот осуществляется ступенчато. На каждой ступени отщепляется один ион водорода. H Cl = H+ +
- 17. Диссоциация оснований Ba(OH)2 = Ba2+ + 2OH- Сa(OH)2 = Сa2+ + 2OH- Основания - при диссоциации
- 18. Диссоциация солей Средние соли – соли, состоящие из атомов металла и кислотного остатка, диссоциируют в одну
- 19. Диссоциация солей Кислые соли – соли, в состав молекул которых кроме атомов металла входят атомы водорода,
- 20. Шведский ученый Сванте Аррениус(1859-1927) В 1887 году создал теорию ЭД. В 1903году был удостоен Нобелевской премии
- 21. Каблуков И.А. Кистяковский В.А.
- 22. Русские химики И.А.Каблуков и В.А.Кистяковский применили к объяснению электролитической диссоциации химическую теорию растворов Д.И.Менделеева и доказали,
- 23. Основные положения теории ЭД 1. Электролиты в водной среде (и в расплавленном состоянии) распадаются на положительно
- 25. Основные положения теории ЭД 2. Беспорядочное движение ионов в растворе под действием электрического поля становится направленным:
- 26. Основные положения теории ЭД 3. Диссоциация – обратимый процесс: параллельно с распадом молекул на ионы (диссоциацией)
- 27. 4. Степень электролитической диссоциации (a) зависит от природы электролита и растворителя, температуры и концентрации. Она показывает
- 28. Основные положения теории ЭД 5. Свойства ионов резко отличаются от свойств нейтральных атомов составляющих их элементов.
- 29. Источники информации: http://slovari.yandex.ru/ http://www.lyceum8.ru/himiya/4.htm http://900igr.net/fotografii/khimija/Dissotsiatsija/010-Mekhanizm-dissotsiatsii-veschestv.html http://him.1september.ru/2003/34/7.htm http://900igr.net/kartinki/khimija/Povarennaja-sol/059-K-r-i-s-t-a-l-l-y-g-a-l-i-t-a.html
- 31. Скачать презентацию

























 Методы восстановления. Формирование СН-связей декарбоксилированием и декарбонилированием
Методы восстановления. Формирование СН-связей декарбоксилированием и декарбонилированием Основные понятия химической термодинамики
Основные понятия химической термодинамики Биологическая роль III(A) группы
Биологическая роль III(A) группы Органические вещества
Органические вещества Презентация на тему Кристаллические решетки
Презентация на тему Кристаллические решетки  Адсорбция твёрдыми адсорбентами
Адсорбция твёрдыми адсорбентами Фторсодержащие полимеры
Фторсодержащие полимеры Презентация на тему Волокна
Презентация на тему Волокна  Презентация на тему Путешествие по континенту Химия
Презентация на тему Путешествие по континенту Химия  Соли в природе и их значение
Соли в природе и их значение Задача №3: Трансмутация. Команда: Карбораны
Задача №3: Трансмутация. Команда: Карбораны Курс химии для основных академических направлений подготовки специалистов НИЯУ МИФИ
Курс химии для основных академических направлений подготовки специалистов НИЯУ МИФИ Металлическая химическая связь
Металлическая химическая связь Карбид кремния
Карбид кремния Кетоновые тела
Кетоновые тела Химия в еде
Химия в еде Степени окисления
Степени окисления Алкины
Алкины Презентация на тему Коррозия
Презентация на тему Коррозия  Ренгеноструктурный и рентгеноспектральный анализы
Ренгеноструктурный и рентгеноспектральный анализы Ароматические углеводороды
Ароматические углеводороды Алканы
Алканы Презентация на тему Органическая химия. История развития
Презентация на тему Органическая химия. История развития  Моноенаминирование 4-пиронов и 4-метилен-4н-пиранов
Моноенаминирование 4-пиронов и 4-метилен-4н-пиранов Особенные свойства муравьиной кислоты
Особенные свойства муравьиной кислоты Физическая химия, термодинамика
Физическая химия, термодинамика Теоретические основы органической химии. Лекция 25
Теоретические основы органической химии. Лекция 25 valentnost
valentnost