Содержание
- 2. ОКСИДЫ Оксиды – сложные вещества, состоящие из двух элементов, один из которых кислород. II II СаО
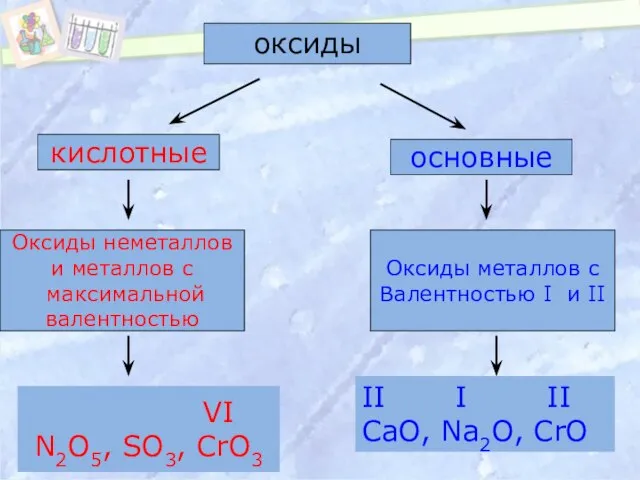
- 3. оксиды кислотные основные Оксиды неметаллов и металлов с максимальной валентностью Оксиды металлов с Валентностью I и
- 4. Классифицировать и назвать оксиды: CO2 MnO K2O Cl2O5 Mn2O7 FeO Оксид углерода IV, кислотный Оксид марганца
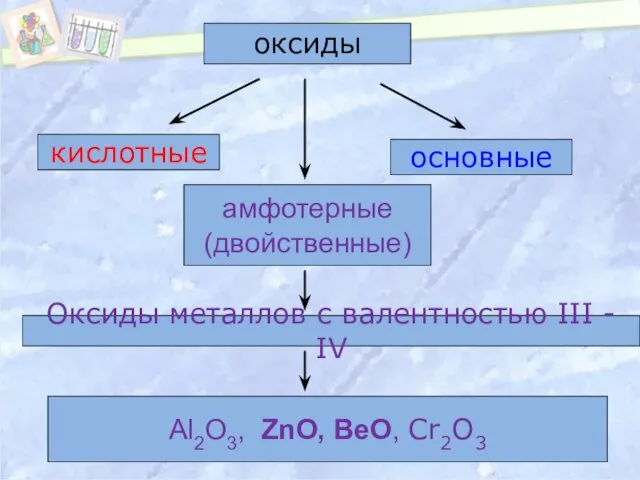
- 6. оксиды кислотные основные амфотерные (двойственные) Оксиды металлов с валентностью III - IV Al2O3, ZnO, BeO, Cr2O3
- 7. Химические свойства оксидов 1) Взаимодействие оксидов с водой : Оксид + Вода Растворимый гидроксид = CaO
- 8. Химические свойства оксидов 2) Взаимодействие оксидов между собой Оксид + оксид Соль = CaO + SO3=
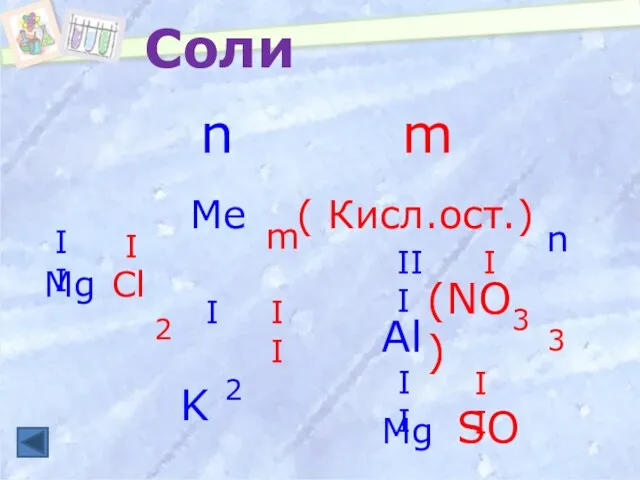
- 9. n m n m Соли Mg Cl 2 Al (NO3) 3 K 2 SO4 II II
- 10. Химические свойства оксидов 3) Взаимодействие оксидов с гидроксидами Оксид + Гидроксид Соль + вода = CaO
- 12. Скачать презентацию






 Тренажёр: знаки химических элементов
Тренажёр: знаки химических элементов Алкены. Физические и химические свойства
Алкены. Физические и химические свойства Окислительно-восстановительные реакции
Окислительно-восстановительные реакции Химически опасные объекты Аварии, связанные с выбросом АХОВ
Химически опасные объекты Аварии, связанные с выбросом АХОВ Материаловедение
Материаловедение Синтетические волокна
Синтетические волокна Презентация на тему Неметаллы, особенности строения
Презентация на тему Неметаллы, особенности строения  Электролиз (катод)
Электролиз (катод) Основные принципы работы химических сенсоров
Основные принципы работы химических сенсоров Химическая картина мира
Химическая картина мира Основания: определение, классификация, химические свойства
Основания: определение, классификация, химические свойства Металлы. Общая характеристика, химические свойства. Получение
Металлы. Общая характеристика, химические свойства. Получение Вебинар. Гидролиз солей
Вебинар. Гидролиз солей Свойства радиоактивных элементов
Свойства радиоактивных элементов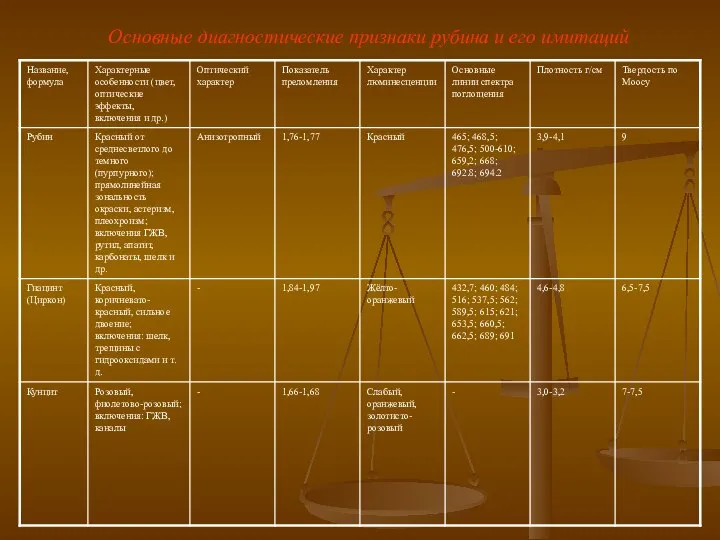 Основные диагностические признаки рубина и его имитаций
Основные диагностические признаки рубина и его имитаций Генетические ряды неорганических соединений
Генетические ряды неорганических соединений Двойные латуни. Диаграмма состояния. Примеси. Структура и свойства
Двойные латуни. Диаграмма состояния. Примеси. Структура и свойства Вуглеводи. Визначення вуглеводів
Вуглеводи. Визначення вуглеводів Галогены. Обобщение знаний
Галогены. Обобщение знаний Подготовка к ГИА по химии
Подготовка к ГИА по химии Предпосылки открытия Периодического закона Д. И. Менделеевым
Предпосылки открытия Периодического закона Д. И. Менделеевым ОВ. Структура и принцип работы параметры ОВ
ОВ. Структура и принцип работы параметры ОВ Абсолютное первенство по химии - 2012
Абсолютное первенство по химии - 2012 строение атома углерода. Валентные состояния атома углерода
строение атома углерода. Валентные состояния атома углерода Общая характеристика элементов IIА группы
Общая характеристика элементов IIА группы Вода… Химические названия
Вода… Химические названия Водород – первый элемент в периодической таблице
Водород – первый элемент в периодической таблице Кристаллы, выращенные учащимися
Кристаллы, выращенные учащимися