Содержание
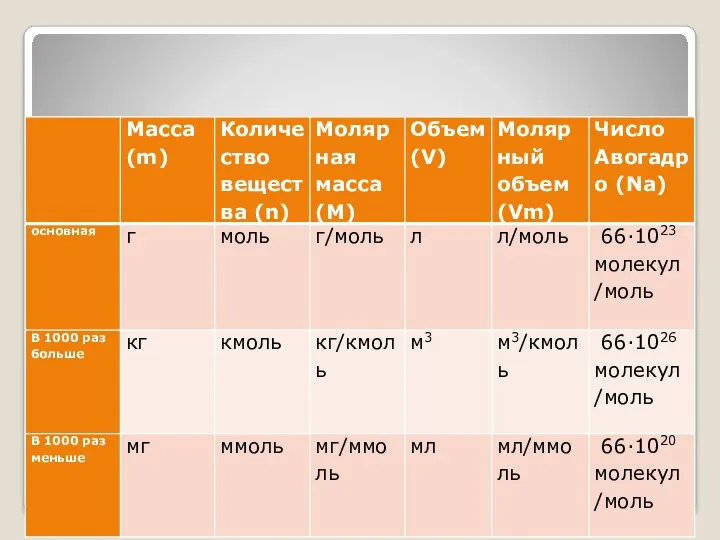
- 2. Моль – такое количество вещества, в котором содержится 6∙1023 молекул этого вещества. Молярная масса – масса
- 3. Буквенные обозначения: Количество вещества - n Молярный объем - Vm Молярная масса - M Масса -
- 4. Основные формулы
- 5. Массовая доля. Массовая доля элементов в веществе. Буквенные обозначения ω – массовая доля (в долях от
- 6. Массовая и объемная доли компонентов смеси (раствора). Буквенные обозначения ω – массовая доля (в долях от
- 7. Расчет массовой или объемной доли выхода продукта реакции от теоретически возможного. Выход продукта реакции от теоретически
- 8. Расчет теплового эффекта реакции. Экзотермические реакции – протекают с выделением теплоты +Q Эндотермические реакции – протекают
- 9. Алгоритм решения задачи . Внимательно прочтите условия задачи 2-3 раза. 2. Кратко запишите, что дано (известно)
- 10. Задачи 1.Определите объем (н.у.) сероводорода массой 13,6 г. 2.Определите массу кислорода объемом 33,6 л(н.у.) 3.Газовая смесь
- 11. 5. Оксид элемента имеет состав ЭО3 Массовая доля кислорода в этом оксиде составляет 60%. Определите какой
- 12. Хлорид элемента имеет состав ЭСl2 Массовая доля хлора в этом хлориде составляет 52,21%. Определите какой элемент
- 13. Определите молярную массу оксида углерода, плотность которого по воздуху составляет 1,51. Какой это оксид углерода?
- 14. Решить самостоятельно
- 15. Массовые доли углерода, азота и водорода равны соответственно 53,33, 31,11 и 15,5%. Вывести молекулярную формулу. Массовые
- 16. Задачи на растворы
- 17. В 300 г воды растворили 20 г глюкозы. Определите массовую долю глюкозы в полученном растворе. Вычислите
- 18. Из 10 кг раствора с массовой долей хлорида натрия 20% при охлаждении выделилось 400г. соли. Чему
- 19. Какую массу раствора с массовой долей гидроксида калия 20% надо прибавить к 1 кг раствора с
- 20. Вычислить среднюю скорость реакции CO + NO2 = CO2 + NO если начальная концентрация CO была
- 21. Задачи по теме скорость химических реакций
- 22. Как изменится скорость химической реакции при повышении температуры реакционной смеси от 20 градусов до 50, если
- 23. Во сколько раз изменится скорость реакции, уравнение которой 2NO + O2 = 2NO2 При увеличении концентрации
- 24. При температуре 20 градусов некоторая реакция заканчивается через 40 минут. Вычислить, через сколько минут закончится эта
- 25. Вычислите как изменится скорость реакции: а) при повышении температуры на 30 градусов. б) при понижении температуры
- 27. Скачать презентацию























 Prezentatsia_Microsoft_PowerPoint
Prezentatsia_Microsoft_PowerPoint Карбоновые кислоты
Карбоновые кислоты Скорость химической реакции
Скорость химической реакции Межкристаллитная коррозия МКК
Межкристаллитная коррозия МКК Стерилизация технологических потоков и оборудования
Стерилизация технологических потоков и оборудования Научно-познавательное шоу Юный химик
Научно-познавательное шоу Юный химик Алканы
Алканы Основные классы неорганических соединений. Гидроксиды
Основные классы неорганических соединений. Гидроксиды Аспирин и его влияние на организм человека
Аспирин и его влияние на организм человека Алканы
Алканы Альдегиды. Строение молекул
Альдегиды. Строение молекул Техника безопасности при использовании различных видов топлива. Практическая работа № 3
Техника безопасности при использовании различных видов топлива. Практическая работа № 3 Сахароза (С12Н22О11)
Сахароза (С12Н22О11) Алюминий
Алюминий Презентация на тему Экологические риски при добыче и переработке нефти
Презентация на тему Экологические риски при добыче и переработке нефти  Дополнительный_материал_09.14_19.10.2022_b0aaa559
Дополнительный_материал_09.14_19.10.2022_b0aaa559 98675992
98675992 Классификация спиртов. Изомерия спиртов
Классификация спиртов. Изомерия спиртов Ионные уравнения реакций
Ионные уравнения реакций Презентация на тему Вопросы от …
Презентация на тему Вопросы от …  Классификация и номенклатура аминов. 11 класс
Классификация и номенклатура аминов. 11 класс Презентация на тему Оксиды
Презентация на тему Оксиды  06_Типы_химических_реакций_в_органической_химии
06_Типы_химических_реакций_в_органической_химии Гибридизация АО. Пространственное строение молекул (геометрия молекул)
Гибридизация АО. Пространственное строение молекул (геометрия молекул) Ионы кальция, как важное звено в нейроцитотоксическом действии кадмия
Ионы кальция, как важное звено в нейроцитотоксическом действии кадмия Строение электронной оболочки атома часть 2
Строение электронной оболочки атома часть 2 Основные законы и понятия химии. Основные классы неорганических соединений. Химический эквивалент. Закон эквивалентов
Основные законы и понятия химии. Основные классы неорганических соединений. Химический эквивалент. Закон эквивалентов Окислительновосстановительные процессы
Окислительновосстановительные процессы