Содержание
- 2. Цели урока: познакомить учащихся с природными соединениями металлов. Сформировать понятия о самородных металлах, минералах и рудах.
- 3. Проблемный вопрос: Могут ли металлы находиться в природе в свободном(или самородном) состоянии, т.е. в виде М
- 4. Металлы могут встречаться в природе или в виде простого вещества(самородка) или в виде сложного вещества это
- 5. Природные образования, содержащие минералы металлов, пригодные для промышленного получения из них металлов, называют рудами. Железная руда
- 6. - Как вы думаете, какой основной химический процесс лежит в основе получения металлов? Ответ: Большинство металлов
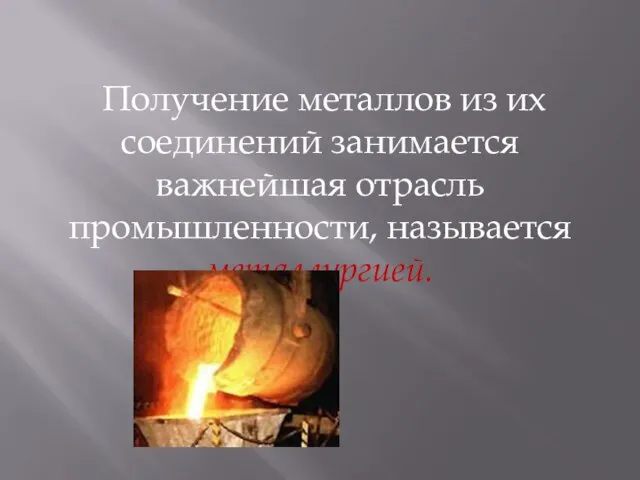
- 7. Получение металлов из их соединений занимается важнейшая отрасль промышленности, называется металлургией.
- 8. Общие способы получения металлов Пирометаллургия Гидрометаллургия Электрометаллургия Термическое разложение соединений Микробиологический
- 9. ПИРОМЕТАЛЛУРГИЯ – это методы извлечения металлов из руд под действием высоких температур. Сульфидные руды подвергают обжигу:
- 10. ГИДРОМЕТАЛЛУРГИЯ – методы получения металлов, основанные на химических реакциях, происходящих в растворах. CuS+4H2SO4=CuSO4+4SO2+4H2O Конц. CuSO4+Fe=FeSO4+Cu Этим
- 11. ЭЛЕКТРОМЕТАЛЛУРГИЯ – выделение металлов из их солей и оксидов под действием электрического тока. электролиз 2Al2O3=4Al+3O2 электролиз
- 12. ТЕРМИЧЕСКОЕ РАЗЛОЖЕНИЕ СОЕДИНЕНИЙ: так получают Ме в особо чистой форме: титан, цирконий, торий – из галогеноидов,
- 13. МИКРОБИОЛОГИЧЕСКИЙ МЕТОД: например тионовые бактерии способны переводить нерастворимые сульфиды в растворимые сульфаты. Серные пузыри. Микробиологи обнаружили
- 14. Закрепление новых знаний и способов действия. Закрепление знаний решение задач по теме «Металлы», упр. 1-3. Домашнее
- 15. Рефлексия. Я считаю, что прошедший урок был…. На уроке мне понравилось….. Мне это пригодится…..
- 17. Скачать презентацию












 Эмульсия. Основные типы эмульсий
Эмульсия. Основные типы эмульсий Квантовая химия
Квантовая химия Алкены Бутен
Алкены Бутен Металлы
Металлы Химический диктант по органической химии. 9 класс
Химический диктант по органической химии. 9 класс Химические реакции. Классификация
Химические реакции. Классификация Знакомство с химией
Знакомство с химией Применение каучука
Применение каучука Неорганический мозговой штурм
Неорганический мозговой штурм Практическая работа: Очистка загрязнённой поваренной соли
Практическая работа: Очистка загрязнённой поваренной соли Буферные системы
Буферные системы Cеминар 6 -Алканы-2
Cеминар 6 -Алканы-2 Химические реакции
Химические реакции Электроосмос. Практическое применение электроосмоса
Электроосмос. Практическое применение электроосмоса Магматические горные породы
Магматические горные породы 1_
1_ Физические и химические свойства металлов
Физические и химические свойства металлов Строение электронных оболочек атома
Строение электронных оболочек атома Железо
Железо Производные салициловой, пара-аминобензойной кислот, применяемые в медицине
Производные салициловой, пара-аминобензойной кислот, применяемые в медицине коррозия металлов
коррозия металлов Индикаторная бумага
Индикаторная бумага Тренажер - Валентность. 8 класс
Тренажер - Валентность. 8 класс Потенциометрический анализ, титрование
Потенциометрический анализ, титрование Алкины
Алкины Лучший тест для подготовки к ЕГЭ по химии
Лучший тест для подготовки к ЕГЭ по химии Тривиальные названия веществ, наиболее часто встречаемых в ЕГЭ
Тривиальные названия веществ, наиболее часто встречаемых в ЕГЭ Блок колонн на установке замедленного коксования производительностью 730000 тонн/год гудрона (поз.к-1, кх-1)
Блок колонн на установке замедленного коксования производительностью 730000 тонн/год гудрона (поз.к-1, кх-1)