Содержание
- 2. Какие из химических реакций являются обратимыми? 1. NaOH + HCl ? NaCl + H2O 2. N2
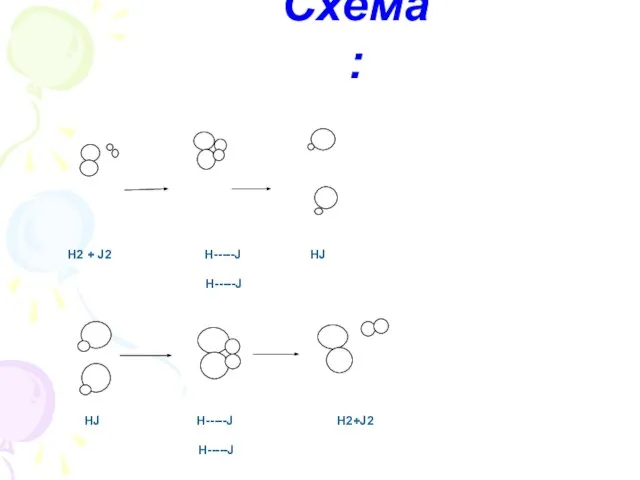
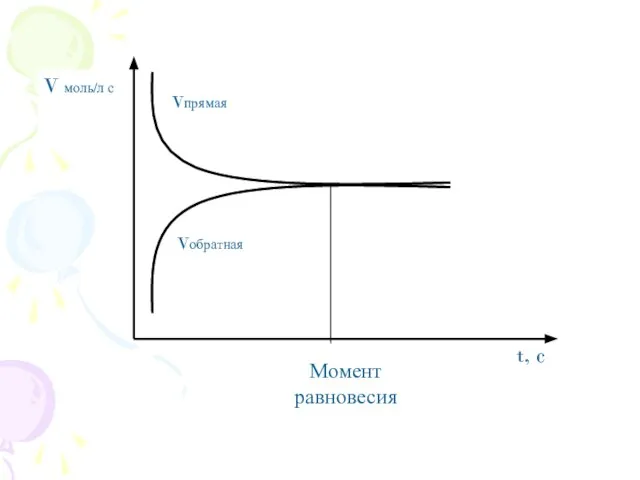
- 3. Схема: Н2 + J2 Н-----J HJ Н-----J HJ Н-----J H2+J2 Н-----J
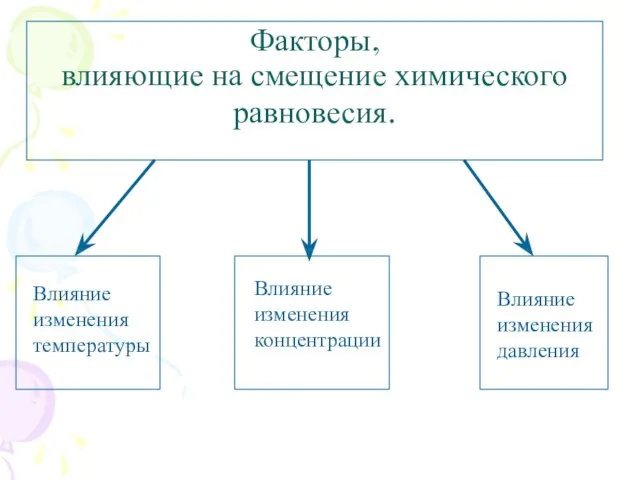
- 5. Факторы, влияющие на смещение химического равновесия.
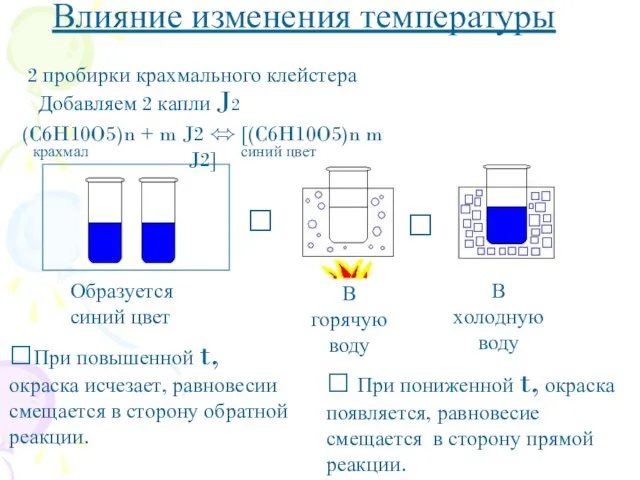
- 6. ? ? Влияние изменения температуры 2 пробирки крахмального клейстера Добавляем 2 капли J2 ?При повышенной t,
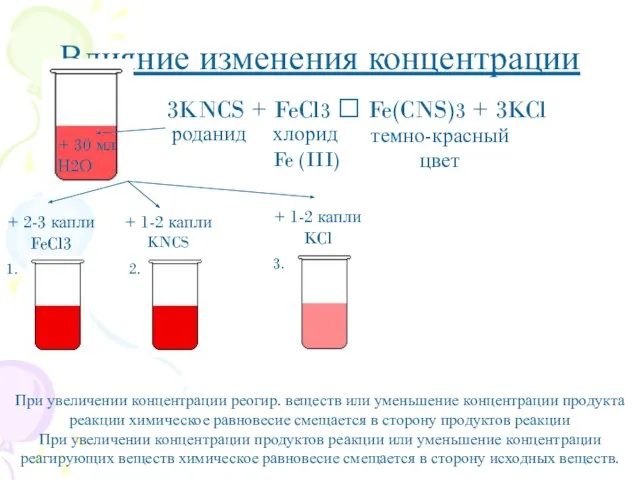
- 7. Влияние изменения концентрации + 2-3 капли FeCl3 + 1-2 капли KNCS + 1-2 капли KCl При
- 8. Влияние изменения давления 2NO2 ⬄ N2O4 + Q При расширении цвет газа стал темно-бурым, а равновесие
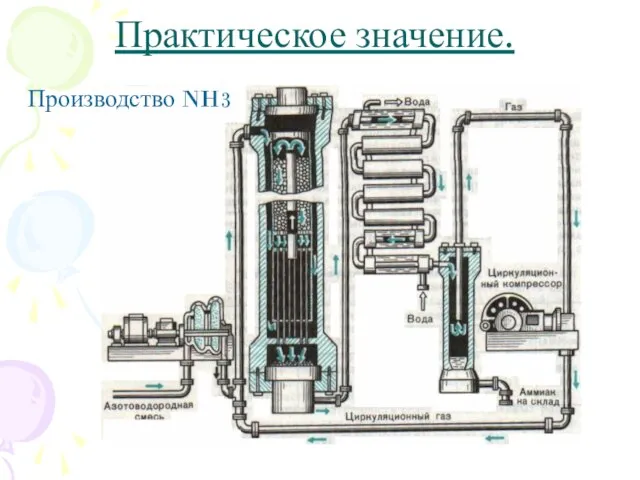
- 9. Практическое значение. Производство NH3
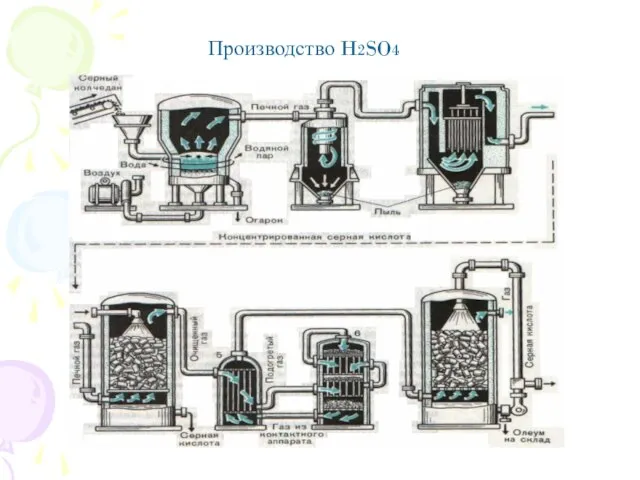
- 10. Производство H2SO4
- 11. Производство HNO3
- 12. 1.Смещение химического равновесия обеспечивает высокий выход желаемого продукта. 2. Открывает путь к управлению химическими реакциями.
- 14. Скачать презентацию




 Свойства кислорода. Оксиды
Свойства кислорода. Оксиды Задача №8: Не тормози. Команда: Карбораны
Задача №8: Не тормози. Команда: Карбораны Натуральный каучук
Натуральный каучук Электростанция в кармане
Электростанция в кармане Железо. Физические свойства
Железо. Физические свойства Общая характеристика неметаллов подгруппы кислород
Общая характеристика неметаллов подгруппы кислород Полимеры
Полимеры Смог як хімічне явище
Смог як хімічне явище Презентация на тему Классы неорганических веществ
Презентация на тему Классы неорганических веществ  Массовая доля элемента в веществе
Массовая доля элемента в веществе Химия и производство
Химия и производство Стеклообразование, структура и свойства стекол системы Na2O – B2O3 – SiO2 на основе комплексного борсодержащего сырья
Стеклообразование, структура и свойства стекол системы Na2O – B2O3 – SiO2 на основе комплексного борсодержащего сырья Использование информационноко-ммуникационных технологий по формированию УУД на уроках химии
Использование информационноко-ммуникационных технологий по формированию УУД на уроках химии Алкины. Ацетилен
Алкины. Ацетилен Оксиды
Оксиды Непредельные углеводороды
Непредельные углеводороды Наркотики и прекурсоры
Наркотики и прекурсоры Повторение классов соединений. Составление формул по названиям
Повторение классов соединений. Составление формул по названиям Основные классы неорганических соединений
Основные классы неорганических соединений Презентация на тему Степень окисления
Презентация на тему Степень окисления  Кислоты основания и соли как электролиты
Кислоты основания и соли как электролиты 14257fc50bc406ef33f49ad14aa3f48b
14257fc50bc406ef33f49ad14aa3f48b Химия и производство
Химия и производство Реакции разложения
Реакции разложения Химическая кибернетика
Химическая кибернетика Титриметрический анализ. Основные понятия
Титриметрический анализ. Основные понятия Метод окислительно - восстановительного титрования
Метод окислительно - восстановительного титрования Химия на войне
Химия на войне