Содержание
- 2. Комплексными называют соединения, содержащие сложные ионы и молекулы, способные к существованию как в кристаллическом виде, так
- 3. СТРОЕНИЕ КОМПЛЕКСНОГО СОЕДИНЕНИЯ K3 [Fe(CN)6] Ион- Комплексо- образователь Лиганды Координационное число Внутренняя сфера Внешняя сфера [Cu(NH3)4]Cl2
- 4. Комплексообразователь (центральный ион) – частица (атом, ион или молекула), координирующая (располагающая) вокруг себя другие ионы или
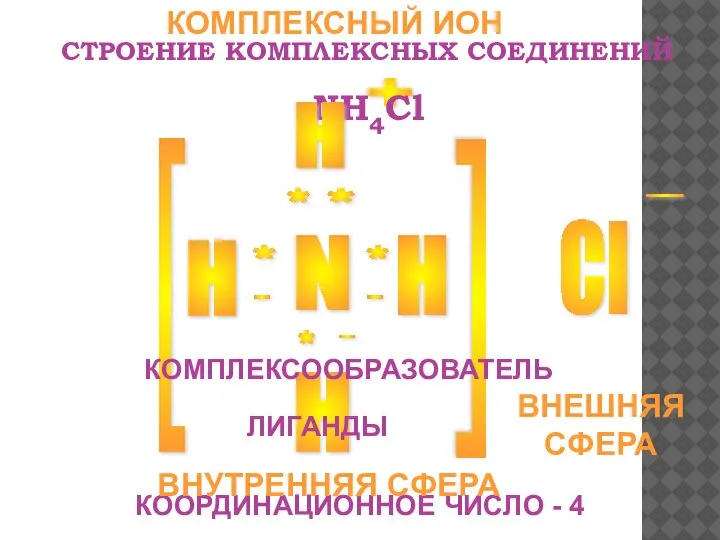
- 5. СТРОЕНИЕ КОМПЛЕКСНЫХ СОЕДИНЕНИЙ N H H H Cl + - [ [ * * * *
- 6. ЛИГАНДАМИ МОГУТ БЫТЬ: А) ПОЛЯРНЫЕ МОЛЕКУЛЫ: NH3 , H2O , CO , NO Б) ПРОСТЫЕ ИОНЫ:
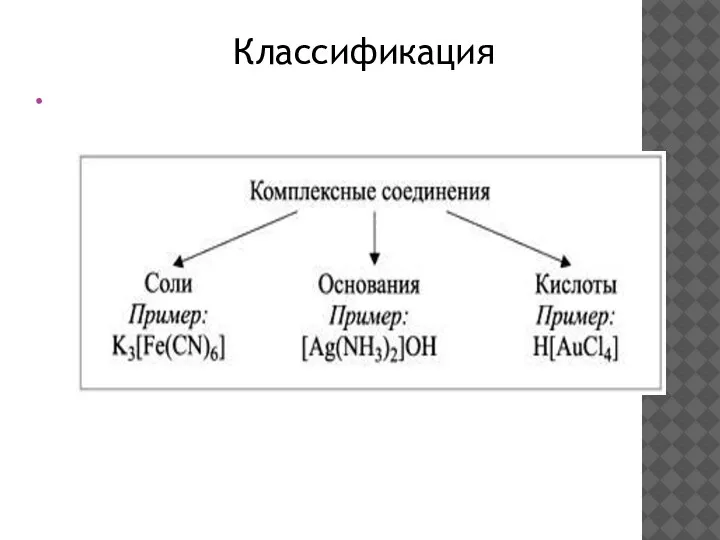
- 7. Классификация 1) По составу.
- 8. 2) По заряду внутренней сферы.
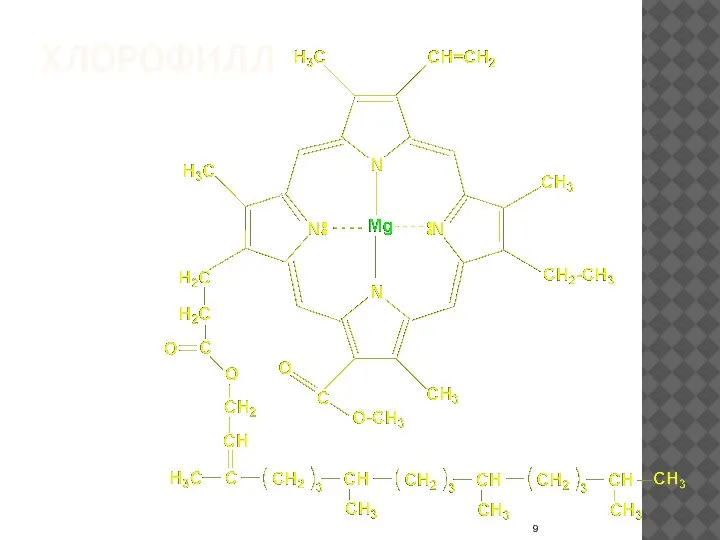
- 9. ХЛОРОФИЛЛ
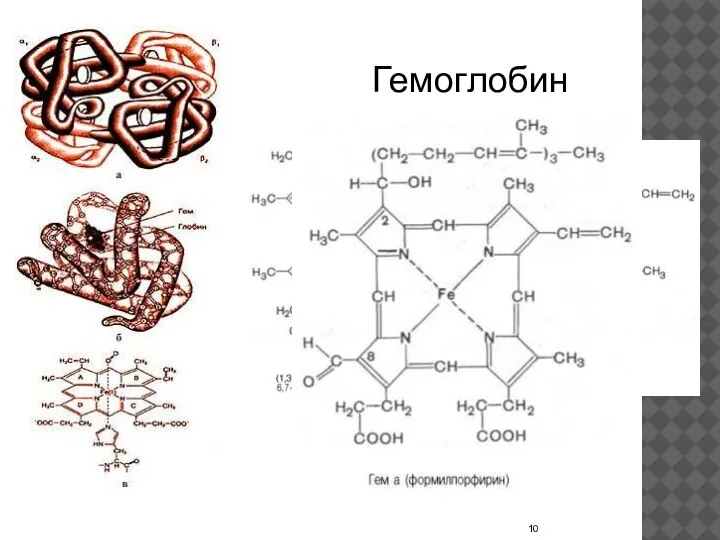
- 10. Гемоглобин
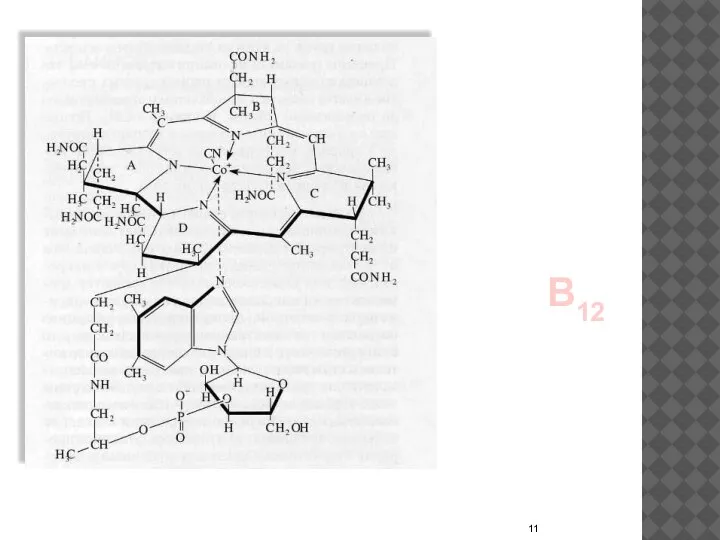
- 11. B12
- 12. ХИМИЧЕСКИЕ СВОЙСТВА КС 1. Диссоциация комплексных соединений K3[Fe(CN)6] = 3K+ + [Fe(CN)6]3- [Cu(NH3)4]SO4 = [Cu(NH3)4]2+ +
- 13. ХИМИЧЕСКИЕ СВОЙСТВА КС 2. Реакции по внешней сфере K3[Fe(CN)6]+ FeCl2= KFe[Fe(CN)6]+2KCl [Cu(NH3)4]SO4 + BaCl2= [Cu(NH3)4]Cl2 +
- 14. ХИМИЧЕСКИЕ СВОЙСТВА КС 3. Реакции с участием лигандов [Cu(NH3)4]SO4 + 4HCl= 4NH4Cl + CuSO4
- 15. ХИМИЧЕСКИЕ СВОЙСТВА КС 4. Реакции по центральному иону [Ag(NH3)2]Cl + KI= AgI + NH3 + KCl
- 17. Скачать презентацию

![СТРОЕНИЕ КОМПЛЕКСНОГО СОЕДИНЕНИЯ K3 [Fe(CN)6] Ион- Комплексо- образователь Лиганды Координационное число Внутренняя](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/930130/slide-2.jpg)



![ХИМИЧЕСКИЕ СВОЙСТВА КС 1. Диссоциация комплексных соединений K3[Fe(CN)6] = 3K+ + [Fe(CN)6]3-](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/930130/slide-11.jpg)
![ХИМИЧЕСКИЕ СВОЙСТВА КС 2. Реакции по внешней сфере K3[Fe(CN)6]+ FeCl2= KFe[Fe(CN)6]+2KCl [Cu(NH3)4]SO4](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/930130/slide-12.jpg)
![ХИМИЧЕСКИЕ СВОЙСТВА КС 3. Реакции с участием лигандов [Cu(NH3)4]SO4 + 4HCl= 4NH4Cl + CuSO4](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/930130/slide-13.jpg)
![ХИМИЧЕСКИЕ СВОЙСТВА КС 4. Реакции по центральному иону [Ag(NH3)2]Cl + KI= AgI + NH3 + KCl](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/930130/slide-14.jpg)
 кулонометрия Дастан
кулонометрия Дастан Методы отбора проб воды. Оформление и подготовка к анализу, протокол исследования воды, определение рН
Методы отбора проб воды. Оформление и подготовка к анализу, протокол исследования воды, определение рН Кремнийорганическая гипотеза
Кремнийорганическая гипотеза Известняк. Разновидности известняка. Области применения
Известняк. Разновидности известняка. Области применения Строение атома
Строение атома Галогеноводородные кислоты
Галогеноводородные кислоты Сухой метод определения глюкозы. Глюкометры
Сухой метод определения глюкозы. Глюкометры Современные сплавы на основе циркония
Современные сплавы на основе циркония Комплексное задание по дисциплине основы материаловедения для группы 18
Комплексное задание по дисциплине основы материаловедения для группы 18 Соли
Соли Минералы и горные породы
Минералы и горные породы lektsia_6 (1)
lektsia_6 (1) Подготовка к контрольной работе химические реакции 8 класс
Подготовка к контрольной работе химические реакции 8 класс Азотосодержащие соединения: Амины. Аминокислоты. Белки
Азотосодержащие соединения: Амины. Аминокислоты. Белки Угольная кислота и её соли
Угольная кислота и её соли Комплексные соединения
Комплексные соединения Альдегиды, строение и свойства
Альдегиды, строение и свойства Презентация на тему Алкены. Строение. Изомерия. Химические свойства. Получение
Презентация на тему Алкены. Строение. Изомерия. Химические свойства. Получение  Распределение электронов в атомах
Распределение электронов в атомах Разработка системы подготовки лаборанта химического анализа
Разработка системы подготовки лаборанта химического анализа Пищевые добавки: вред и польза
Пищевые добавки: вред и польза Строение и функции нуклеиновых кислот. Лекция №3
Строение и функции нуклеиновых кислот. Лекция №3 Исследование биодеградации полимерных материалов методом АСМ
Исследование биодеградации полимерных материалов методом АСМ Коррозия металлов
Коррозия металлов Кислород. Физические и химические свойства. Получение
Кислород. Физические и химические свойства. Получение Классификация сложных неорганических веществ. Оксиды
Классификация сложных неорганических веществ. Оксиды Виготовлення водних розчинів з заданою масовою часткою розчиненої речовини
Виготовлення водних розчинів з заданою масовою часткою розчиненої речовини Стелс-материалы
Стелс-материалы