Содержание
- 2. Состав Кислоты - это сложные вещества, в молекулах которых содержат атомы водорода и кислотный остаток H-R,
- 3. Классификация кислот Одноосновные кислоты, например, HCl, HNO3 (отщепляют при диссоциации один атом водорода) Многоосновные кислоты, например,
- 4. Разбавление серной кислоты Относительно смешивания серной кислоты с водой с давних пор существует строгое правило: «Сначала
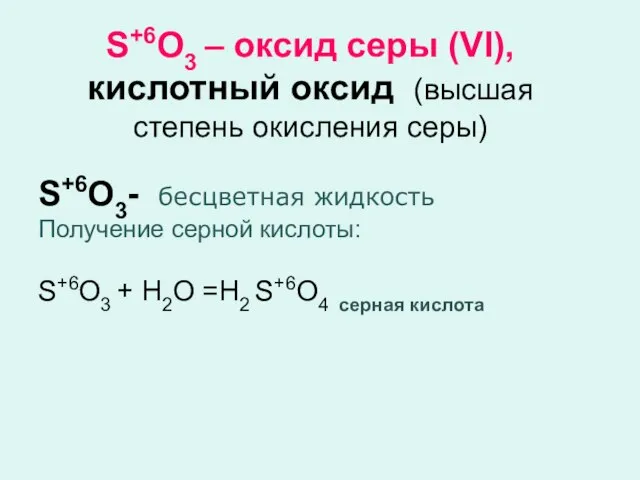
- 5. S+6O3 – оксид серы (VI), кислотный оксид (высшая степень окисления серы) S+6O3- бесцветная жидкость Получение серной
- 6. Химические свойства серной кислоты разбавленная серная кислота проявляет все характерные свойства кислот: С оксидами металлов.(реакция обмена)
- 7. Качественная реакция на ион –SO42- Реактивом на серную кислоту и ее соли является катион бария ,
- 8. Концентрированная серная кислота Ме+Н2SO4(кoнц)→МеSO4+H2O+(Н2S,S,SO2) Серная кислота(конц) восстанавливается до (Н2S,S,SO2) в зависимости от активности металла и условий
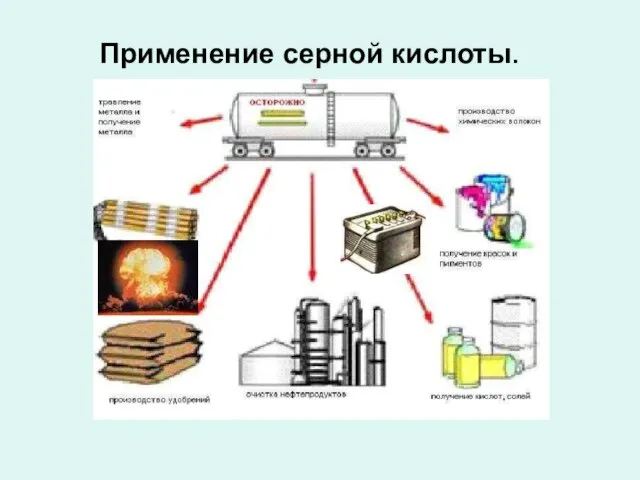
- 9. Применение серной кислоты.
- 10. Сульфат натрия.
- 11. Сульфат никеля
- 12. Сульфат меди дать классификацию химическим реакциям.
- 14. Скачать презентацию








 Презентация на тему Окислительно-восстановительные реакции
Презентация на тему Окислительно-восстановительные реакции  Презентация на тему Сложные эфиры. Жиры
Презентация на тему Сложные эфиры. Жиры  Пентоза - відновлювальна сировина для синтезу фуранових сполук
Пентоза - відновлювальна сировина для синтезу фуранових сполук Дождь из облака
Дождь из облака По страницам истории российской химической науки
По страницам истории российской химической науки Явление хемилюменисценции
Явление хемилюменисценции Сложные вещества кислоты
Сложные вещества кислоты Что изучает химия?
Что изучает химия? Окислительно-восстановительные реакции. Классификация ОВР
Окислительно-восстановительные реакции. Классификация ОВР Термодинамика. Основные понятия и законы. Особенности термодинамики живых систем
Термодинамика. Основные понятия и законы. Особенности термодинамики живых систем Аналитический обзор по теме Процесс разложения аммиака
Аналитический обзор по теме Процесс разложения аммиака Презентация на тему Игра «Путешествие в страну Атомолия»
Презентация на тему Игра «Путешествие в страну Атомолия»  Белки
Белки Углеводороды. Общие знания
Углеводороды. Общие знания Ca КАЛЬЦИЙ
Ca КАЛЬЦИЙ Органическая химия. Йенс Якоб Берцелиус (1779 - 1848)
Органическая химия. Йенс Якоб Берцелиус (1779 - 1848) Презентация на тему Альдегиды (10 класс)
Презентация на тему Альдегиды (10 класс)  Щелочные металлы
Щелочные металлы Жесткость воды и способы ее устранения
Жесткость воды и способы ее устранения Презентация на тему Валентность и степень окисления (8 класс)
Презентация на тему Валентность и степень окисления (8 класс)  Основной государственный экзамен. Химия 2022. Задание 2
Основной государственный экзамен. Химия 2022. Задание 2 Своя игра. Атомы
Своя игра. Атомы ИКТ как средство реализации проблемного обучения на уроках химии
ИКТ как средство реализации проблемного обучения на уроках химии Алюминий. Применение
Алюминий. Применение Хлороводород и соляная кислота
Хлороводород и соляная кислота Химические свойства оксидов
Химические свойства оксидов Химическая связь. Строение вещества
Химическая связь. Строение вещества Презентация на тему Основания и их классификация
Презентация на тему Основания и их классификация