Содержание
- 2. Цель урока: познакомиться с историей открытия и распространением щелочных металлов в природе и живых организмах; изучить
- 3. Металлы Сu, Au, Ag не взаимодействуют с водой даже при нагревании. Металлы обладают электропроводностью и теплопроводностью.
- 7. История открытия Нахождение в природе Нахождение в живых объектах природы Физические свойства, особенности строения атомов Химические
- 8. В ЧЁМ УНИКАЛЬНОСТЬ ЩЕЛОЧНЫХ МЕТАЛЛОВ?
- 9. ИСТОРИКИ
- 10. ЛИТИЙ (Lithium) 3Li Литий – самый лёгкий серебристо – белый металл. Открыт в 1817 году шведским
- 11. Вскоре Арфведсон обнаружил литий в сподумене LiAl[Si2O6], позже ставшем важнейшим минералом элемента № 3. В 1818
- 12. НАТРИЙ (Natrium)11Na Натрий – мягкий, серебристо – белый металл. В чистом виде получен при электролизе едкого
- 13. КАЛИЙ (Kalium) 19K Калий – серебристо-белый, очень мягкий и легкоплавкий металл. Получен при электролизе едкого кали
- 14. РУБИДИЙ (Rubidium) 37Rb Рубидий – лёгкий и очень мягкий (как воск),серебристо-белый металл. Открыт в 1861 году
- 15. ЦЕЗИЙ (Caesium) 55Cs Блестящая поверхность цезия имеет бледно-золотистый цвет. В 1860 году немецкие учёные Р. Бунзен
- 16. Цезий, как известно, был первым элементом, открытым с помощью спектрального анализа, разработанного в 1859 году немецкими
- 17. Франций (Franium) 87Fr Возможность существования и основные свойства элемента №87 были предсказаны Д.И.Менделеевым. В 1871 году
- 18. Первое сообщение об открытии 87-элемента как продукта радиоактивного распада актиния-228 сделал в 1913 году английский химик
- 19. ГЕОЛОГИ
- 20. Нахождение в природе Натрий и калий широко распространены в природе в виде солей Соединения других щелочных
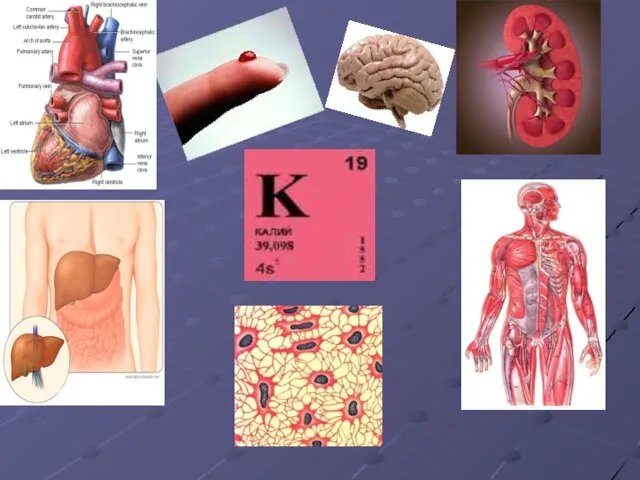
- 21. БИОЛОГИ
- 25. Среднее содержание в организме человека 608мг. Суточная потребность 1.5-6мг.
- 26. Суточная потребность 0,004-0,03мг
- 27. В организме человека не содержится.
- 28. ФИЗИКИ
- 29. ХИМИКИ
- 30. ТЕХНОЛОГИ - ПРАКТИКИ
- 31. LI
- 32. Na
- 33. K
- 34. Rb
- 35. Cs
- 36. Франций . Последний член семейства щелочных металлов франций настолько радиоактивен, что его нет в земной коре
- 37. Правильные ответы Б В Г В А
- 38. Согласны синий Не согласны красный
- 39. ИТОГОВАЯ ОЦЕНКА 10 – 12 баллов 5 8 – 10 баллов 4 6 – 8 баллов
- 40. ПАРАД МЕТАЛЛОВ, КАК ПАРАД ПЛАНЕТ, НЕТ ГЛАВНЫХ И ВТОРОСТЕПЕННЫХ НЕТ. МЕТАЛЛЫ РАЗНЫЕ ПО-СВОЕМУ ВАЖНЫ И В
- 42. Скачать презентацию







![Вскоре Арфведсон обнаружил литий в сподумене LiAl[Si2O6], позже ставшем важнейшим минералом элемента](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/291668/slide-10.jpg)


























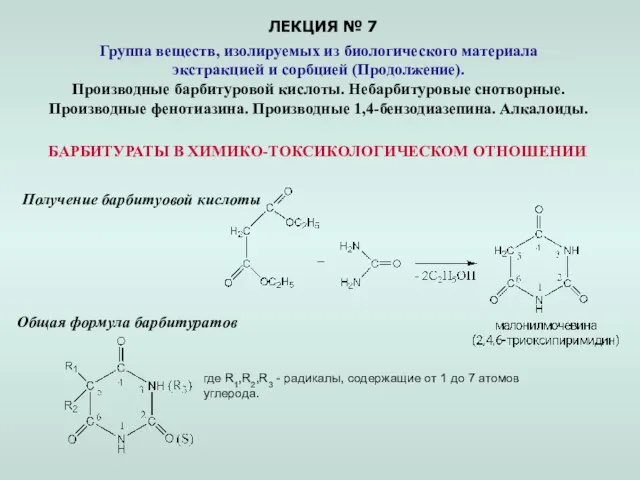 Презентация по Химии "Группа веществ, изолируемых из биологического материала экстракцией и сорбцией"
Презентация по Химии "Группа веществ, изолируемых из биологического материала экстракцией и сорбцией"  Элемент протактиний
Элемент протактиний Презентация на тему Аминокислоты
Презентация на тему Аминокислоты  Презентация на тему Атомная энергетика
Презентация на тему Атомная энергетика  Вода – уникальное вещество на планете Земля
Вода – уникальное вещество на планете Земля Золь. Свойства золи
Золь. Свойства золи Электролиз
Электролиз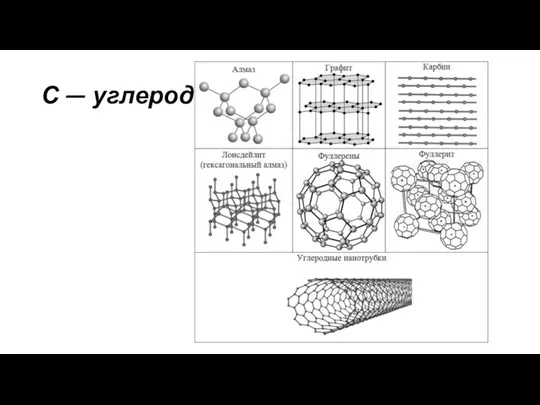 С - углерод. Применение
С - углерод. Применение Окислительно-восстаовительные реакции
Окислительно-восстаовительные реакции Алкены
Алкены 9 урок простые и сложные вещества
9 урок простые и сложные вещества Взаимодействие металлов с водой, щелочами, кислотами, солями, простыми веществами
Взаимодействие металлов с водой, щелочами, кислотами, солями, простыми веществами Презентация на тему Строение атома
Презентация на тему Строение атома  Химия в моей специальности
Химия в моей специальности Химическая мастерская
Химическая мастерская Строение вещества
Строение вещества Металлы. Общая характеристика ( 9 класс)
Металлы. Общая характеристика ( 9 класс) Заманауи косметика биотехнологиясы
Заманауи косметика биотехнологиясы Применение алкенов
Применение алкенов Соли азотной кислоты
Соли азотной кислоты Катаболизм пуриновых нуклеотидов
Катаболизм пуриновых нуклеотидов Основания. Щелочи – растворимые основания
Основания. Щелочи – растворимые основания Основания, их классификация и свойства
Основания, их классификация и свойства Закон сохранения массы веществ
Закон сохранения массы веществ Плотность вещества
Плотность вещества Химико-аналитический контроль
Химико-аналитический контроль Химик белемнәрне тормышта куллану
Химик белемнәрне тормышта куллану Алканы – строение, химические свойства
Алканы – строение, химические свойства