Содержание
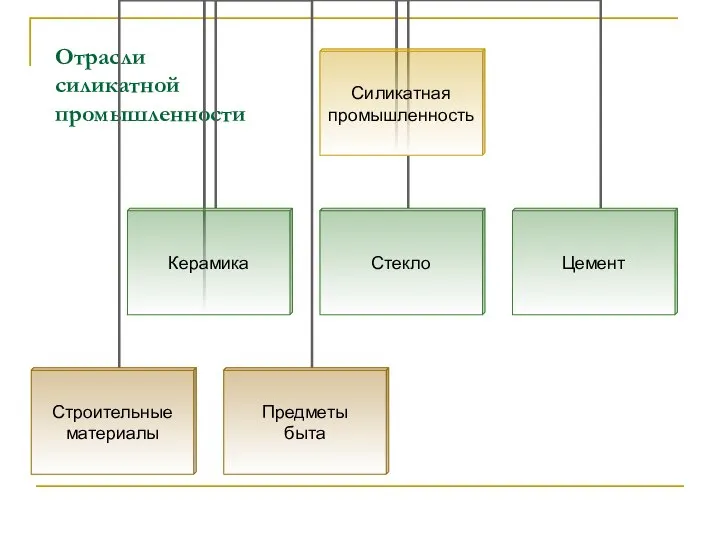
- 2. Отрасли силикатной промышленности
- 3. Выставочный зал №1 « Керамика» Изделия из красной глины Горшечники. Древнеегипетская настенная роспись. Греческая ваза.V век
- 4. Сырьё: Глина. В её состав входит каолин(AI2O3.2SiO2.2H2O) и в виде механических примесей песок(SiO2) и известняк (CaCO3).
- 5. Изделия из белой глины. Фарфор. Родина фарфора – Китай.
- 6. В России производство фарфора было налажено на императорском заводе под Петербургом в 1746 году. Фарфор. Надглазурная
- 7. Признаки фарфора: тонкость изделия, белый цвет, отсутствие пористости, термическая и химическая прочность. Изделия Дулёвского фарфорового завода.
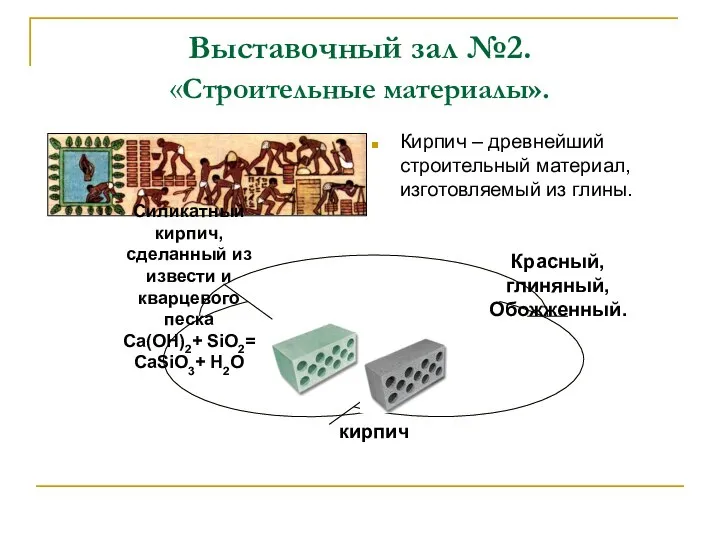
- 8. Выставочный зал №2. «Строительные материалы». Кирпич – древнейший строительный материал, изготовляемый из глины.
- 9. Производство цемента «Цемент» в переводе с латинского означает битый камень. Портландцемент запатентован в Англии в 1824
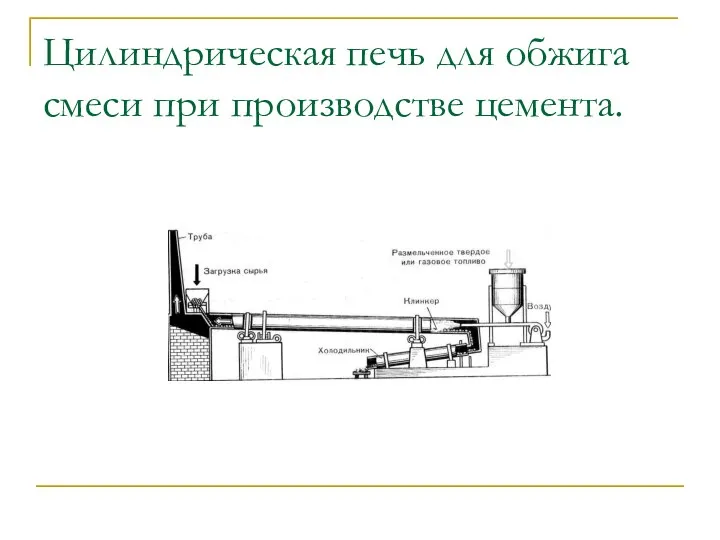
- 10. Цилиндрическая печь для обжига смеси при производстве цемента.
- 11. Химические реакции, лежащие в основе производства. Обезвоживание каолина: AI2O3.2SiO2.2H2O=AI2O3.2SiO2 +2H2O Разложение известняка: CaCO3=CaO+CO2 Образование силикатов и
- 12. Выставочный зал №3. « Стекло». Оконное стекло. Для его изготовления берут только чистый кварцевый песок, соду
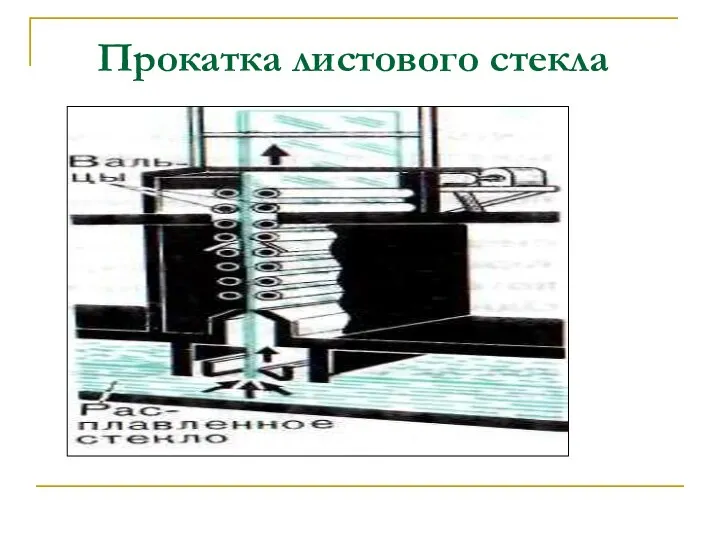
- 13. Прокатка листового стекла
- 14. Виды стекла: Химическое стекло. Если вместо соды взять поташ(K2CO3), то получается более тугоплавкое стекло. Его используют
- 15. Хрустальное стекло В качестве сырья берут поташ (K2CO3),оксид свинца(II),кварцевый песок( SiO2). Стекло сильно преломляет свет, имеет
- 16. Цветные стёкла. Красители: синее стекло-оксид кобальта(CoO), зелёное стекло-оксид хрома(III)(Cr2O3), жёлтое стекло-оксид железа(III)(Fe2O3). При добавлении мелкораздробленного золота
- 17. Жидкое стекло. Это концентрированные растворы силикатов натрия и калия. Их получают сплавлением песка с карбонатами или
- 18. Бисер – мелкие бусинки с отверстиями для продевания нитки. Применяется для украшения 6000 лет. Самый лучший
- 19. Контрольное задание: 1.Из предложенного списка выбрать формулы оконного стекла, химического стекла, мела, соды, известняка, песка. а/
- 20. Проверь себя: 1.оконного стекла – б, химического стекла –д, мела – а, соды – г, известняка
- 22. Скачать презентацию















 Водородная химическая связь
Водородная химическая связь Ионные реакции
Ионные реакции Периодическая система химических элементов Д.И. Менделеева
Периодическая система химических элементов Д.И. Менделеева Получение металлов
Получение металлов Презентация на тему Применение солей в быту
Презентация на тему Применение солей в быту  Полимеры. Применение
Полимеры. Применение Закономерности протеканий химических реакций
Закономерности протеканий химических реакций Строение, свойства, биологическая роль дезоксисахаров и аминосахаров
Строение, свойства, биологическая роль дезоксисахаров и аминосахаров Процессы в растворах: электролитическая диссоциация (ЭД)
Процессы в растворах: электролитическая диссоциация (ЭД) Степень окисления. Составление химических формул бинарных соединений
Степень окисления. Составление химических формул бинарных соединений Лекция 1
Лекция 1 Аминокислоты. Викторина
Аминокислоты. Викторина Презентация на тему "Азотная кислота"
Презентация на тему "Азотная кислота" Общие способы получения металлов
Общие способы получения металлов Физические и химические свойства металлов
Физические и химические свойства металлов Сложные эфиры
Сложные эфиры Примеры реакций в жизни и в быту
Примеры реакций в жизни и в быту Презентация на тему Количество вещества
Презентация на тему Количество вещества  Полисахариды. Крахмал и целлюлоза
Полисахариды. Крахмал и целлюлоза Счастливый случай
Счастливый случай Презентация на тему Знаешь ли ты классы неорганических веществ
Презентация на тему Знаешь ли ты классы неорганических веществ  Кислородосодержащие органические соединения. Cпирты (алканолы)
Кислородосодержащие органические соединения. Cпирты (алканолы) Химические формулы. Относительная молекулярная масса. 8 класс
Химические формулы. Относительная молекулярная масса. 8 класс Решение задач на смеси, растворы и сплавы
Решение задач на смеси, растворы и сплавы Лекция 3
Лекция 3 Харктеристика металлов
Харктеристика металлов Строение вещества
Строение вещества Растворы. Лекция 7
Растворы. Лекция 7