Содержание
- 2. ОСНОВНІ ПРАВИЛА ТЕХНІКИ БЕЗПЕКИ ПІД ЧАС РОБОТИ В КАБІНЕТІ ХІМІЇ: I1. Виконуйте тільки ті досліди, що
- 3. ПРАВИЛА ПОЖЕЖНОЇ БЕЗПЕКИ: 1. Посуд, в якому спалахнула рідина (бензин, гас, ацетон, скипидар, ефір, спирт, бензол),
- 4. Органічних сполук значно більше за кількістю, ніж неорганічних. На цю закономірність учені-хіміки звернули увагу давно. Тривалий
- 5. Цінними джерелами різних органічних сполук є також продукти сухої перегонки кам’яного вугілля — коксовий газ, кам’яновугільна
- 6. ЗАПОВНІТЬ ТАБЛИЦЮ САМОСТІЙНО
- 7. Предмет органічної хімії Кекулє в 1851 р. визначив органічну хімію як хімію сполук Карбону. Однак це
- 8. Це приклади органічних сполук. Рисочками позначені зв,язки. Це називається- структурні формули. Зверніть увагу з яких елементів
- 13. Скачать презентацию
Слайд 2ОСНОВНІ ПРАВИЛА ТЕХНІКИ БЕЗПЕКИ ПІД ЧАС РОБОТИ В КАБІНЕТІ ХІМІЇ:
I1. Виконуйте тільки
ОСНОВНІ ПРАВИЛА ТЕХНІКИ БЕЗПЕКИ ПІД ЧАС РОБОТИ В КАБІНЕТІ ХІМІЇ:
I1. Виконуйте тільки

ті досліди, що узгоджені з учителем.
2. Забороняється брати речовини руками і пробувати її на смак.
3. Для визначення запаху речовини треба долонею зробити рух під отвору посудини до носа.
4, Відкривши склянку з реактивом, ставте пробку догори.
5. Посудину, з якої взято реактив, відразу закривайте пробкою і ставте на місце.
6. Надлишок узятого не зливайте (не зсипайте) у ту ж саму посудину, а лише у спеціальну посудину.
7. Під час нагрівання пробірок і колб з реактивами користуйтесь тримачем. Отвір посудини спрямовуйте в бік від тих, що працюють поруч.
8. Нагрівайте посудину з реактивом рівномірно, увесь об'єм рідини, не вище її рівня.
9. Не зазирайте в посудину, яку нагріваєте або в яку наливаєте раеактив.
10. Якщо кислота або луг потрапили на руки або одяг, негайно змийте їх великою кількістю води і повідомте про це вчителя.
11. Кислоту слід наливати у воду повільно, тонким струменем, переміщуючи; категорично забороняється наливати воду в кислоту.
2. Забороняється брати речовини руками і пробувати її на смак.
3. Для визначення запаху речовини треба долонею зробити рух під отвору посудини до носа.
4, Відкривши склянку з реактивом, ставте пробку догори.
5. Посудину, з якої взято реактив, відразу закривайте пробкою і ставте на місце.
6. Надлишок узятого не зливайте (не зсипайте) у ту ж саму посудину, а лише у спеціальну посудину.
7. Під час нагрівання пробірок і колб з реактивами користуйтесь тримачем. Отвір посудини спрямовуйте в бік від тих, що працюють поруч.
8. Нагрівайте посудину з реактивом рівномірно, увесь об'єм рідини, не вище її рівня.
9. Не зазирайте в посудину, яку нагріваєте або в яку наливаєте раеактив.
10. Якщо кислота або луг потрапили на руки або одяг, негайно змийте їх великою кількістю води і повідомте про це вчителя.
11. Кислоту слід наливати у воду повільно, тонким струменем, переміщуючи; категорично забороняється наливати воду в кислоту.
Слайд 3ПРАВИЛА ПОЖЕЖНОЇ БЕЗПЕКИ:
1. Посуд, в якому спалахнула рідина (бензин, гас, ацетон, скипидар,
ПРАВИЛА ПОЖЕЖНОЇ БЕЗПЕКИ:
1. Посуд, в якому спалахнула рідина (бензин, гас, ацетон, скипидар,

ефір, спирт, бензол), накривають скляною, фарфоровою посудиною більшою розміру або дерев'яними дошками тощо. Категорично забороняється задмухувати полум'я.
2. Розлиту на столі чи підлозі рідину, що зайнялася, засипають піском або накривають ковдрою. Не намагайтеся гасити полум'я водою. У разі великих пожеж застосовують вогнегасник.
3. Якщо на працівникові зайнявся одяг, його швидко аогортають ковдрою, залишаючи голову відкритою. Можна також зірвати палаючий одяг або направити на нього струмінь води. Однак найліпше качатися по підлозі чи землі. Не можна допускати, щоб потерпілий бігав, збивав полум'я руками, бо рух роздмухує полум'я.
2. Розлиту на столі чи підлозі рідину, що зайнялася, засипають піском або накривають ковдрою. Не намагайтеся гасити полум'я водою. У разі великих пожеж застосовують вогнегасник.
3. Якщо на працівникові зайнявся одяг, його швидко аогортають ковдрою, залишаючи голову відкритою. Можна також зірвати палаючий одяг або направити на нього струмінь води. Однак найліпше качатися по підлозі чи землі. Не можна допускати, щоб потерпілий бігав, збивав полум'я руками, бо рух роздмухує полум'я.
Слайд 4Органічних сполук значно більше за кількістю, ніж неорганічних. На цю закономірність учені-хіміки
Органічних сполук значно більше за кількістю, ніж неорганічних. На цю закономірність учені-хіміки

звернули увагу давно. Тривалий час органічні сполуки виділяли в окрему групу речовин, які можна одержати тільки з рослин або тварин та які утворюються під впливом таємничої життєвої сили «vis vitalis». Засновником теорії «віталізму» й органічної хімії як науки загалом уважають шведського вченого Й. Я. Берцеліуса. Теорія «віталізму» особливо наголошувала на істотних відмінностях між органічними й неорганічними речовинами, але проіснувала недовго. У 1828 році учень Берцеліуса К. Веллер синтезував з неорганічних речовин сечовину — речовину, безумовно, органічного походження.
Подальшому розвитку органічної хімії сприяли дослідження в галузі синтезу органічних речовин у пошуках нових матеріалів, барвників, ліків тощо.
Першими джерелами одержання органічних речовин були тваринні й рослинні організми, продукти їх життєдіяльності. Рослинний світ, особливо дерева, є головним виробником органічних речовин. Деревина є цінною сировиною для хімічної переробки. Так, суха перегонка деревини з давніх часів застосовувалася для одержання таких органічних речовин, як оцтова кислота, метиловий спирт, ацетон, феноли. Сьогодні хімічна переробка деревини використовується в паперовій промисловості, у виробництвах целюлози, штучного волокна, кінофотоплівки, етилового спирту та ін
Подальшому розвитку органічної хімії сприяли дослідження в галузі синтезу органічних речовин у пошуках нових матеріалів, барвників, ліків тощо.
Першими джерелами одержання органічних речовин були тваринні й рослинні організми, продукти їх життєдіяльності. Рослинний світ, особливо дерева, є головним виробником органічних речовин. Деревина є цінною сировиною для хімічної переробки. Так, суха перегонка деревини з давніх часів застосовувалася для одержання таких органічних речовин, як оцтова кислота, метиловий спирт, ацетон, феноли. Сьогодні хімічна переробка деревини використовується в паперовій промисловості, у виробництвах целюлози, штучного волокна, кінофотоплівки, етилового спирту та ін
Слайд 5Цінними джерелами різних органічних сполук є також продукти сухої перегонки кам’яного вугілля
Цінними джерелами різних органічних сполук є також продукти сухої перегонки кам’яного вугілля

— коксовий газ, кам’яновугільна смола. Слід згадати також і такі джерела, як горючі сланці й торф.
З кам’яним вугіллям успішно суперничають нафта і природний газ. Наразі світове виробництво продуктів основного органічного синтезу базується на використанні нафти й природного газу (95 %). Вугілля, сланці, торф і деревина забезпечують не більш ніж 5 % споживаної сировини.
Органічні речовини, їх відмінності від неорганічних, елементи-органогени
Органічні сполуки відрізняються від неорганічних низкою характерних особливостей:
✵ майже всі органічні речовини горять або легко руйнуються внаслідок нагрівання з окисниками, виділяючи CO2 (за цією ознакою можна встановити приналежність досліджуваної речовини до органічних сполук);
✵ у молекулах органічних сполук Карбон може бути з’єднаний майже з будь-яким елементом Періодичної системи;
✵ органічні молекули можуть містити послідовність атомів Карбону, з’єднаних у ланцюги (відкриті або замкнені);
✵ молекули більшості органічних сполук не дисоціюють на досить стійкі іони;
✵ реакції органічних сполук протікають значно повільніше й у більшості випадків не завершуються остаточно;
✵ серед органічних сполук дуже поширене явище ізомерії; Ізомері́я — існування сполук, однакових за хімічним складом, але різних за будовою і властивостями. Такі сполуки називають ізомерами.
З кам’яним вугіллям успішно суперничають нафта і природний газ. Наразі світове виробництво продуктів основного органічного синтезу базується на використанні нафти й природного газу (95 %). Вугілля, сланці, торф і деревина забезпечують не більш ніж 5 % споживаної сировини.
Органічні речовини, їх відмінності від неорганічних, елементи-органогени
Органічні сполуки відрізняються від неорганічних низкою характерних особливостей:
✵ майже всі органічні речовини горять або легко руйнуються внаслідок нагрівання з окисниками, виділяючи CO2 (за цією ознакою можна встановити приналежність досліджуваної речовини до органічних сполук);
✵ у молекулах органічних сполук Карбон може бути з’єднаний майже з будь-яким елементом Періодичної системи;
✵ органічні молекули можуть містити послідовність атомів Карбону, з’єднаних у ланцюги (відкриті або замкнені);
✵ молекули більшості органічних сполук не дисоціюють на досить стійкі іони;
✵ реакції органічних сполук протікають значно повільніше й у більшості випадків не завершуються остаточно;
✵ серед органічних сполук дуже поширене явище ізомерії; Ізомері́я — існування сполук, однакових за хімічним складом, але різних за будовою і властивостями. Такі сполуки називають ізомерами.
Слайд 6 ЗАПОВНІТЬ ТАБЛИЦЮ САМОСТІЙНО
ЗАПОВНІТЬ ТАБЛИЦЮ САМОСТІЙНО

Слайд 7 Предмет органічної хімії
Кекулє в 1851 р. визначив органічну хімію як хімію
Предмет органічної хімії
Кекулє в 1851 р. визначив органічну хімію як хімію
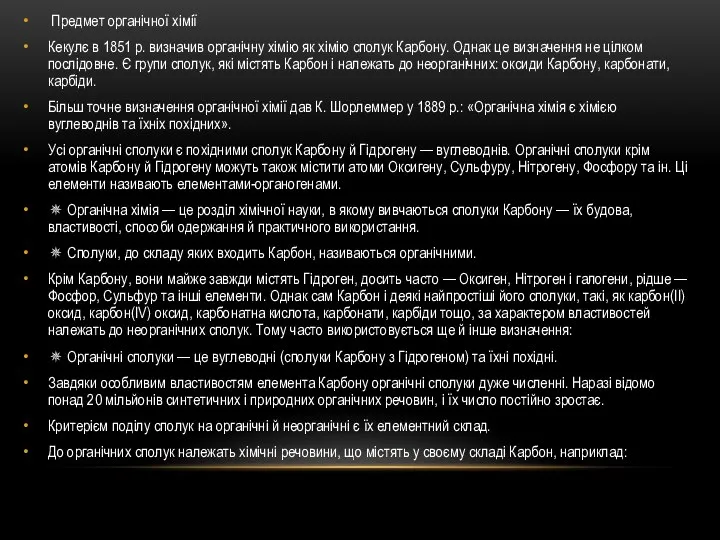
сполук Карбону. Однак це визначення не цілком послідовне. Є групи сполук, які містять Карбон і належать до неорганічних: оксиди Карбону, карбонати, карбіди.
Більш точне визначення органічної хімії дав К. Шорлеммер у 1889 р.: «Органічна хімія є хімією вуглеводнів та їхніх похідних».
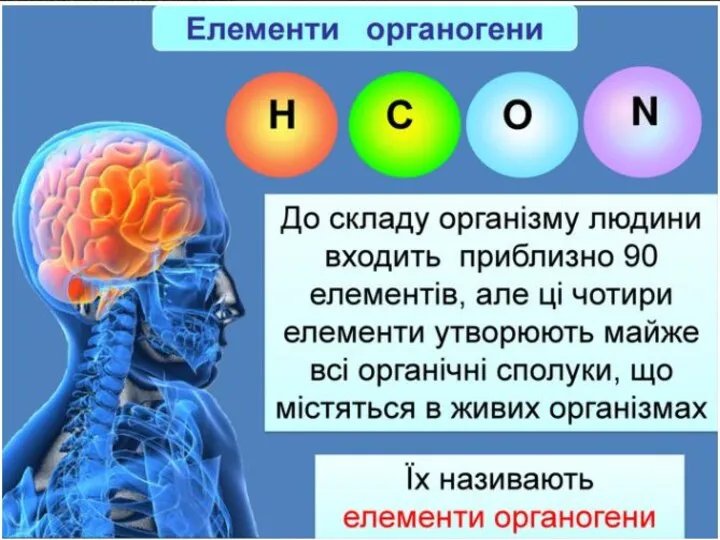
Усі органічні сполуки є похідними сполук Карбону й Гідрогену — вуглеводнів. Органічні сполуки крім атомів Карбону й Гідрогену можуть також містити атоми Оксигену, Сульфуру, Нітрогену, Фосфору та ін. Ці елементи називають елементами-органогенами.
✵ Органічна хімія — це розділ хімічної науки, в якому вивчаються сполуки Карбону — їх будова, властивості, способи одержання й практичного використання.
✵ Сполуки, до складу яких входить Карбон, називаються органічними.
Крім Карбону, вони майже завжди містять Гідроген, досить часто — Оксиген, Нітроген і галогени, рідше — Фосфор, Сульфур та інші елементи. Однак сам Карбон і деякі найпростіші його сполуки, такі, як карбон(ІІ) оксид, карбон(IV) оксид, карбонатна кислота, карбонати, карбіди тощо, за характером властивостей належать до неорганічних сполук. Тому часто використовується ще й інше визначення:
✵ Органічні сполуки — це вуглеводні (сполуки Карбону з Гідрогеном) та їхні похідні.
Завдяки особливим властивостям елемента Карбону органічні сполуки дуже численні. Наразі відомо понад 20 мільйонів синтетичних і природних органічних речовин, і їх число постійно зростає.
Критерієм поділу сполук на органічні й неорганічні є їх елементний склад.
До органічних сполук належать хімічні речовини, що містять у своєму складі Карбон, наприклад:
Більш точне визначення органічної хімії дав К. Шорлеммер у 1889 р.: «Органічна хімія є хімією вуглеводнів та їхніх похідних».
Усі органічні сполуки є похідними сполук Карбону й Гідрогену — вуглеводнів. Органічні сполуки крім атомів Карбону й Гідрогену можуть також містити атоми Оксигену, Сульфуру, Нітрогену, Фосфору та ін. Ці елементи називають елементами-органогенами.
✵ Органічна хімія — це розділ хімічної науки, в якому вивчаються сполуки Карбону — їх будова, властивості, способи одержання й практичного використання.
✵ Сполуки, до складу яких входить Карбон, називаються органічними.
Крім Карбону, вони майже завжди містять Гідроген, досить часто — Оксиген, Нітроген і галогени, рідше — Фосфор, Сульфур та інші елементи. Однак сам Карбон і деякі найпростіші його сполуки, такі, як карбон(ІІ) оксид, карбон(IV) оксид, карбонатна кислота, карбонати, карбіди тощо, за характером властивостей належать до неорганічних сполук. Тому часто використовується ще й інше визначення:
✵ Органічні сполуки — це вуглеводні (сполуки Карбону з Гідрогеном) та їхні похідні.
Завдяки особливим властивостям елемента Карбону органічні сполуки дуже численні. Наразі відомо понад 20 мільйонів синтетичних і природних органічних речовин, і їх число постійно зростає.
Критерієм поділу сполук на органічні й неорганічні є їх елементний склад.
До органічних сполук належать хімічні речовини, що містять у своєму складі Карбон, наприклад:
Слайд 8Це приклади органічних сполук. Рисочками позначені зв,язки. Це називається- структурні формули. Зверніть
Це приклади органічних сполук. Рисочками позначені зв,язки. Це називається- структурні формули. Зверніть
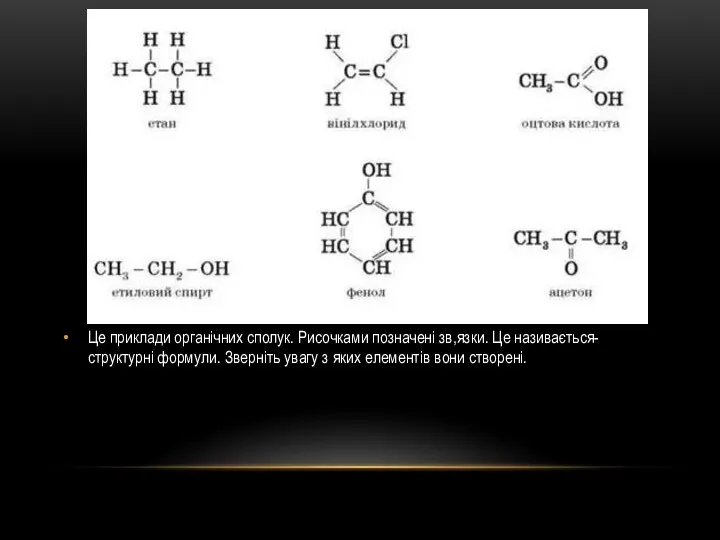
увагу з яких елементів вони створені.


 Номенклатура алкенов. Теория
Номенклатура алкенов. Теория Органическая химия. Введение
Органическая химия. Введение Ковалентная связь. Радикалы
Ковалентная связь. Радикалы Нефть и основные продукты её переработки
Нефть и основные продукты её переработки Уран гексафториді
Уран гексафториді Основной государственный экзамен. Химия 2022. Задание 2
Основной государственный экзамен. Химия 2022. Задание 2 Материаловедение. Технология конструкционных материалов. Диаграмма состояния Fe-Fe3C
Материаловедение. Технология конструкционных материалов. Диаграмма состояния Fe-Fe3C Карбораны. Особенности строения молекулы. Получение и химические свойства
Карбораны. Особенности строения молекулы. Получение и химические свойства Кристаллические решётки
Кристаллические решётки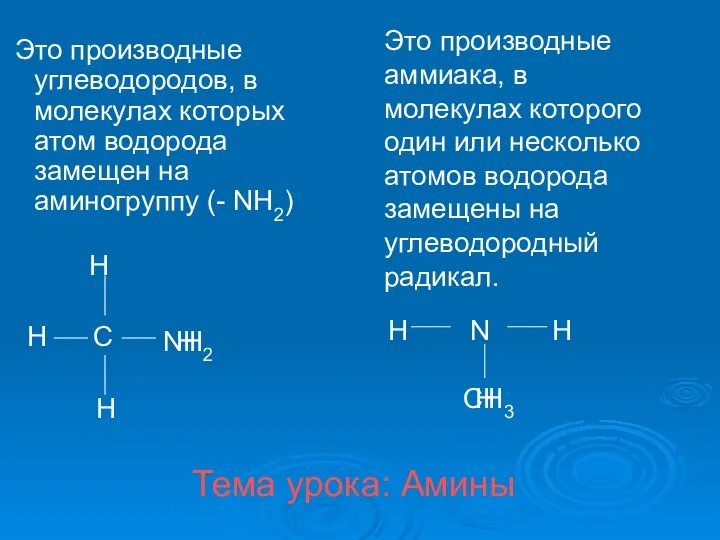 Амины. Классификация аминов
Амины. Классификация аминов Химия. Контроль знаний
Химия. Контроль знаний Основные классы неорганических соединений
Основные классы неорганических соединений Технология получения красного фосфора
Технология получения красного фосфора Составление химических формул методом нулевой суммы
Составление химических формул методом нулевой суммы Ионные уравнения
Ионные уравнения Химия вокруг нас и для нас
Химия вокруг нас и для нас Переработка нефти
Переработка нефти Пути использования активной уксусной кислоты
Пути использования активной уксусной кислоты Прикладная геохимия
Прикладная геохимия Бутилацетат. Химическая формула бутилацетата
Бутилацетат. Химическая формула бутилацетата Изомерия. Виды изомерии
Изомерия. Виды изомерии Термическая обработка. Превращения в стали при нагревании. Перегрев и пережег стали. Видманштеттовая струкрура
Термическая обработка. Превращения в стали при нагревании. Перегрев и пережег стали. Видманштеттовая струкрура Количественный анализ. Титрование
Количественный анализ. Титрование Строение атома
Строение атома ОВР
ОВР ОГЭ №2, вопрос 1-16
ОГЭ №2, вопрос 1-16 Сухой метод определения глюкозы. Глюкометры
Сухой метод определения глюкозы. Глюкометры Пропиловый спирт C3H7OH
Пропиловый спирт C3H7OH