Содержание
- 2. Загадка Очень древний я металл, Счёт столетьям потерял. Был нескромным я не в меру, Тысячи лет
- 3. «Третий лишний». Задание: Решите анаграммы и исключите лишнее. леруогд иксолодр ддрооов золеже углерод кислород водород железо
- 4. Охарактеризуйте Fe как химический элемент, составив предложения со словами и словосочетаниями: Порядковый номер, номер периода ,
- 5. Задание Закончите электронно - буквенную формулу и нарисуйте графическую формулу строения атома железа: Железо(№ 131835)
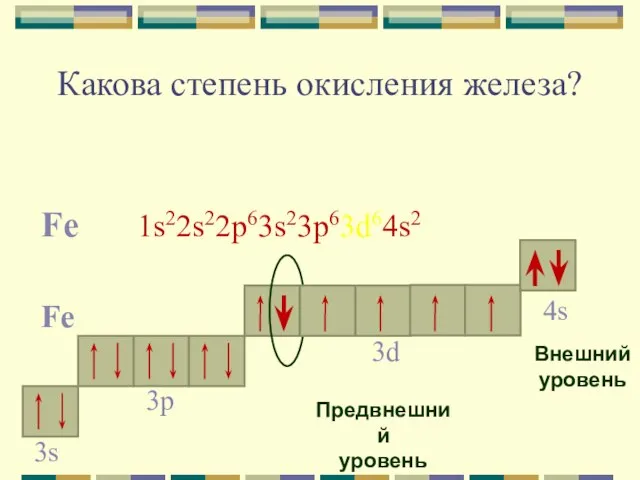
- 6. Какова степень окисления железа? Fe 1s22s22p63s23p63d64s2 Fe 4s Внешний уровень 3d Предвнешний уровень 3p 3s
- 7. Для железа характерны две основные степени окисления: +2, +3. Fe0 - 2e- = Fe+2 Fe0 -
- 8. Задание: Рассмотрите образец металла (№ 131836). Опишите физические свойства металла (№ 131797).. Используя текст учебник, заполните
- 9. Выберите и запишите цифры только тех свойств, которые не относятся к физическим свойствам железа: Серебристо-белый металл
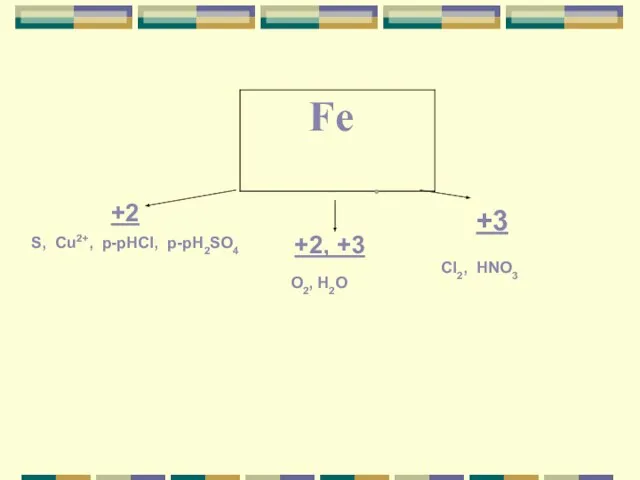
- 10. +2 +2, +3 +3 S, Cu2+, p-рHCI, p-рH2SO4 O2, H2O CI2, HNO3
- 11. Химические свойства железа Взаимодействие железа с хлором Видеофрагмент (№ 54490): 2Fe + 3Cl2 = 2FeCl3
- 12. Химические свойства железа Взаимодействие железа сВзаимодействие железа с Взаимодействие железа с кислородом: Видеофрагмент (№ 131824) Fe
- 13. : Какие из реакций соответствуют схеме Fe+2 → Fe+3 FeCI2 + CI2 = FeCI3 FeCI3 +
- 14. Задание: Расставить коэффициенты в уравнениях 1 и 3 методом электронного баланса, определить окислитель и восстановитель в
- 15. Нахождение в природе В земной коре 5,1% железа, 4 место после кислорода, кремния и алюминия. По
- 16. Нахождение в природе Метеоритное железо(№ 131727) Запишите не менее 4 -х формул соединений железа, встречающихся в
- 17. Природные соединения железа Fe FeS Пирит (железный или серный колчедан) FeCO3 Сидерит Fe2O3*3H2O Лимонит (бурый железняк)
- 18. Генетические связи Fe - ОТ ЖЕЛЕЗА ДО ОКСИДА ЖЕЛЕЗА (- ОТ ЖЕЛЕЗА ДО ОКСИДА ЖЕЛЕЗА (II-
- 19. ПРИМЕНЕНИЕ(№ 207382) Чистое железо способно быстро намагничиваться и размагничиваться, поэтому его применяют для изготовления трансформаторов, электромоторов
- 20. Домашнее задание § 14, с. 76 -78 № 5 с. 82 - всем № 6 с.
- 21. Используемая литература: 1. Горковенко М. Ю. Химия. 9 класс. Поурочные разработки к учебнику О. С. Габриеляна
- 23. Скачать презентацию

















 Структура материалов. Введение в науку о материалах
Структура материалов. Введение в науку о материалах Презентация на тему Алканы
Презентация на тему Алканы  Исследование фармакологических препаратов на хлориды, методом аргентометрии
Исследование фармакологических препаратов на хлориды, методом аргентометрии Подготовка к ЕГЭ
Подготовка к ЕГЭ Дополнительный_материал_11.15_23.09.2022_e4f87550
Дополнительный_материал_11.15_23.09.2022_e4f87550 Распределение электронов в атоме по энергетическим уровням
Распределение электронов в атоме по энергетическим уровням Nanofibers of aluminum oxide
Nanofibers of aluminum oxide Сложные эфиры. Жиры. Мыла
Сложные эфиры. Жиры. Мыла Презентация на тему Состав, строение и свойства стекла и хрусталя
Презентация на тему Состав, строение и свойства стекла и хрусталя  Электролитическая диссоциация
Электролитическая диссоциация Металлы. Общая характеристика ( 9 класс)
Металлы. Общая характеристика ( 9 класс) Галогены. Положение галогенов в ПСХЭ
Галогены. Положение галогенов в ПСХЭ Разработка математического описания расчета октанового числа бензинов каталитического риформинга с групповой кинетикой
Разработка математического описания расчета октанового числа бензинов каталитического риформинга с групповой кинетикой Презентация на тему Ковалентная неполярная связь
Презентация на тему Ковалентная неполярная связь  Аминокислоты. Пептиды. Белки
Аминокислоты. Пептиды. Белки Значение коллодиной химии в производстве
Значение коллодиной химии в производстве Соляная кислота
Соляная кислота Применение алкинов
Применение алкинов Возможности модернизации совместного производства фенола и ацетона кумольным способом
Возможности модернизации совместного производства фенола и ацетона кумольным способом Санитарно-гигиенические показатели питьевой воды
Санитарно-гигиенические показатели питьевой воды Аминокислоты. Химические и физические свойства
Аминокислоты. Химические и физические свойства Получение и реакции пиразина
Получение и реакции пиразина Способы получения металлов
Способы получения металлов Сера. Характеристика химического элемента и простого вещества
Сера. Характеристика химического элемента и простого вещества Спирты и их производные. Применение метанола и этанола
Спирты и их производные. Применение метанола и этанола Периодический закон, 9 класс (1)
Периодический закон, 9 класс (1) Молекулярно-механическое изнашивание
Молекулярно-механическое изнашивание Кислоты. Тест
Кислоты. Тест